Кислородная резка металлов
Основные условия, которые необходимо соблюдать при кислородной резке металлов и сплавов.
- Температура, при которой метал воспламеняется в кислороде, должна быть ниже его температуры плавления. Низкоуглеродистая сталь лучше всего подходит для такого вида резки потому, что температура ее воспламенения примерно 1300 C, а плавления — 1500C. При увеличении содержания углерода в стали, кислородная резка ухудшается, потому что повышается температура воспламенения, и снижается температура плавления.
- При резке высокохромистой стали и алюминия, могут образовываться тугоплавкие оксиды, температура плавления которых больше температуры плавления метала. Что приводит к необходимости использовать специальные флюсы для резки данного метала.
- Для поддержания непрерывного процесса резки, необходимо большое количество тепла, выделяемого при сгорании металла в кислороде. Например, при резки стали 30% тепла выделяется пламенем резака, остальные 70% получаются при сгорании метала.

- Жидкотекучие шлаки, которые образовываются при резки, должны легко выдуваться.
- Что бы избежать неустойчивости и прерывания резки, необходимо, что бы теплопроводность сплавов и металлов была не высокой. Для этого нужно, что бы тепло от шлаков и пламени не отводилось от места резки.
Подогревающие пламя используется для начального подогрева металла. Непрерывный процесс резки обеспечивается подогревающим пламенем, которое на протяжении всей резки подогревает верхнюю часть кромки метала до температуры его воспламенения. Химический состав и толщина металла влияют на необходимую мощность подогревающего пламени.
Мощность подогревающего пламени на прямую зависит от толщины разрезаемого метала. Чем больше толщина металла, тем меньше роль подогревающего пламени. Максимальная эффективность резки получается на расстоянии 2-3 мм от конца ядра пламени.
Для непрерывного окисления металла перемещать резак нужно с такой скоростью, что бы металл успевал окисляться по все толщине.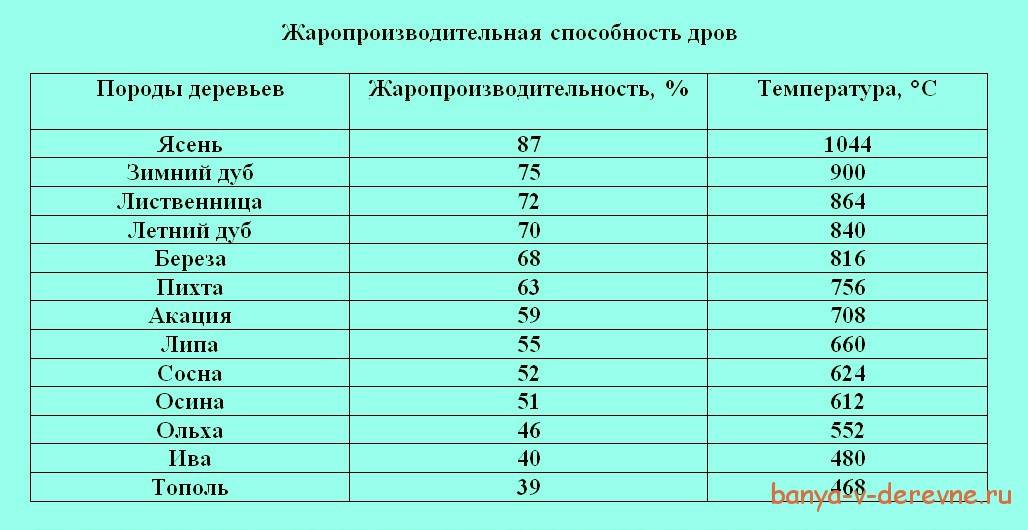 Необходимо также учитывать, что на выдувание окислов при резке, расход кислорода должен быть больше из узкого реза, нежели с широкого. Это объясняется тем, что при узком разрезе шлаки могут быстро сцепляться с кромкой металла, чего нет при увеличении реза, там облегчается удаление шлаков.
Необходимо также учитывать, что на выдувание окислов при резке, расход кислорода должен быть больше из узкого реза, нежели с широкого. Это объясняется тем, что при узком разрезе шлаки могут быстро сцепляться с кромкой металла, чего нет при увеличении реза, там облегчается удаление шлаков.
Условия резки металлов | Сварка металлов
Не все металлы и сплавы поддаются резке окислением. Окислительная резка требует выполнения следующих условий.
Температура воспламенения
Температура воспламенения металла должна быть ниже температуры его плавления. В этом случае металл горит в твердом состоянии; поверхность реза получается гладкой, верхние края кромки реза не подплавляются, продукты горения в виде шлака легко удаляются из полости реза кислородной струей и форма реза остается постоянной.
Этому условию отвечает железо и углеродистые стали. Техническое железо горит в кислороде при температуре 1050 — 1360 °С в зависимости от его состояния (прокат, порошок и др.
Не поддаются резке окислением алюминий и его сплавы. Температуры воспламенения и плавления алюминия соответственно равны 900 и 660 °С. Следовательно, алюминий может гореть только в жидком состоянии, поэтому получить постоянную форму реза невозможно.
Температура плавления
Температура плавления образующихся при резке оксидов и шлаков должна быть ниже температуры плавления металла. В этом случае они становятся жидкотекучими и беспрепятственно удаляются из области реза кислородной струей.
Оксиды в виде FeO, Fe3O4, образующиеся при окислении железа в процессе резки, имеют температуру плавления 1350 и 1400 °С, т. е. ниже температуры плавления железа. Поэтому низкоуглеродистые стали поддаются резке окислением. Стали, содержащие более 0,65% углерода, имеют температуру плавления ниже температуры плавления оксидов железа, и резка их окислением в обычных условиях затруднительна.
Некоторые металлы образуют оксиды с высокими температурами плавления, например оксиды алюминия — 2050 °С, хрома около 2270 °С, никеля 1985 °С, меди 1230 °С.
Эти оксиды, получаемые при резке хромистых и хромоникелевых сталей, меди и ее сплавов, чугунов и др., по сравнению с разрезаемым металлом являются тугоплавкими. Они при обычной окислительной резке не могут быть удалены из области резки, так как закрывают место окисления подогретого до температуры воспламенения металла от струи кислорода, и резка становится невозможной.
Теплоотвод
Металлы должны обладать небольшой теплопроводностью, чтобы не было сильного теплоотвода от места резки, иначе процесс резки прервется.
Примечание. Разрезаемость может оцениваться также и по эквивалентному углероду, определяемому по соответствующей формуле.
Медь, алюминий и их сплавы обладают высокой теплопроводностью по сравнению с железом и сталью; практически не удается сконцентрировать нагрев этих металлов до температуры воспламенения подогревающим пламенем по всей толщине листа. Поэтому указанные металлы не поддаются обычной кислородной резке.
Сущность и основные условия резки металла
Сущность процесса резки. Кислородная резка металла, основана на свойстве железа гореть в струе чистого кислорода, будучи нагретым, до температуры, близкой к температуре плавления.
Кислородная резка металла, основана на свойстве железа гореть в струе чистого кислорода, будучи нагретым, до температуры, близкой к температуре плавления.
Температура загорания железа в кислороде зависит от состояния, в котором оно находится. Так, например, железный порошок загорается при 315° С, тонкое листовое или полосовое железо — при 930° С, а поверхность крупного куска стали — при 1200-1300° С. Горение железа происходит с выделением значительного количества тепла и может поддерживаться за счет теплоты сгорания железа.
Как показал анализ шлака, 30-40% удаленного из реза металла составляет не сгоревшее, а только расплавившееся железо; 90-95% окислов состоят из FeO.
Скорость реакции Fе + О = FеО пропорциональна , где — давление кислорода в месте реакции. При повышении давления кислорода в струе процесс резки ускоряется за счет повышения скорости реакции окисления и за счет более быстрого удаления окислов из места разреза.
Нагревание металла при резке производят газокислородным пламенем.
Кроме подогрева металла до температуры горения в кислороде, подогревающее пламя выполняет еще следующие дополнительные функции:
- подогревает переднюю (в направлении резки) верхнюю кромку реза впереди струи режущего кислорода до температуры воспламенения, что обеспечивает непрерывность процесса резки;
- вводит в зону реакции окисления дополнительное тепло, покрывающее его потери за счет теплопроводности металла и в окружающую среду; это имеет особенно важное значение при резке металла малой толщины;
- создает защитную оболочку вокруг режущей струи кислорода, предохраняющую от подсоса в нее азота из окружающего воздуха;
- подогревает дополнительно нижнюю кромку реза, что важно при резке больших толщин.
Мощность подогревающего пламени зависит от толщины и состава разрезаемой стали и температуры металла перед резкой.
Металл нагревают на узком участке в начале реза, а затем на нагретое место направляют струю режущего кислорода, одновременно передвигая резак по намеченной линии реза. Металл сгорает по всей толщине листа, в котором образуется узкая щель. Интенсивное горение железа в кислороде происходит только в слоях, пограничных с поверхностью режущей струи кислорода, который проникает (диффундирует) в металл на очень малую глубину.
С момента начала резки дальнейший подогрев металла до температуры воспламенения происходит, в основном, за счет тепла реакции горения железа. При чистой, свободной от ржавчины и окалины поверхности, резка может продолжаться и без дополнительного подогрева. Однако лучше продолжать резать с подогревом, так как это ускоряет процесс.
Для заготовительной резки стали применяют кислород чистотой не ниже 98,5-99,5%. С понижением чистоты кислорода резка идет медленнее и требует большего расхода кислорода. Например, в пределах чистоты кислорода от 99,5 до 97,5% понижение чистоты на 1 % увеличивает расход кислорода на 1 м шва на 25-35%, а время резки — на 10-15%.
Скорость резки, толщина металла, расход ацетилена в подогревающем пламени и эффективная мощность пламени связаны между собой зависимостью.
Производительность резки зависит также от распределения подогрева. Применение нескольких подогревающих пламен увеличивает скорость резки по сравнению с таковой при одном подогревающем пламени (при равных расходах ацетилена в обоих случаях). Общий предварительный подогрев металла при резке (до любой температуры) позволяет значительно увеличить скорость резки.
Основные условия резки. Для процесса резки металла кислородом необходимы следующие условия:
- температура горения металла в кислороде должна быть ниже температуры плавления, иначе металл будет плавиться и переходить в жидкое состояние до того, как начнется его горение в кислороде;
- образующиеся окислы металла должны плавиться при температуре более низкой, чем температура горения металла, и не быть слишком вязкими; если металл не удовлетворяет этому требованию, то кислородная резка его без применения специальных флюсов невозможна, так как образующиеся окислы не смогут выдуваться из места разреза;
- количество тепла, выделяющееся при сгорании металла в кислороде, должно быть достаточно большим, чтобы обеспечить поддержание процесса резки;
- теплопроводность металла не должна быть слишком высокой, так как иначе, вследствие интенсивного теплоотвода, процесс резки может прерываться.

Температура — воспламенение — металл
Температура — воспламенение — металл
Cтраница 1
Температура воспламенения металла в кислороде должна быть ниже температуры его плавления. Чугун, большинство высоколегированных сталей и цветных металлов не удовлетворяют этому условию. [1]
Температура воспламенения металла должна быть ниже температуры его плавления. [3]
Температура воспламенения металла в кислороде должна быть ниже температуры его плавления. Чугун, большинство высоколегированных сталей и цветных металлов не удовлетворяют Этому условию. [5]
Температура воспламенения металла оказывает решающее влияние на время задержки воспламенения металлической частицы. При горении в пламени конденсированной системы время задержки воспламенения определяется, в основном, разницей между температурой среды и температурой воспламенения частиц, а также размером частиц. Эта зависимость соответствует влиянию размера частиц на время их прогрева.
[6]
Эта зависимость соответствует влиянию размера частиц на время их прогрева.
[6]
Температура воспламенения металла в кислороде должна быть ниже температуры его плавления. Этому условию удовлетворяет малоуглеродистая сталь, температура воспламенения которой около 1350 С, а температура плавления 1500 С. Чугун, большинство высоколегированных сталей и цветных металлов этому требованию не удовлетворяют. [7]
Температура воспламенения металла в кислороде должна быть ниже температуры плавления; в противном случае металл будет выплавляться раньше и стекать, не успевая сгореть. [9]
Температура воспламенения металла в кислороде должна быть ниже температуры его плавления. Этому условию удовлетворяет низкоуглеродистая сталь, температура воспламенения которой около 1350 С, а температура плавления 1500 С. Высоколегированные стали, чугуны и цветные металлы не удовлетворяют этому, требованию.
[10]
Высоколегированные стали, чугуны и цветные металлы не удовлетворяют этому, требованию.
[10]
Температура воспламенения металла в кислороде должна быть ниже температуры его плавления. Лучше: всех металлов и сплавов этому требованию удовлетворяют низкоутлеродистые стали, температура воспламенения которых в кислороде — около 1300 С, а температура плавления — около 1500 С. Увеличение содержания углерода в стали сопровождается повышением температуры воспламенения в кислороде с понижением температуры плавления. Поэтому с увеличением содержания углерода кислородная резка сталей ухудшается. [11]
Температура воспламенения металла в кислороде должна быть ниже температуры его плавления. Лучше всех металлов и сплавов этому требованию удовлетворяют низкоуглероддстые стали, температура воспламенения которых в кислороде — около 1300 С, а температура плавления — около 1500 С.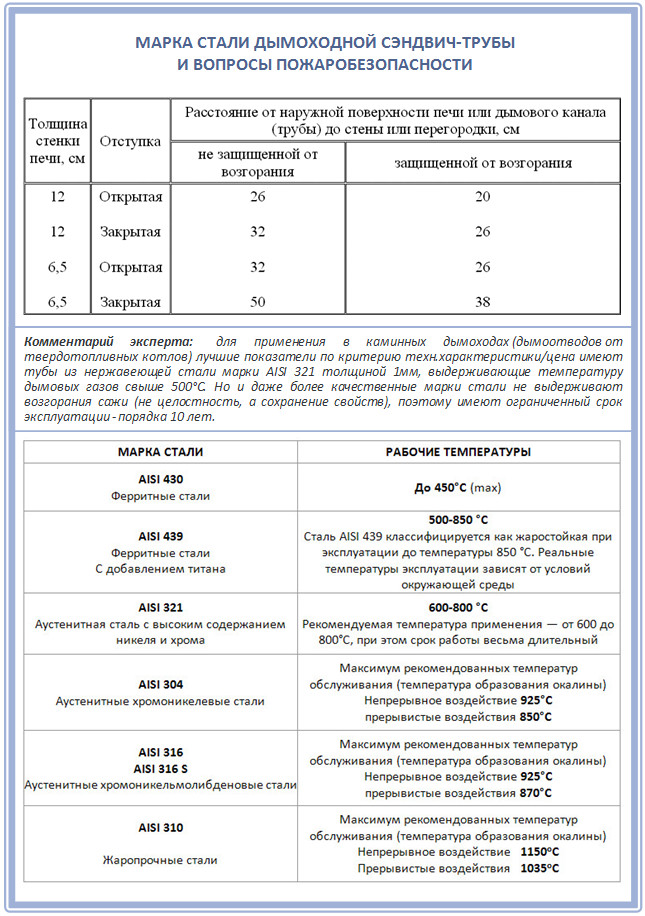 Увеличение содержания углерода в стали сопровождается повышением температуры воспламенения в кислороде с понижением температуры плавления. Поэтому с увеличением содержания углерода кислородная резка сталей ухудшается.
[12]
Увеличение содержания углерода в стали сопровождается повышением температуры воспламенения в кислороде с понижением температуры плавления. Поэтому с увеличением содержания углерода кислородная резка сталей ухудшается.
[12]
Температура воспламенения металла в кислороде должна быть ниже температуры его плавления. Лучше всех металлов и сплавов этому требованию удовлетворяют низкоуглеродистые стали, температура воспламенения которых в кислороде около 1300 С, а температура плавления около 1500 С. Увеличение содержания углерода в стали сопровождается повышением температуры воспламенения в кислороде с понижением температуры плавления. Поэтому с увеличением содержания углерода кислородная резка сталей ухудшается. [13]
Температура воспламенения металла в кислороде должна быть ниже температуры его плавления. В наибольшей степени этому условию удовлетворяет низкоуглеродпстая сталь, температура воспламенения которой около 1350 С, а температура плавления 1500 С. Чугун, большинство высоколегированных сталей и цветных металлов не удовлетворяют этому условию.
[14]
Чугун, большинство высоколегированных сталей и цветных металлов не удовлетворяют этому условию.
[14]
Температура воспламенения металла в кислороде ( температура, при которой металл интенсивно окисляется в кислородной струе), должна быть ниже температуры его плавления. [15]
Страницы: 1 2 3 4
Влияние состава стали на резку
Влияние состава стали на резку
Категория:
Технология кислородной резки
Влияние состава стали на резку
Температура воспламенения стали в кислороде зависит от содержания углерода и других элементов, от состояния ее поверхности (рыхлости, шероховатости), давления и скорости струи кислорода и др.
Чистое железо в виде куска имеет температуру воспламенения в кислороде 1050 °С, а температуру плавления 1539 °С. При содержании в стали 0,7% углерода температура ее воспламенения в кислороде повышается до 1300 °С и достигает температуры плавления этой стали. В этом случае процесс резки затрудняется.
При содержании в стали 0,7% углерода температура ее воспламенения в кислороде повышается до 1300 °С и достигает температуры плавления этой стали. В этом случае процесс резки затрудняется.
Шероховатая поверхность стали облегчает ее воспламенение. Рыхлость материала снижает температуру воспламенения. Например, если прокатное железо интенсивно окисляется при температуре 1050 °С, то железный порошок начинает гореть в кислороде при температуре 315 °С.
При давлении кислорода 25 кгс/см2 и скорости потока 180 м/с температура воспламенения низкоуглеродистой стали в кислороде снижается до 700—750 °С.
При кислородной резке, так же как и при сварке, вблизи места реза образуется зона термического влияния, что способствует образованию трещин при остывании кромок.
При резке нержавеющих сталей возможна межкристаллитная коррозия (выпадение карбидов хрома из раствора) после резки и ржавление. Поэтому кромки этих сталей после резки кислородом часто фрезеруют или строгают на глубину 0,5—3 мм при толщине до 100 мм.
Для некоторых марок высоколегированной стали после резки кислородом применяют термическую обработку для восстановления структуры металла на кромках.
Свойство стали разрезаться кислородом без образования закаленного участка вблизи места резки принято называть разрезаемостью.
Оценка разрезаемости в зависимости от химического состава стали проводится по четырехбалльной системе: 1) хорошо разрезающиеся, 2) удовлетворительно, 3) ограниченно и 4) плохо разрезающиеся стали.
Реклама:
Читать далее:
Режимы резки
Статьи по теме:
Наивысшая температура пламени горелки. Регулировка пламени горелки.
Длина подогревательного пламени зависит от его мощности, т. е. от количества горючего газа, подводимого к пламени, а также от рода горючего газа.
Наивысшая температура пламени горелки.
Температура пламени является одним из важнейших его свойств, от которого зависит скорость резки.
Температура пламени зависит от рода горючего и состава смеси, подаваемой в резак. Она различна для разных зон пламени.
Наиболее высокую температуру пламени дает ацетилен, обеспечивающий быстрый нагрев металла до температуры начала горения. Поэтому ацетилен является наиболее распространенным горючим газом, применяемым при кислородной резке.
Наибольшую температуру (около 3100°С) имеет ацетилено-кислородное пламя на расстоянии 3—4 мм от конца ядра по оси пламени. По мере удаления от ядра температура понижается.
Распределение температуры в нормальном ацетилено-кислородном подогревательном пламени по его длине показано на рис. 1.
Слишком высокая температура, развиваемая ацетилено-кислородным пламенем, часто приводит к оплавлению кромок разрезаемых деталей. Поэтому ацетилен, несмотря на все его преимущества, дает при резке менее чистый рез, чем водород, пары бензина и керосина и другие горючие газы.
Регулировка пламени горелки.
От правильной регулировки подогревательного пламени в значительной мере зависит качество резки. Кислородная резка ведется при нормальном или слегка окислительном пламени.
У резаков с концентрическим расположением мундштуков правильно отрегулированное пламя окружает режущую струю кислорода, при этом внутреннее ядро должно быть симметричным и везде одинаковым по яркости.
Если мундштуки резака сдвинуты, сечение кольцевого канала, из которого вытекает горючая смесь, нарушается и пламя получается односторонним. Таким пламенем резку производить нельзя, так как одна кромка разреза будет сильнее нагреваться, оплавляться и рез получится нечистым. Применение разработанных одним из институтов разъемных самоцентрирующихся мундштуков обеспечивает (вследствие самоцентрирования) симметричную форму пламени.
Очень часто происходит засорение канала, по которому проходит горючая смесь, в результате чего пламя разбивается на отдельные струйки и становится неравномерным. Таким пламенем резать нельзя, так как помимо получения некачественного реза заметно снижается производительность.
Таким пламенем резать нельзя, так как помимо получения некачественного реза заметно снижается производительность.
Регулировка пламени заключается в том, чтобы создать симметричное по отношению к режущей струе кислорода нормальное или слегка окислительное пламя необходимой мощности. Мощность пламени устанавливается в зависимости от толщины разрезаемого металла.
Обычно при правильно установленном давлении и полностью открытых кислородном и ацетиленовом вентилях (на резаке) в зажженном подогревательном пламени есть некоторый избыток ацетилена. Постепенным перекрыванием ацетиленового вентиля достигается нормальное пламя.
Нормальное пламя должно быть создано при не полностью открытых вентилях для возможности дальнейшей регулировки.
Регулировку на слегка окислительное пламя начинают с установления нормального пламени, а затем прибавляют кислород или убавляют ацетилен до тех нор, пока пламя не приобретет требуемой величины.
В правильно отрегулированном пламени (если регулировка производилась при закрытой режущей струе кислорода) после пуска струи давление кислорода подогревательного пламени несколько понижается и пламя становится ацетиленистым. Поэтому окончательную регулировку подогревательного пламени следует вести при открытом вентиле режущего кислорода, а после регулировки вентиль следует закрыть.
Поэтому окончательную регулировку подогревательного пламени следует вести при открытом вентиле режущего кислорода, а после регулировки вентиль следует закрыть.
Если режущий кислород подается в резак по отдельному от подогревательного кислорода шлангу, дополнительная регулировка пламени не требуется.
Статья оказалась полезной?! Поделись с друзьями в социальных сетях!!!
Металлоконструкции после пожара
Последствия теплового воздействия на пожаре на металлы (сплавы) и конструкции из них можно разделить на 6 основных групп, условно расположив их (исходя из температуры наступления) в следующий ряд:
1) деформации;
2) образование окислов на поверхности металла;
3) структурные изменения, сопровождающиеся изменением физико-химических и механических свойств;
4) растворение металла в металле;
5) расплавление и проплавление;
6) горение металла (сплава).
Результаты протекания этих процессов при осмотре места пожара можно зафиксировать визуально или с помощью инструментальных средств, а полученную таким образом информацию использовать при поисках очага пожара.
Рассмотрим последовательно перечисленные выше процессы и возможности экспертного использования полученных сведений. Основное внимание при этом уделим сталям — наиболее распространенному сплаву.
Деформации
Известно, что критическая температура, при которой металлические конструкции теряют несущую способность, составляет: у стальных конструкций — от 440-500 до 550-6000 С; у конструкций из алюминиевых сплавов — около 2500 С.
Потеря несущей способности у металлоконструкции связана, прежде всего, с тем, что она гнётся, деформируется. Эти деформации при осмотре места пожара можно увидеть и нужно оценить.
Заметные деформации у стальных конструкций происходят, как отмечают специалисты, уже при температуре 3000 С. При нагреве до 550-6000 С деформации становятся значительными по величине и в 15-20 % случаев могут привести к обрушению конструкции.
При нагреве до 550-6000 С деформации становятся значительными по величине и в 15-20 % случаев могут привести к обрушению конструкции.
Оценка величины и направленности деформаций даёт определённую информацию об относительной интенсивности и направленности теплового воздействия в тех или иных зонах.
Отметим визуальные признаки, которые следует фиксировать и оценивать.
а) Направление деформации металлических сплавов.
Металлоконструкции и их отдельные элементы деформируются, как правило, в сторону наибольшего нагрева. Кстати, это свойство не только металлов, но и большинства других материалов, например, стекла.
б) Величина деформации.
Очевидно, что величина деформации и конструкции должна быть пропорциональна температуре и длительности её нагрева. Поэтому, казалось бы, на месте пожара наиболее «горячей» зоной можно смело считать ту, в которой металлоконструкции имеют наибольшую деформацию. Однако не все так просто, и наибольшая деформация происходит не всегда там, где имело место наибольшая температура, наиболее интенсивный и продолжительный нагрев. Она может быть и там, где конструктивный элемент несёт более высокую нагрузку или на него действует наибольший изгибающий момент.
Тем не менее на рассредоточенных по зоне горения однотипных и относительно одинаково нагруженных конструкциях оценить величину деформации в сравнении друг с другом очень полезно.
Чтобы количественно оценить степень деформации рассчитывают так называемую величину относительной деформации.
в) Взаимное расположение деформированных (обрушившихся) конструкций.
При осмотре места пожара нужно обращать внимание на взаимное расположение в пространстве, деформированных либо обрушившихся конструкций. Иногда это даёт полезную для установления очага пожара информацию.
г) «Высота излома» вертикальных несущих конструкций.
Не менее полезно при осмотре ряда однотипных вертикальных несущих металлоконструкций сравнивать минимальную высоту, на которой начинается существенная деформация каждой из конструкций. Замечено, что при нагреве в ходе пожара вертикальные несущие металлоконструкции (например, металлические стойки павильонов, ангаров и других подобных сооружений) как бы подламываются на определенной высоте. Чем ближе очаг пожара к конструкции, тем на меньшей высоте на прогревается до критической температуры восходящими конвективными потоками. Таким образом, зафиксировав высоту излома вертикальных конструкций, мы имеем возможность проявить своеобразный «макроконус» — признак направленности распространения горения от очага к периферии.
д) Значительные по величине локальные деформации.
Значительные по величине и чётко выраженные локальные деформации металлоконструкций, особенно балок перекрытия и тому подобных элементов — важный очаговый признак, на который обязательно следует обращать внимание. Данные деформации образуются в начальной стадии пожара, когда в объёме помещения, справа и слева от локально нагреваемого участка ещё холодно, а под данным участком собственно и происходит горение. В противном случае, если деформация балки происходила на стадии развившегося пожара, при относительно равномерной температуре на уровне потолка во всем помещении, то она должна была деформироваться относительно равномерно, с максимальным прогибом по центру, где на балку действует максимальный изгибающий момент.
Образование окислов на поверхности металла
Алюминий и его сплавы.
Известно, что на поверхности алюминия и его сплавов уже при обычных температурах существует микронной толщины окислый слой, который предохраняет алюминий от окисления. Окисел этот выполняет свою функцию и при нагреве алюминиевого изделия на пожаре, вплоть до достижения температуры плавления. Какой либо полезной экспертной информацией из исследования окисного слоя на алюминии извлечь не удается.
Медь.
На поверхности медных изделий до температуры примерно 1000 С присутствует черная пленка окисла (CuO, окись меди). При нагреве выше 1000 С и достаточной длительности образуется пленка закиси меди красного цвета (Cu2О). Это обстоятельство даёт возможность в отдельных ситуациях оценивать, превышала ли температура в зоне, где находится медное изделие, указанную величину.
Сталь.
Если поверхность стального изделия обработанная, гладкая, то первый признак теплового воздействия, который можно обнаружить визуально, — так называемые «цвета побежалости». Они появляются при нагревании стали до температуры 200-3000 С благодаря образованию на её поверхности микронной толщины пленки окисла. Толщина слоя окисла зависит от температуры нагрева (чем больше температура, тем окисел толще), а за счёт интерференции света с изменением толщины пленки меняется и её свет. Таким образом, получается, что цвет пленки окисла («цвет побежалости») зависит от температуры нагрева стали и может использоваться для её примерного определения при исследовании пожара.
Оценка нагрева металлических конструкций по «цветам побежалости» при поисках очага пожара используется редко. Чаще это делается при установлении причины пожара, связанного с трением, локальным перегревом в технологических установках, двигателях и т.д.
Окалина.
Высокотемпературный окисел — окалина — образуется на сталях обыкновенного качества (за время нагрева, характерное для среднего пожара) при температуре от 7000 С и выше.
Рост толщины окалины происходит по параболическому закону; чем больше температура и длительность нагрева, тем она толще. От температуры образования оскалины зависит и её состав.
Она может состоять из трех слоев различных окислов — вустита (оксида двухвалентного железа, FeO), гематита (оксида трехвалентного железа Fe2O3) и магнетита (оксида двух — трёхвалентного железа, Fe3O4). Чем выше температура, тем больше в окалине вустита и меньше гематита. Вустит имеет черный цвет, а гематит рыжий. Это обстоятельство позволяет по цвету окалины и её толщине примерно, ориентировочно оценивать температуру нагрева металлоконструкций.
Низко температурная окалина (700-7500 С), в которой мало вустита, обычно имеет рыжеватый оттенок и достаточно тонкая. Окалина, образовавшаяся при 900-1000 С и более, — толстая и чёрная. Если окисел на поверхности стальной конструкции рыхлый и рыжий — это, скорее всего, вообще не окалина, а обыкновенная ржавчина.
Цвет окалины и её толщина дают возможность примерной оценки температуры нагрева стальных конструкций на пожаре. При этом, однако, не исключены ошибки, поэтому лучше всё-таки проводить инструментальные исследования окалины и определять таким образом не только температуру, но и длительность нагрева конструкции.
Расплавления и проплавления металла
Расплавления и проплавления (образование сквозных отверстий) металлов и сплавов на пожарах, особенно крупных, встречаются не так уж и редко. Можно считать, что это наиболее высокая степень термических поражений конструкций и отдельных предметов.
В 70-х гг. В. Г. Выскребцов (ВНИИСЭ) предложил даже использовать так называемый «метод температур плавлений» для поисков очага пожара. Метод заключался в фиксации мест, где расплавился тот или иной материал, и определении, таким образом, распределения температурных зон по месту пожара. Известно, например, что температура плавления составляет: меди — 10830 С; стали — 1300-14000 С. Таким образом, если в зоне А расплавился алюминиевый провод, что температура там превышала 6000 С, а в зоне Б, где оплавились медные провода, она была, как минимум, 1080-10900 С.
Конечно, фиксировать на месте пожара зоны, где расплавился тот или иной материал, весьма полезно. Но считать это самостоятельным методом установления очага пожара было бы неразумно; да и температурные зоны устанавливаются таким путём достаточно условно — если расплавился алюминий, то это не значит, что температура была 6000 С — она могла быть и 700 — 900 — 1000…0 С.
Кроме того, нужно иметь ввиду, что так называемые «проплавления» в металле могут возникнуть и при температуре, ниже температуры плавления. Возможно это, как минимум по двум причинам. 1) Локальный нагрев тонкого стального изделия (листа, проволоки и т.д.) приводит к образованию слоя окалины, соизмеримого по толщине с самим изделием. Окалина, не обладает достаточной механической прочностью, затем может выкрошиться, и на изделии после пожара обнаружится «дырка». В качестве примера приведём исследование пожара, произошедшего на складе одного из научно-исследовательских институтов. При осмотре места пожара там было обнаружено несколько стоящих вертикально рулонов сетки Рабица, на боку которых имелись вытянутые по вертикали каверны — проплавления сетки на глубину до нескольких сантиметров. Наличие таких проплавлений показалось дознавателю очень подозрительным — ведь температура плавления стали, как указывалось выше, 1300-14000 С, и обеспечить такую температуру могло лишь применение каких-то таинственных спецсредств поджога. Все оказалось, однако, более прозаично. Когда остатки сетки по периметру прожогов исследовали, то оказалось, что проволочки полностью состоят из оксидов железа (неокисленного железа там уже нет), т.е. сталь полностью превратилась в окалину. Для такого процесса не нужна температура 1300-1400, достаточно и 800-9000 С. Однако почему разрушения имеют такой специфический, локальный характер? Оказалось, что над рулонами сетки, на деревянных антрисолях склада хранилось несколько тонн полиэтиленовой пленки. При пожаре полимер плавился, горел, а часть его стекала на расположенные ниже рулоны сетки. Прилипающий к сетке и горящий полимер и привёл в кончном счёте к образованию столь странных «проплавлений». 2) Растворение металла в металле. Расплавленный в ходе пожара более легкоплавкий металл при попадании на металл более тугоплавкий может привести к «растворению» последнего в расплаве первого металла. При чём происходит это при температуре, значительно ниже температуры плавления «тугоплавкого металла».
Про достоинства металлочерепицы написано уже немало статей, наша будет более интересная так как мы расскажем не только про достоинства, а и укажем некоторые особенности данного кровельного материала.
Такой процесс возможен, например, при попадании расплавленного алюминия на медь и её сплавы. Происходит это за счёт образования эвтектического сплава меди с алюминием. Известно, что чистая медь имеет температуру плавления 10830 С. В тоже время эвтектический сплав «медь+алюминий» плавится при температуре 6600 С, а «медь+расплавленная латунь» при 870-9800 С.
Способностью растворяться в расплавленном алюминии обладает также сталь.
Растворение стали в алюминии происходит в три этапа: а) окалинообразование на стали, протекающее под воздействием попавшего на неё расплавленного алюминия; б) химическое взаимодействие образовавшихся оксидов железа с расплавленном алюминием по реакции: Fe2O3+2AL -> AL2O+2Fe+847,8 кДж. Реакция эта, как видно из уравнения, сопровождается сильным тепловыделением, что приводит к дополнительному разогреву в зоне реакции и соответственно интенсификации последней; в) растворение восстановленного из окисла железа в расплавленном алюминии (например, при температуре 9000 С в алюминии может раствориться до 10% Fe).
Конечным результатом протекания указанных реакций может быть проплавление (дырка) в тонком стальном листе, в стенке стальной трубы и т.д. Квалификационным признаком, позволяющим отличить такую дырку от проплавления, возникшего, например, под действием электрической дуги, является характерный контур проплавления (в форме лужицы, потека) и тоненькая каемка алюминия обычно сохраняющаяся по периметру дырки.
Горение металлов и сплавов
Известна способность к горению щёлочных и щёлочноземельных металлов (К, Na, Mg). Менее известно, однако, что в определённых условиях способны гореть (т. е. взаимодействовать с кислородом воздуха) металлы и сплавы, обычно не считающиеся горючими. Примером в данном случае могут быть широко распространенные в качестве конструкционных материалов алюмомагниевые сплавы.
Cтруктурные изменения, сопровождающиеся изменением физико-химических свойств
Изменения структуры металла при нагревании происходят в довольно широком интервале температур, но, как правило, незаметно для глаза. Их надо выявлять инструментальными методами, с помощью соответствующих приборов. В частности, широко используются такие методы как: металлография, магнитные исследования.
Воспламенение и горение черных металлов при высоком давлении и высокой скорости в газообразном кислороде
Симпозиум по кислородным компрессорам и насосам , Атланта, Джорджия, 9–11 ноября 1971 г., Compressed Gas Association, Inc.
M. D. Hersey: Американское общество инженеров военно-морского флота , 1924, Vol. 36. С. 231–243.
Google Scholar
W. C. Reynolds: NASA Tech.Примечание TND-182, октябрь 1959.
Пол Р. Хилл, Дэвид Адамсон, Дуглас Х. Фоланд и Уолтер Э. Брессетт: Меморандум Национального консультативного комитета по исследованиям в области аэронавтики, NACA RM L55L23b.
Л. Э. Дин и У. Р. Томпсон: ARS Journal , июль 1961 г., стр. 917–923.
А. Х. Тенч, Ханс М. Родер и А. Ф. Кларк: Сжигание металлов в кислороде — фаза II: эксперименты по массовому сжиганию , NBSIR 73: 345, декабрь 1973.
Google Scholar
Л. Киршфельд: Archiv Eisenhuttenw. , сентябрь 1962 г., т. 33. С. 617–621.
CAS Google Scholar
Л. Киршфельд: Archiv Eisenhuttenw. , июль 1968 г., т. 39. С. 535–539.
CAS Google Scholar
Л. Киршфельд: Archiv Eisenhuttenw., июль 1968 г., т. 39. С. 823–826.
Google Scholar
Л. Киршфельд: Angew Chem. , 1959, т. 71. С. 663–667.
Артикул CAS Google Scholar
Л. Киршфельд: Metall , февраль 1967 г., Vol. 21. С. 98–102.
CAS Google Scholar
Л.Киршфельд: Металл , 1960, т. 14. С. 213–219.
CAS Google Scholar
Л. Киршфельд: Metall , август 1960, стр. 792–796.
Л. Киршфельд: Archiv Eisenhuttenw. , январь 1961 г., т. 32. С. 57–62.
Google Scholar
Л. Киршфельд: Металл , сентябрь 1961 г., т. 15, стр.873–878.
CAS Google Scholar
П. Л. Харрисон и А. Д. Йоффе: Труды Королевского общества , Vol. 261A, стр. 537–370.
Дж. Дж. Нихарт и С. П. Смит: AMRL-TDR-64-76, Union Carbide Corp., Linde Div., Октябрь 1964 г.
WA Riehl, CF Key и JB Gayle: NASA Tech . Репортаж Р-180.
«Реакционная способность металлов с жидким и газообразным кислородом», DMIC, Battelle Memorandum 163, 15 января 1963 г.
Льюис Гринспен: Review of Scientific Instruments , февраль 1958 г., Vol. 29. С. 172–173.
Артикул CAS Google Scholar
Роберт Дж. Швингхамер и Карло Ф. Ки: NASA TMX-64899, 29 ноября 1974 г.
CF Key, JC Austin и JW Bransford: NASA TMX-64783, сентябрь 1973 г.
DL Pippen and JS Stradling: Material Research and Standards , June 1971, Vol.53. С. 35–53.
Google Scholar
C. F. Key: Materials Research and Standards , June 1971, Vol. 11. С. 28–51.
CAS Google Scholar
C. F. Ключ: Совместимость материалов с LOX — Vol. I, NASA TMX-64711, октябрь 1972 г.
W. R. Blackstone, B. B. Baber и P. M. Ku: Southwest Research Institute, AFAPL TR-67-41, декабрь 1967.
Р.Дж. Швингхамер: NASA TMX-64634, 4 января 1972 г.
Джек Л. Кристиан, Джеймс Э. Чафей, Абрахам Херлих, Джеймс Ф. Уотсон и Уильям Э. Витцелл: Металл Прогресс , апрель 1963 г., стр. 100–103, 122–123.
A. A. Wells: British Welding Journal , сентябрь 1955 г., стр. 392–400.
Х. Бауэр, В. Вегенер и К. Ф. Виндгассен: Cryogenics , июнь 1970, Vol. 10, стр.241–248.
Артикул Google Scholar
Х. Бауэр, В. Вегенер и К. Ф. Виндгассен: Cryogenics , декабрь 1971 г., Vol. 11. С. 469–476.
Артикул CAS Google Scholar
Ф. Э. Литтман, Ф. М. Черч и Э. М. Киндерман: Journal of Less Common Metals , 1961, Vol. 3. С. 367–378.
Артикул CAS Google Scholar
И. Глассман и др.: Ежегодное собрание НАТО AGARD, февраль 1970 г., Материалы конференции № 52, стр. 19 (1–30).
О. Кубащевски и Э. Эванс: Металлургическая термохимия , Pergamon Press, Oxford, 1958.
Google Scholar
К. К. Келли: Бюллетень 584, Горное управление, 1960.
Почему металлы не горят? | Научные вопросы с удивительными ответами
Категория: Химия Опубликовано: 18 февраля 2018 г.
Фейерверк — пример горящего металла.Изображение в общественном достоянии, источник: OSHA.
Металлы горят. Фактически, большинство металлов выделяют много тепла при горении, и их трудно погасить. Например, термит используется для сварки рельсов поездов. Топливом в термите является металлический алюминий. Когда горит термит, атомы алюминия связываются с атомами кислорода, образуя оксид алюминия, выделяя при этом много тепла и света. В качестве другого примера, ручные бенгальские огни используют в качестве топлива алюминий, магний или железо. Пламя бенгальского огня отличается от пламени дровяного огня, потому что металл имеет тенденцию гореть горячее, быстрее и полнее, чем дерево.Это то, что придает зажженному бенгальскому огню характерное искристое пламя. Фактически, большинство фейерверков содержат металлическое топливо. Другой пример: старые лампы-вспышки, используемые в фотографии, были не чем иным, как горящими кусочками магния в стеклянной колбе. Кроме того, твердотопливные ракетные ускорители космического челнока использовали в качестве топлива алюминий. Некоторые металлы, например натрий, горят настолько хорошо, что мы не делаем из них предметы повседневного обихода. Любой бойскаут, который развел огонь, используя стальную вату, может подтвердить, что металл горит.
Тем не менее, вы можете задаться вопросом, почему, если поднести зажженную спичку к алюминиевой фольге, она не загорится.Точно так же, если поставить металлическую сковороду на кухонный огонь, она не загорится. В повседневных ситуациях кажется, что металлические предметы не так сильно горят. Как это возможно, если металлы действительно горят? Здесь задействованы три основных фактора.
Во-первых, если у вас есть твердый кусок металла, трудно поднести атомы кислорода достаточно близко к большинству атомов металла, чтобы они могли вступить в реакцию. Чтобы сжечь металл, каждый атом металла должен подойти достаточно близко к атому кислорода, чтобы соединиться с ним.Для больших кусков металла; как ложки, горшки и стулья; большинство атомов просто слишком глубоко похоронены, чтобы иметь доступ к молекулам кислорода. Кроме того, металлы не испаряются легко. Когда вы сжигаете кусок дерева или восковую свечу, частицы топлива легко испаряются, а это означает, что при небольшом нагреве они вылетают в воздух, где у них есть лучший доступ к атомам кислорода. Напротив, твердые металлы имеют тенденцию иметь свои атомы очень плотно связанные друг с другом, а это означает, что гораздо труднее использовать тепло для испарения металла.Кроме того, органические материалы, такие как дерево или ткань, содержат много собственного кислорода, тогда как сырые металлы — нет. Это одна из причин, по которой металлическую ложку намного труднее обжечь, чем деревянную, хотя обе они состоят из больших кусков материала.
Помня об этом факте, все, что нам нужно сделать, это вручную разбить атомы металла на части, чтобы они лучше горели. На практике это означает измельчение металла до мелкого порошка. При использовании в качестве топлива в коммерческих продуктах и промышленных процессах металлы обычно имеют форму порошка.Хотя, даже если вы измельчили металлический блок до порошка, он все равно не будет гореть так эффективно, как если бы вы просто использовали кислород из окружающего воздуха. Проблема в том, что воздух на самом деле не содержит столько кислорода. Воздух в основном состоит из азота. Лучше всего подмешивать кислород прямо в порошок. Сырой кислород не будет работать так хорошо, потому что это газ при комнатной температуре, который улетает. Вместо этого к металлическому порошку можно примешать твердые соединения, содержащие слабосвязанные атомы кислорода.Таким образом, атомы кислорода могут стабильно сидеть рядом с атомами металла, готовые вступить в реакцию. Такой подход — наиболее эффективный способ заставить металлы хорошо гореть. Например, термит — это просто алюминиевый порошок (топливо), смешанный с оксидом железа (источником кислорода).
Вторая причина того, что обычные металлические предметы не горят так хорошо, заключается в том, что металлы обычно имеют более высокую температуру воспламенения. Поскольку атомы в типичном металле так прочно связаны друг с другом, требуется больше энергии, чтобы разбить их и освободить, даже если атомы кислорода находятся рядом с ними.Пламя свечей, спичек, костров и кухонных плит просто не нагревается настолько, чтобы воспламенить большинство металлов, даже если металл находится в идеальной порошковой форме. Для воспламенения большинства металлов необходимо использовать химические реакции, приводящие к более высоким температурам. Например, горение полосок магния можно использовать для воспламенения термитов.
Последняя причина того, что обычные металлические предметы не горят так хорошо, заключается в том, что металлы, как правило, являются отличными проводниками тепла. Это означает, что если пятно на металлическом предмете начинает накапливать некоторое количество тепла, тепло очень быстро течет через металл к более холодным частям предмета.Это затрудняет накопление достаточного количества тепла в одном месте для достижения температуры воспламенения. Даже если у вас есть факел, работающий при достаточно высокой температуре, трудно использовать факел для зажигания куска металла, потому что тепло продолжает уходить через металл.
Таким образом, поскольку большинство атомов в твердом куске металла не имеют доступа к атомам кислорода, потому что металлы имеют высокую температуру воспламенения и поскольку металлы являются хорошими проводниками тепла, они не горят очень хорошо в повседневных ситуациях.Идеальный способ заставить металл гореть — это измельчить его в порошок, смешать с окислителем, удержать его так, чтобы тепло не могло уйти, а затем применить устройство для зажигания с высокой температурой.
Темы: атом, атомы, горение, горение, огонь, металл, металлы
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно.Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом.Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
металлов | Бесплатный полнотекстовый | Сжигание металлов в атмосфере, обогащенной кислородом
С развитием технологий металлы должны соответствовать все более строгим требованиям, применяемым в экстремальных условиях. Большинство металлов демонстрируют явление, которое отличается от окисления или плавления, но похоже на горение дерева и нейлона в обогащенной кислородом атмосфере, называемое горением металлов [1].Поэтому металлы, используемые в атмосфере, обогащенной кислородом, могут воспламениться. Некоторые металлические материалы трудно воспламенить на воздухе, но они сильно горят или даже достигают предела взрываемости в атмосфере, обогащенной кислородом. Когда происходит возгорание, это приводит к серьезным последствиям. В двигателях на жидком кислороде / керосине произошла серия катастрофических аварий. Например, в 1980 году на испытательном полигоне Космического центра Джонсона произошел взрыв, вызванный возгоранием вторичного алюминиевого клапана, когда давление кислорода достигло 6000 фунтов на квадратный дюйм (41.4 МПа). Другой случай произошел в Центре космических полетов им. Маршалла в 1992 году, когда прокладки и поршни из нержавеющей стали 316 сгорели в атмосфере с давлением кислорода 35 МПа, что привело к взрыву испытательного стенда. активно работал над борьбой с кислородными пожарами в экспериментах и производстве. Методы испытаний на горение металлов можно проследить еще в 1921 году, когда Джон. К. Маббс проверил несколько материалов (твердые каучуки, волокна и металлы) на 13 баллов.Сжатие 8 МПа. При использовании жидкого кислорода в ракетах совместимость материалов с кислородом является проблемой для надежности и безопасности ракетных двигателей. В результате Американское общество по испытанию материалов (ASTM) организовало Комитет G-4 для написания стандартов для испытаний и выбора материалов для работы с кислородом в 1975 году [2]. Национальное управление по аэронавтике и исследованию космического пространства (НАСА) приложило большие усилия для разработки информации о совместимости материалов с кислородом.НАСА провело ряд испытаний для измерения совместимости, и наиболее распространенными из них являются испытания на механическое воздействие жидким кислородом при атмосферном давлении и испытания на механическое воздействие кислорода под высоким давлением (представленные и подробно описанные в разделе «Методы испытаний») [3]. Хаст и Кларк и др. сообщили о воспламеняемости некоторых чистых металлов [4], а исследования показали, что медь показывала температуру воспламенения около 1030 ° C. Эта температура примерно на 60 ° C ниже точки плавления, и он не воспламеняется до точки плавления, когда давление кислорода ниже 34.5 МПа. Поэтому считается, что медь трудно воспламеняется. Сообщалось, что железо воспламеняется при 930 ° C, что на 600 ° C ниже его точки плавления. Другие сообщили, что температура воспламенения железа составляла 1315 ° C, что также явно было ниже точки плавления [5]. В результате, даже при атмосферном давлении, сопротивление горению железа низкое. Дзюнъити Сато, японский исследователь, изучал воспламеняемость железа в атмосфере высокого давления, обогащенной кислородом [6]. Он обнаружил, что когда горячее железо горит в кислороде, оксид и естественная конвекция влияют на свойства горения.Химические свойства магния были очень активными, а сплавы Mg были склонны к окислению и горению. Температура воспламенения чистого магния на воздухе составляла около 630–640 ° C [7,8,9,10]. Некоторые элементы могут напрямую улучшить температуру воспламенения, например Er [11,12], Gd [13], Y [14,15,16] и другие редкоземельные элементы [17,18], но основные легирующие элементы Mg, такие как Al [16,19], Zn [20], Mn [21] и Cd [22,23], снижают температуру воспламенения. Например, температура воспламенения достигла 500 ° C, когда к сплавам Mg было добавлено 20 мас.% Al [19], и Zn также снизил температуру воспламенения сплавов Mg; его эффект был меньше, чем у Al [20].Алюминий показал температуру воспламенения выше, чем его точка плавления, которая была описана как точка плавления оксида алюминия (2050 ° C) [4,5]. Было обнаружено, что никель воспламеняется при его температуре плавления [4,5]. Серебро невозможно воспламенить ни при каком давлении кислорода [4,5]. Изучены наиболее основательные работы в этой области. Состав металлических материалов, структура оксида и фазовое превращение были важными составляющими воспламеняемости. Дрейзин сообщил о фазовом превращении в процессе горения [24].Результаты экспериментов показали, что реакция и кислород в твердом растворе вызывают фазовое превращение. Тайал и Уилсон изучали взаимосвязь между составом и воспламеняемостью бинарного сплава на основе никеля [25]. Они обнаружили, что порог давления сильно изменился после добавления легирующих элементов с различным содержанием. Нихарт и Смит обнаружили, что никель, латунь и инконель 600 (76Ni15Cr8Fe) показали отличные свойства сопротивления горению, но свойства аустенитной нержавеющей стали и алюминия были относительно плохими [26].Киршфельд и Миллер сравнили сопротивление горению нескольких распространенных сплавов. Они обнаружили, что Monel 400 (66,5Ni31,5Cu) имеет лучшую стойкость к горению, за ним идут нержавеющие стали 304, а стойкость к горению серого чугуна лучше, чем углеродистых сталей [27,28]. Титан может воспламеняться на воздухе при температуре около 1600 ° C из-за его низкой теплопроводности, высокого сродства к кислороду и высокой теплоты сгорания [29,30,31,32]. Характеристики горения различных титановых сплавов, таких как TC4 [33,34,35], TC11 [36,37] и Ti40 [38,39], были изучены методом трения.Результат показал, что контактная сила и концентрация кислорода, соответствующая воспламенению, подчиняются параболической зависимости [36,37,38]. Все характеристики горения можно суммировать в виде трех моделей горения, называемых жидкофазной моделью горения, паровой моделью горения и смешанной моделью горения [40]. В модели горения жидкой фазы энергия, обеспечиваемая промотором, расплавляла конец образца, и реакция окисления между жидким образцом и кислородом происходила в плавящейся оксидной массе.В случае модели горения в паровой фазе реакция окисления между металлическим паром и кислородом происходила в газовой фазе вокруг расплавленной массы. Модель смешанно-фазового горения представляла собой смесь двух моделей.Аварии показывают, что горение металлов в атмосфере, обогащенной кислородом, представляет собой новый вид отказа без каких-либо предварительных мероприятий, что приводит к серьезным ограничениям на их применение. Чтобы понять теоретические основы и оценить безопасность эксплуатации, в этой статье обсуждается краткий обзор поведения металлов при горении.
ПРОЦЕССЫ СГОРАНИЯ МЕТАЛЛОВ. Отчет лаборатории аэронавтики № 473 (Технический отчет)
Глассман, И. ПРОЦЕССЫ СГОРАНИЯ МЕТАЛЛОВ. Отчет лаборатории аэронавтики № 473 . США: Н. П., 1959.
Интернет. DOI: 10,2172 / 4229886.
Глассман, И. ПРОЦЕССЫ СГОРАНИЯ МЕТАЛЛОВ.Отчет лаборатории аэронавтики № 473 . Соединенные Штаты. https://doi.org/10.2172/4229886
Глассман И. Сб.
«ПРОЦЕССЫ СГОРАНИЯ МЕТАЛЛОВ. Отчет № 473 лаборатории аэронавтики». Соединенные Штаты. https://doi.org/10.2172/4229886. https://www.osti.gov/servlets/purl/4229886.
@article {osti_4229886,
title = {ПРОЦЕССЫ СГОРАНИЯ МЕТАЛЛОВ.Отчет Лаборатории аэронавтики № 473},
author = {Glassman, I},
abstractNote = {Поскольку легкие металлические элементы, несомненно, будут играть все большую и большую роль в качестве топлива в современных химических и ядерно-химических силовых установках, интерес к их характеристикам горения растет. Здесь представлены некоторые предварительные выводы о характеристиках горения. Эти выводы основаны на фундаментальных физических соображениях, а не на экспериментальных результатах.Также предлагается аналитический подход к расчету скорости горения металлов. Этот подход отличается от диффузионно-капельного подхода тем, что он включает в себя параметры обратной связи излучения и потерь. Такие условия могут быть важны при высоких температурах диффузионной пленки, окружающей горящий металл. (auth)},
doi = {10.2172 / 4229886},
url = {https://www.osti.gov/biblio/4229886},
журнал = {},
номер =,
объем =,
place = {United States},
год = {1959},
месяц = {8}
}
Воспламенение и горение черных металлов при высоком давлении и высокой скорости в газообразном кислороде (Журнальная статья)
Бейтс, К. Э., Рен, Дж. Э., Монро, Р., и Груш, К. Д. Воспламенение и горение черных металлов при высоком давлении и высокой скорости в газообразном кислороде . США: Н. П., 1979.
Интернет. DOI: 10.1007 / BF02833991.
Бейтс, К.Е., Рен, Дж. Э., Монро, Р., и Груш, К. Д. Воспламенение и горение черных металлов при высоком давлении и высокой скорости в газообразном кислороде . Соединенные Штаты. https://doi.org/10.1007/BF02833991
Бейтс, К. Э., Рен, Дж. Э., Монро, Р., и Груш, К. Д.Пт.
«Воспламенение и горение черных металлов при высоком давлении и высокой скорости в газообразном кислороде». Соединенные Штаты. https://doi.org/10.1007/BF02833991.
@article {osti_6007122,
title = {Воспламенение и горение черных металлов при высоком давлении и высокой скорости в газообразном кислороде},
author = {Бейтс, К. Э. и Рен, Дж. Э. и Монро, Р. и Груш, К. Д.},
abstractNote = {Определены условия воспламенения - горения нескольких черных металлов, включая AISI 1025, AISI 4140, высокопрочный чугун и нержавеющие стали 304, 410, 17-4 PH и CA15.Условия кислорода включали скорость приблизительно 430 метров в секунду (1400 футов в секунду) и давление от 20 до 68 атм (от 300 до 1000 фунтов на квадратный дюйм). Когда 1025 стальных образцов были разрушены в атмосфере кислорода 68 атм (1000 фунтов на кв. Дюйм), 427 м / с (1400 футов / с), было обнаружено, что эта сталь воспламеняется и горит при номинальной температуре около 480 ° С / К (400 ° С / Ф). . В аналогичных условиях AISI 4140 воспламеняется при температуре около 590 ° C / ° C (600 ° / ° F), а ковкий чугун воспламеняется при температуре 530 ° C / ° C (200 ° C / ° F) или ниже.Нержавеющая сталь (304, 17-4 PH и CA15) воспламеняется при температуре около 590 ° C / ° C (600 ° C / ° F), а нержавеющая сталь 410, которая казалась более устойчивой к возгоранию, воспламенялась при температуре около 645 ° C. sup 0 / K (700 / sup 0 / F). Температура воспламенения увеличивалась для всех материалов по мере снижения давления кислорода.},
doi = {10.1007 / BF02833991},
url = {https://www.osti.gov/biblio/6007122},
journal = {Дж. Матер. Energy Syst .; (США)},
number =,
объем = 1: 1,
place = {United States},
год = {1979},
месяц = {6}
}
Вот как горит стальная вата (и почему это похоже на смерть криптона)
Эта царапающая стальная вата, которая очищает ваши грязные сковороды, — это больше, чем трудолюбие; когда горит огонь, он просто великолепен, как показал пользователь Reddit ЧазДодж в недавнем видео, в котором жилистая горящая дымка выглядит как смерть планеты Криптон.
Хотя это не взрыв, вызванный цепной ядерной реакцией — а-ля Криптон — световое шоу, создаваемое горящей стальной ватой, является результатом высокоскоростного окисления.
Вот как это работает: каждый раз, когда что-то горит, вы видите окисление. Это означает, что атом, молекула или ион теряют один или несколько электронов. Ржавчина, например, возникает, когда кислород попадает в железо, и в этом процессе железо теряет электроны и образует оксид железа. Ржавчина — это медленная версия реакции горящих (окисляющих) металлических полос, из которых состоит стальная вата, наблюдаемая в сообщении Reddit.[Могут ли люди спонтанно воспламениться?]
Тем не менее, мы используем кухонную утварь из нержавеющей стали (которая содержит железо), не ожидая, что она воспламенится от случайной искры. Что дает?
Причина, по которой железный блок, такой как посуда, не загорается, заключается в том, что площадь поверхности мала по сравнению с объемом, сказал Live Science Джейсон Бенедикт, доцент химии в Университете Буффало. Ржавое железо на самом деле выделяет некоторое количество тепла в реакции, но его очень мало.Кроме того, большой железный блок может поглотить и рассеять большую часть этой тепловой энергии до того, как температура блока повысится. (Вы можете увидеть этот эффект, нагревая металлическую ложку при перемешивании макаронных изделий — маленькая ложка очень быстро становится слишком горячей, чтобы ее держать, в то время как большая ложка занимает больше времени.)
Стальная вата, с другой стороны, состоит из большого количества тонкие нити, и поэтому гораздо больше атомов железа контактирует с кислородом воздуха. Когда вы добавляете тепло (как от пламени), вы добавляете энергии утюгу, и это увеличивает вероятность его реакции с другими элементами.
«Когда вы добавляете тепло, вы преодолеваете энергетический барьер, чтобы реакция происходила быстрее», — сказал Бенедикт. Как только эта реакция начнется, и поскольку она сама генерирует тепло, она нагревает соседние атомы. В блоке железа тепло передается многим другим атомам железа. Но в тонком железном волокне меньше твердого материала, способного поглощать его (воздух поглощает тепло, но намного эффективнее, чем твердые частицы), поэтому он продолжает гореть. Продуктом горения являются частицы ржавчины или оксида железа, так же как продукт горения дерева — черный пепел (или углерод).
Контакт с кислородом имеет решающее значение для того, насколько быстро и насколько горячо горит железо в стальной вате — среда с чистым кислородом делает пламя намного горячее, и утюг горит быстрее. (В то время как стальная вата часто покрыта другими химическими веществами — например, порошковым мылом — горит и смешивается с кислородом только железо.)
Воздух содержит только около 20 процентов кислорода, поэтому горение происходит с половинной скоростью это похоже на взрыватель динамита из мультфильма. Вот что происходит на видео — кислорода достаточно, чтобы сжечь железо, но недостаточно, чтобы он вспыхнул сразу.Опять же, можно провести аналогию с деревом: подуйте небольшое пламя, и дополнительный кислород может заставить дерево гореть быстрее, в то время как если вы закроете вентиляционные отверстия на старомодной дровяной печи, огонь погаснет до тлеющих углей и сгорит еще больше. медленно.
Именно поэтому порошковые металлы легко горят и поэтому используются при сварке. Хороший пример — термит. Термит представляет собой смесь порошка железа и алюминия, который при достаточном нагревании начинает реагировать с кислородом и гореть при высокой температуре — достаточной для расплавления металла и сварки.Термит также появляется четвертого июля — это ингредиент в составе бенгальских огней.
Примечание редактора: Эта статья была обновлена, чтобы указать, что окисление — это потеря электронов, а не получение кислорода, как было заявлено ранее.
Первоначально опубликовано на Live Science.
.