Использование и применение формул массы через плотность и объём
Физика — наука невероятно увлекательная, если разобраться, что там к чему. А формулы в ней отражают реальные физические процессы, только в цифрах. И если вы будете понимать, почему формула именно такова, то учиться будет много легче. Но все сразу рассказать невозможно, и сегодня мы разберемся, как произвести нахождение массы через плотность и объём.
Прежде, чем приступить к изучению формул массы, плотности и объёма, следует уточнить некоторые детали:
- Во-первых, объём вещества зависит от температуры. При нагревании твёрдое вещество расширяется, при низкой температуре уменьшается. Есть также особые моменты, как в случае с жидким водородом. Он не может существовать при высокой температуре, потому что превратится в газ.
- Во-вторых, разные организации и страны имеют свои стандарты условий, при которых проводятся измерения. Иными словами, числовой показатель плотности одного и того же вещества в разных странах будет отличаться. Поэтому, прежде чем утверждать, что показатели неверные или правильные, следует уточнить условия, при которых эти показатели были получены.
- В-третьих, помимо температуры, на фактор объёма могут влиять и такие показатели, как атмосферное давление. Оно особо важно при измерении плотности газов, так как на твёрдые вещества это практически не влияет.
Формула и удивительная история её возникновения
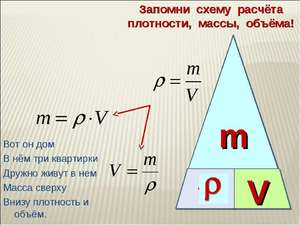
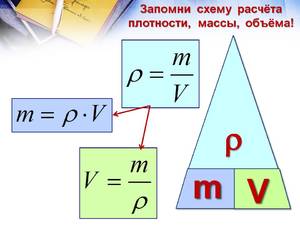
Самая обычная формула для большинства случаев имеет вид: m = pV , где m – масса тела, p и V – плотность вещества и его объём, занимаемый в пространстве соответственно. Можно, конечно, не заморачиваться и посчитать всё на онлайн-ресурсах, но знать формулу всё же полезно. Соответственно V = m / p , p = m / V .
Самое интересное – это то, что формулу нашёл мужик, который бегал голышом по улице и был при этом другом царя. Интересно? Тогда следующие три абзаца для вас.
Был в Древней Греции такой царь-тиран, как Гиерон II. Он начал подозревать, что его корону сделали не из чистого золота и ювелиры его облапошили. Но Гиерон не знал, как можно это доказать. Тогда он обратился к умнейшему человеку того времени – Архимеду. Получив приказ разобраться с делами государственной важности, Архимед день за днём стал искать решение вопроса.
Ох, и нелёгкая же задачка выпала учёному. Ведь на то время не было ни нужных формул, ни современных девайсов, ни гугла, чтобы быстренько найти решение. И вот однажды, придя в баню и погрузившись в неё, Архимед заметил, что выливающаяся вода равна по объёму тому, что погружено в воду.
Эврика! – Прокричал Архимед и нагишом поспешил в свою лабораторию проводить опыты. Учёный сложил все данные в своей голове и позже проделал следующий опыт: он взял корону и опустил её в воду. Затем он взял кусок золота такого же веса и опустил его также в воду. Объём вытесненной воды получился разным. Если бы корона была сделана из чистого золота, то её объём и слитка совпали. Это доказывало то, что ювелиры обманули царя. Кто бы мог подумать, что одно из величайших открытий появилось благодаря обманщикам, тирану и учёному.
Обозначения и термины
Далее будет приведён список понятий и их определение в условиях понятий об измерениях плотности:
- Масса – плотность тела, помноженная на его объём, занимаемый в пространстве. Это также величина, определяющая силу воздействия гравитационного поля на объект.
- Объём – физическая величина, характеризующая количество пространства, занимаемое объектом.
- Плотность определяет то, какое количество вещества умещается в объёме при определённом весе в стандартных условиях.
- Нормальные/стандартные условия в разных организациях имеют свои значения. К таким условиям относятся температура окружающей среды, атмосферное давление и в отдельных случаях прочие параметры.
- Атмосферное давление – понятие, применяемое больше для газов, так как на их объём имеет большое влияние, нежели на твёрдые вещества. Атмосферное давление можно определить как силу, с которой воздействует воздух на Землю под действием гравитационного поля.
- Температура – физический показатель степени нагрева вещества. Чем больше температура, тем больше объём тела.
Примеры решения задач
Прежде чем приступить к примерам, следует понимать, что если данные даны в килограммах и кубических сантиметрах, то нужно либо сантиметры перевести в метры, либо килограммы перевести в граммы.
Задача 1. Найти массу тела, состоящего из вещества, плотность которого равна 2350 кг/м³ и имеет объём 20 м³. Применяем стандартную формулу и с лёгкостью находим значение. m = p*V= 2 350 * 20 = 47 000 кг.
Задача 2. Уже известно, что плотность чистого золота без примесей равна 19,32 г/см³. Найти массу драгоценной цепочки из золота, если объём составляет 3,7 см³. Воспользуемся формулой и подставим значения. p = m / V = 19,32/3,7 = 5,22162162 гр.
Задача 3. На склад поставили металл с плотностью 9250 кг/м³. Масса составляет 1,420 тонн. Нужно найти занимаемый металлом объём. Тут нужно сначала перевести либо тонны в килограммы, либо метры в километры. Проще будет воспользоваться первым методом. V = m / p = 1420/9250 = 0.153513514 м³.
Зачем и кому нужно знать эти формулы
В любой стране есть стандарты, по которым производится продукция. Неважно, какая это отрасль – пищевая, химическая или другая. Стандарты также могут быть мировыми. Так вот для того чтобы выпускаемая на заводах продукция соответствовала этим стандартам и нужны знания о плотности, массе и объёме.
Но зачем кому-то придерживаться чьих-то правил? Для начала, эти правила взяты не с потолка. К этому пришли разные бизнесмены со всего мира и нашли оптимальное решение, удовлетворяющее как производителей, так и конечных пользователей продукта. Если бы все выпускали продукцию как им вздумается, то людям было бы очень тяжело выбрать производителя. Ведь даже сейчас, со всеми стандартами и ГОСТами выбор просто огромный.
Кроме того, игнорируя физику и математику, можно выработать продукцию себе же в убыток или сделать продукцию, которая не оправдает ожиданий и будет выглядеть не так, как задумывал производитель. Есть и другие ситуации, где необходимы знания подобного рода – при подсчёте планируемого объёма, который займёт продукция на складе; вес продукции, которую нужно будет перевести и т.д.
Эти знания могут потребоваться инженерам, технологам, конструкторам и прочим профессиям, чья деятельность связана с физическими материалами. Конечно, для простого обывателя эти знания могут и не пригодиться. Однако, стоит вспомнить про случай с Архимедом и тогда вы поймёте, что знания – защита от обмана и настоящая сила!
Видео
В видео очень подробно объясняется, как рассчитать массу и объем тела по его плотности.
Что такое масса в физике? Виды массы, формулы, масса в современной физике :: SYL.ru
Масса в физике является одним из основных понятий, которое используется во многих законах динамики и статики. Поэтому необходимо четко разобраться, что это за величина. В данной статье рассматривается подробно вопрос, что такое масса в физике. Итак, приступим.
Виды, значение
Что такое масса в физике? Кратко можно сказать, что под этим термином понимают физическую величину, присущую материи. Она определяет ее гравитационные, инерционные и энергетические свойства. Масса измеряется в килограммах в системе СИ.
Проявляет себя эта величина несколькими способами. Во-первых, существует так называемая инерционная масса. Она определяет возможность изменять скорость тела при воздействии внешней силы на него и рассчитывается по такой формуле: m=F/a. Где a — ускорение, которое возникает в результате действия силы F. Чем больше инерционная масса, тем сложнее разогнать тело и труднее остановить его.
Еще одной формулой, которая дает ответ на вопрос, как найти в физике массу (инерционную), является следующая: m=p/v. Где p — импульс тела, v — скорость.
Во-вторых, следует сказать о гравитационной массе. Что такое в физике обозначает этот термин? Это величина, которая является коэффициентом пропорциональности в формуле для силы гравитационного притяжения между двумя телами. Эта формула называется законом всемирного тяготения, записывается так: F=G*m1*m2 /r2. Здесь r — расстояние между телами, G — постоянная гравитации. Массы m1 и m2 показывают интенсивность силы притяжения F.
Наконец, в-третьих, масса — это величина, описывающая энергию, заключенную в телах. Интерпретация этих величин как единой материи стала возможной благодаря появлению теории относительности Эйнштейна и развитию атомной отрасли промышленности.
В настоящее время в результате анализа большого количества экспериментальных данных доказано, что все описанные виды массы являются одной и той же характеристикой. Например, разница между инерционной и гравитационной величиной находится в области погрешности измеряемых приборов.
Масса и вес
При рассмотрении вопроса, что такое масса в физике, выше было сказано, что она пропорциональна количеству вещества, но не является им. Здесь же скажем, что вес тела пропорционален его массе, но ею не является.
Эти понятия часто путают между собой. Когда мы измеряем свою массу тела в килограммах с помощью каких-либо весов, то на самом деле мы определяем вес. Под последним понимают значение силы, с которой тело давит на опору или с которой растягивает нить, прикрепленную к нему.
Вес тела по абсолютной величине совпадает с силой тяжести. Расчет его выполняется по формуле: P=m*g. Где g = 9,81 м/с2 — ускорение, которое всем телам сообщает притяжение нашей планеты вблизи ее поверхности. Последняя формула позволяет определить массу: m=P/g.
Весы для измерения массы
Весы напольные, электронные, ручные, используемые для измерения массы тела в физике, откалиброваны специальным образом. Они показывают сразу килограммы. То есть, пересчитывают вес в массу по формуле, представленной в пункте выше. Вот так устроены эти приборы.
Другим способом измерения массы являются весы с двумя плечами рычага. Для определения рассматриваемой величины с помощью таких устройств используют набор эталонных гирь. Ими стараются уравновесить измеряемое тело.
Расчет массы через плотность и объем
Как найти массу в физике? Вычислить эту величину можно не только применяя различные формулы, в которые входят значения действующих на тело сил. Как было отмечено, рассматриваемая характеристика зависит линейно от количества вещества. Последнее занимает некоторую часть пространства, которая называется объемом. А друг с другом они связаны через плотность. Поясним подробнее.
Соответствующая формула, связывающая объем, массу и плотность в физике, выглядит так: m=ρ*V.
Если два тела обладают одинаковым объемом, но имеют разную плотность, то масса того тела будет больше, у которого плотность выше. Примером таких материалов являются дерево и металл или пух и камень. Соответственно, увеличение объема тела при постоянной плотности приводит к возрастанию его массы. Это доказывает аддитивность последней.
Масса и бозон Хиггса
В настоящее время в физике существует актуальная и важная задача, которая заключается в создании единой физической теории наблюдаемой Вселенной. Эта теория должна будет объединить все существующие виды взаимодействия, их насчитывается четыре, три из них уже агрегированы — это ядерное (сильное), слабое и электромагнитное. Проблема возникла при описании в рамках полученной теории явления гравитации.
Она связана прямым образом с массой тела. Причиной существования последней является так называемый бозон Хиггса. Эта элементарная частица, взаимодействуя с пространством и временем, приводит к его искривлению, что проявляется в виде явления массы. Бозон Хиггса был обнаружен в результате экспериментов на большом коллайдере в ЦЕРН. В настоящее время многие группы ученых работают над проблемой создания общей теории, в которой массе будет отведена ключевая позиция.
Формула массы в химии
Определение и формула для расчета массы
Одним из основополагающих законов в химии является закон сохранения массы (масса веществ, вступивших в химическую реакцию, всегда равна массе образовавшихся веществ), который говорит о том, что зная массу веществ, вступивших в реакцию мы легко можем рассчитать массу продуктов этой реакции и наоборот.
Для того, чтобы определить массу вещества используют следующую формулу:
m = n×M,
где n — количество вещества (моль), а М – молярная масса вещества (г/моль), откуда следует, что единицей измерения массы является [г].
Моль – это количество вещества, которое содержит столько же частиц (молекул, атомов, ионов, электронов), сколько атомов углерода содержится в 12 г изотопа 12С.
Масса одного атома 12С равна 12 а.е.м., поэтому число атомов в 12 г изотопа 12С равно:
NA = 12 г / 12 × 1,66057×10-24 г = 1/1,66057×10-24 = 6,0221×10-23.
Таким образом, моль вещества содержит 6,0221×10-23 частиц этого вещества.
Физическую величину NA называют постоянной Авогадро, она имеет размерность [NA] = моль-1. Число 6,0221×10-23 называют числом Авогадро.
Молярная масса (М)
M = NA × m (1 молекулы) = NA × Mr × 1 а.е.м. = (NA ×1 а.е.м.) × Mr = × Mr.
Это означает, что если масса некоторой молекулы равна, например, 44 а.е.м., то масса одного моля молекул равна 44 г.
Постоянная Авогадро является коэффициентом пропорциональности, обеспечивающим переход от молекулярных отношений к молярным.
Примеры решения задач
Масса — Уикипедия
Уикипедия — ашық энциклопедиясынан алынған мәлімет
Масса – материяның инерциялық және гравитациялық қасиетін анықтайтын физикалық шама. Латынның massa – үйінді, кесек деген сөзінен алынған. “Масса” ұғымын механикаға Исаак Ньютон енгізген. Ньютонның классикалық механикасындағы масса дене импульсінің (қозғалыс мөлшерінің) анықтамасына енеді. Дене импульсі (р) дененің қозғалу жылдамдығына () пропорционал болады: р=m, (1) мұндағы пропорционалдық коэффициент m – берілген дене үшін тұрақты шама, оның массасы. Массаның эквиваленттік анықтамасы Ньютон классикалық механикасының қозғалыс теңдеуінен шығады: f=ma (2) Бұл жерде масса денеге әсер ететін күш (f) пен осы күштің салдарынан болатын дененің үдеуі (а) арасындағы пропорционалдық коэффициент (1) және (2) қатынастарынан анықталатын масса инерциалдық немесе инерттік масса деп аталады. Ол дененің динамикалық қасиетін сипаттайды әрі дене инерциясының өлшеуіші болып есептеледі. Ньютонның гравитациялық теориясында масса тартылыс өрісінің көзі ретінде алынады. Әрбір дене өзінің массасына пропорционал болатын тартылыс өрісін туғызады. Осы өріс салдарынан пайда болатын денелер арасындағы тартылыс күші Ньютон ашқан бүкіл әлемдік тартылыс заңы бойынша анықталады: f = G (3)
мұндағы r – денелердің массалар центрі арасындағы қашықтық, G – әмбебап гравитациялық тұрақты, m1 және m2 – тартылатын денелердің массасы. (3) формуладан Жердің тартылыс өрісінде дененің m массасы мен оның Р салмағы арасындағы тәуелділікті алуға болады: Р = mg, (4) мұндағы g = GМ/r2 – жердің гравитациялық өрісіндегі еркін түсу үдеуі (М – Жердің массасы, r ≈ R, ал R – Жер радиусы). (3) және (4) қатыстары бойынша анықталатын масса дененің гравитациялық массасы деп аталады. Классикалық физикада дене массасы ешбір процесс кезінде өзгермейді деп саналады [Массаның (заттың) сақталу заңы]. “Масса” ұғымы жарық жылдамдығымен с=3.1010 см/с шамалас өте үлкен жылдамдықпен қозғалатын дене (не бөлшек) қозғалысын қарастыратын Альберт Эйнштейннің арнайы салыстырмалық теориясында терең мағынаға ие болды. Релятивистік механика деп аталатын жаңа механикада импульс пен бөлшек жылдамдығы арасындағы байланыс: р = (5)
қатысы арқылы беріледі [шағын жылдамдықта (<<с) бұл қатыс (1) қатысына айналады]. m0 шамасы тыныштық массасы деп аталады. Қозғалған бөлшек массасы (m) жылдамдыққа тәуелді шама ретінде анықталады: m = , (6)
яғни бөлшек (дене) массасы қозғалыс жылдамдығының өсуіне байланысты артады. Релятивистік механикада (1) және (2) теңдеулердегі массаның анықтамасы бір-біріне эквивалентті емес, өйткені үдеу өзін қоздырған күшке параллель болмайды және масса бөлшек жылдамдығының бағытына тәуелді болып қалады. Салыстырмалық теориясы бойынша бөлшектің массасы (m) оның энергиясымен (Е) мына қатыс арқылы байланысады:
- E=mc2{\displaystyle E=mc^{2}} (7)
Сонымен масса энергиямен әрқашанда байланыста болады. Сондықтан релятивистік механикада классикалық физикадағы екі заң – массаның сақталу заңы мен энергияныңсақталу заңы – бөлек-бөлек емес, толық энергияның сақталу заңы деп аталатын бір заңға біріктірілген. Масса бірлігіне бірліктердің СГС жүйесінде – грамм (г), ал бірліктердің халықаралық жүйесінде (СИ) – килограмм (кг) алынады. Атомдар мен молекулалар массасы, әдетте массаның атомдық бірлігімен өлшенеді. Элементар бөлшектердің массасын не электрон массасы (mе) бірлігімен не бөлшектің тыныштық энергиясын көрсете отырып, энергетикалық бірлікпен өлшейді. Электрон массасы (mе) 0,511 МэВ, протон массасы – 1836,1 me немесе 938,2 МэВ, т.б. құрайды. Массаның табиғатын ашу – қазіргі физиканың шешілмеген маңызды міндеттерінің бірі. Элементар бөлшектердің массасы олардың өздері байланысқан өрістер (электрмагниттік, ядролық, т.б.) арқылы анықталады деп қабылданған. Алайда массаның сандық теориясы әлі жасалған жоқ.
Өлшем бірліктері[өңдеу]
Масса – экономикада: тауарлардың мөлшері (тауар‚ ақша массасы‚ конкурстық масса). Топтамалардың құнын‚ шамасын‚ салық салу базасын‚ т.б. анықтау үшін пайдаланылатын тауарлардың аса маңызды сипаттамаларының бірі. Мынадай салмақ (масса) өлшемдері қолданылады: 1 тонна = 10 центнер = 1000 килограмм = 1000000 грамм 1 ағылшын тоннасы = 20 центнер = 2240 сауда фунты 1 сауда фунты = 16 сауда унциясы = 256 сауда драхмасы 1 ағылшын тоннасы = 1016 килограмм 1 ағылшын сауда центнері = 50‚802 килограмм 1 сауда фунты = 0‚453 килограмм 1 сауда унциясы=28‚349 грамм 1 сауда драхмасы = 1‚77 грамм 1 ағылшын граны = 64‚799 грамм 1 американ шағын тоннасы = 907‚17 килограмм 1 дәріханалық фунт=12 дәріханалық унция = 373‚24 грамм 1 дәріханалық унция=8 дәріханалық драхма=31‚103 грамм 1 дәріханалық драхма = 3 скрупула = 3‚888 грамм 1 пұт = 16‚38 килограмм 1 байырғы орыс фунты = 409‚5 грамм 1 лот = 12‚8 грамм 1 мысқал = 4‚266 грамм 1 үлес = 44‚43 миллиграмм
Масса ақауы[өңдеу]
Масса ақауы, масса дефектісі – атом ядросын құраушы нуклондар (нейтрондар мен протондар) массаларының қосындысы мен ядро массасының (М) арасындағы айырым ():=ZMp+(A––Z)Mn–M, мұндағы Z – ядродағы протондардың саны, А – ядроның массалық саны, Мр мен Мn – протон мен нейтронның массалары. Масса ақауы массаның атомдық бірлігімен өрнектеледі және ол ядродағы нуклондардың байланыс энергиясына тең (кері таңбамен алынған). Масса ақауы неғұрлым үлкен болса, солғұрлым байланыс энергиясы жоғары және ядро орнықты болады.
Масса тұрақтылық заңы, масса сақталу заңы – реакцияға қатысқан заттардың (реагенттердің) массаларының қосындысы реакция нәтижесінде түзілген заттардың (өнімдердің) массаларының қосындысына тең. 1774 – 89 ж. француз химигі Антуан Лавуазье, өзі жасаған күрделі тәжірибелерге сүйене отырып, тұжырымдаған. Мысалы, 32 г оттек пен 4 г сутек қосылғанда 36 г су түзіледі; 2Н2+О2 =2Н2О. Мұндағы реакцияға түскен реагенттердің жалпы массасы (36 г) реакция нәтижесінде түзілген өнімнің массасына (36 г) тең.[1]
Релятивистік масса[өңдеу]
Релятивистік масса –– бөлшектің толық энергиясының вакуумдағы жарық жылдамдығының шаршысына қатынасымен анықталатын масса.[2][3]
Пайдаланылған cілтемелер[өңдеу]
- ↑ Балалар Энциклопедиясы, 6 том.
- ↑ Орысша-қазақша түсіндірме сөздік: Механика / Жалпы редакциясын басқарған э.ғ.д., профессор Е. Арын — Павлодар : «ЭКО»ҒӨФ. 2007.-29 1 б. ISBN 9965-08-234-0
- ↑ Полиграфия, өлшеу техникасы, ағаш өңдеу жабдыктары және металл өңдеу техникасы мен технологиясы: Қазақша-орысша терминдердің түсіндірме сөздігі.
Формула веса
В обиходе и повседневной жизни понятия «масса» и «вес» абсолютно идентичны, хотя семантическое их значение принципиально разное. Спрашивая «Какой у тебя вес?» мы подразумеваем «Сколько в тебе килограммов?». Однако на вопрос, с помощью которого мы пытаемся выяснить этот факт, ответ дается не в килограммах, а в ньютонах. Придется вернуться к школьному курсе физики.
Вес тела — величина, характеризующая силу, с которой тело оказывает давление на опору или подвес.
Для сравнения, масса тела ранее грубо определялась как «количество вещества», современное определение звучит таким образом:
Масса — физическая величина, отражающая способность тела к инерции и являющаяся мерой его гравитационных свойств.
Понятие массы вообще несколько шире представленного здесь, однако наша задача состоит несколько в другом. Вполне достаточно уяснить факт действительного различия между массой и весом.
Кроме того, единица измерения массы — килограммы, а веса (как вида силы) — ньютоны.
И, пожалуй, самое главное отличие веса от массы содержит в себе сама формула веса, которая выглядит следующим образом:
P=mg
где P — собственно вес тела (в Ньютонах), m — его масса в килограммах, а g — ускорение свободного падения, которое принято выражать в виде 9,8 Н/кг .
Иными словами, формула веса может быть понята на таком примере:
Гиря массой 1 кг подвешена к неподвижному динамометру, с тем, чтобы определить ее вес. Поскольку тело, да и сам динамометр, находятся в покое, то смело можно умножать его массу на ускорение свободного падения. Имеем: 1 (кг) х 9,8 (Н/кг)= 9,8 Н. Именно с такой силой действует гиря на подвес динамометра. Отсюда ясно, что вес тела равняется силе тяжести. Однако это не всегда так.
Самое время сделать важное замечание. Формула веса равняется силе формуле тяжести лишь в случаях, когда:
- тело находится в состояние покоя;
- на тело не действует сила Архимеда (выталкивающая сила). Любопытный факт, касающийся выталкивающей силы: известно, что тело, погруженное в воду, вытесняет объем воды, равный своем весу. Но оно не просто выталкивает воду, тело становится «легче» на объем вытесненной воды. Вот почему поднять в воде девушку массой 60 кг можно шутя и смеясь, а на поверхности это сделать куда сложнее.
При неравномерном движении тела, т.е. когда тело совместно с подвесом движутся с ускорением a,меняет свой облик и формула веса. Физика явления меняется незначительно, но в формуле такие изменения находят следующее отражение :
P=m (g-a).
Как можно заменить по формуле, вес может быть отрицательным, но для этого ускорение, с которым движется тело, должно быть больше ускорения свободного падения. И тут опять важно отличать вес от массы: отрицательный вес не влияет на массу (свойства тела остаются те же), однако он фактически становится направлен в противоположную сторону.
Хорош пример с ускоренным лифтом: при его резком ускорении на непродолжительное время создается впечатление»притягивания к потолку». С таким ощущением, конечно, столкнуться достаточно просто. Гораздо сложнее прочувствовать состояние невесомости, которое в полной мере ощущают космонавты на орбите.
Невесомость — по сути, отсутствие веса. Для того чтобы такое было возможным, ускорение, с которым движется тело, должно быть равно пресловутому усорению g (9,8 Н/кг). Добиться такого эффекта проще всего на околоземной орбите. Гравитация, т.е. притяжение, по-прежнему действует на тело (спутник), однако она пренебрежимо мала. А ускорение дрейфующего по орбите спутника также стремится к нулю. Тут-то и возникает эффект отсутствия веса, поскольку тело вообще не соприкасается ни с опорой, ни с подвесом, а попросту парит в воздухе.
Частично с таким эффектом можно столкнуться при взлете самолета. На секунду возникает ощущение подвешенности в воздухе: в этот момент ускорение, с которым движется самолет, равно ускорению свободного падения.
Вновь возвращаясь к отличиям веса и массы, важно помнить, что формула веса тела отличается от формулы массы, которая выглядит как:
m=ρ/V,
то есть плотность вещества, деленная на его объем.
Формула молекулярной массы элемента в химии
Определение и формула молекулярной массы
Массы атомов и молекул очень малы, поэтому в качестве единицы измерения удобно выбрать массу одного из атомов и выражать массы остальных атомов относительно нее. Именно так и поступал основоположник атомной теории Дальтон, который составил таблицу атомных масс, приняв массу атома водорода за единицу.
До 1961 года в физике за атомную единицу массы (а.е.м. сокращенно) принимали 1/16 массы атома кислорода 16О, а в химии – 1/16 средней атомной массы природного кислорода, который является смесью трех изотопов. Химическая единица массы была на 0,03% больше, чем физическая.
В настоящее время за в физике и химии принята единая система измерения. В качестве стандартной единицы атомной массы выбрана 1/12 часть массы атома углерода 12С.
1 а.е.м. = 1/12 m(12С) = 1,66057×10-27 кг = 1,66057×10-24 г.
Относительная атомная и молекулярная масса элемента
При расчете относительной атомной массы учитывается распространенность изотопов элементов в земной коре. Например, хлор имеет два изотопа 35Сl (75,5%) и 37Сl (24,5%).Относительная атомная масса хлора равна:
Ar(Cl) = (0,755×m(35Сl) + 0,245×m(37Сl)) / (1/12×m(12С) = 35,5.
Из определения относительной атомной массы следует, что средняя абсолютная масса атома равна относительной атомной массе, умноженной на а.е.м.:
m(Cl) = 35,5 ×1,66057×10-24 = 5,89×10-23 г.
Относительная молекулярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы, например:
Mr(N2O) = 2×Ar(N) + Ar(O) = 2×14,0067 + 15,9994 = 44,0128.
Абсолютная масса молекулы равна относительной молекулярной массе, умноженной на а.е.м.
Число атомов и молекул в обычных образцах веществ очень велико, поэтому при характеристике количества вещества используют специальную единицу измерения – моль.
Моль – это количество вещества, которое содержит столько же частиц (молекул, атомов, ионов, электронов), сколько атомов углерода содержится в 12 г изотопа 12С.
Масса одного атома 12С равна 12 а.е.м., поэтому число атомов в 12 г изотопа 12С равно:
NA = 12 г / 12 × 1,66057×10-24 г = 1/1,66057×10-24 = 6,0221×10-23.
Таким образом, моль вещества содержит 6,0221×10-23 частиц этого вещества.
Физическую величину NA называют постоянной Авогадро, она имеет размерность [NA] = моль-1. Число 6,0221×10-23 называют числом Авогадро.
Молярная масса вещества
Легко показать, что численные значения молярной массы М и относительной молекулярной массы Mr равны, однако первая величина имеет размерность [M] = г/моль, а вторая безразмерна:
M = NA × m (1 молекулы) = NA × Mr × 1 а.е.м. = (NA ×1 а.е.м.) × Mr = × Mr.
Это означает, что если масса некоторой молекулы равна, например, 44 а.е.м., то масса одного моля молекул равна 44 г.
Постоянная Авогадро является коэффициентом пропорциональности, обеспечивающим переход от молекулярных отношений к молярным.
Примеры решения задач
Формула атомной массы элемента в химии
Определение и формула атомной массы
Массы атомов и молекул очень малы, поэтому в качестве единицы измерения удобно выбрать массу одного из атомов и выражать массы остальных атомов относительно нее. Именно так и поступал основоположник атомной теории Дальтон, который составил таблицу атомных масс, приняв массу атома водорода за единицу.
До 1961 года в физике за атомную единицу массы (а.е.м. сокращенно) принимали 1/16 массы атома кислорода 16О, а в химии – 1/16 средней атомной массы природного кислорода, который является смесью трех изотопов. Химическая единица массы была на 0,03% больше, чем физическая.
В настоящее время за в физике и химии принята единая система измерения. В качестве стандартной единицы атомной массы выбрана 1/12 часть массы атома углерода 12С.
1 а.е.м. = 1/12 m(12С) = 1,66057×10-27 кг = 1,66057×10-24 г.
При расчете относительной атомной массы учитывается распространенность изотопов элементов в земной коре. Например, хлор имеет два изотопа 35Сl (75,5%) и 37Сl (24,5%).Относительная атомная масса хлора равна:
Ar(Cl) = (0,755×m(35Сl) + 0,245×m(37Сl)) / (1/12×m(12С) = 35,5.
Из определения относительной атомной массы следует, что средняя абсолютная масса атома равна относительной атомной массе, умноженной на а.е.м.:
m(Cl) = 35,5 ×1,66057×10-24 = 5,89×10-23 г.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
Формула массы — определение и решенные примеры
Концепция массы измеряет количество материи, существующей в объекте. Это количественное свойство объекта против ускорения. Масса и вес объекта не совпадают. Молярная масса (M) — это физическое свойство, которое определяется как масса одного моля химического вещества или как отношение массы химического соединения к его количеству химического вещества. Единица измерения молярной массы — кг / моль.
Формула массы представлена как
Масса = ρ × v
Где,
ρ = плотность и
v = объем
Формула массы задается как
м = вес / г
Где,
w = вес
м = масса
г = плотность
Формула массы также дается как
m = F / a
Если ускорение — это сила тяжести, тогда
M = Ф / г
Где,
F = сила
G = гравитация
Согласно соотношению массы и энергии Эйнштейна
m = (E / c 2 )
Где,
м = масса
E = энергия
c = скорость света (3 × 10 8 м / с)
Формула массы кинетической энергии дается как
К.E = ½ мв 2
Где,
m = масса,
v = скорость.
Пример 1
Рассчитайте массу, если вес тела 80 Н.
Решение:
Дано,
масса корпуса = 80 Н
Масса тела выражается числом
.м = вес / г
м = 80 / 9,8
м = 8,163 кг
Пример 2
Определите массу тела, если K.E составляет 70 Дж, а скорость — 8 м / с.
Решение:
Дано:
к.э. = 70 Дж
v = 8 м / с
масса выражается через
м = 2 к.э. / об 2
м = (2 × 70) / 8 2
м = 14o / 64
м = 2,18 кг
.Формула Масса
3.5 Формула массы
Цель обучения
- Определите формульную массу ионного соединения.
Один навык, который понадобится в будущих главах, — это способность определять массу формулы ионного соединения. Эта величина называется формулой массы — сумма масс элементов в формуле ионного соединения. Формула массы получается путем сложения масс каждого отдельного атома в формуле соединения.Поскольку правильная формула является электрически нейтральной (без получения или потери чистых электронов), ионы можно рассматривать как атомы для вычисления формулы массы.
Начнем с расчета формулы массы хлорида натрия (NaCl). Эта формула массы представляет собой сумму атомных масс одного атома натрия и одного атома хлора, которую мы находим из периодической таблицы; здесь мы используем массы до двух десятичных знаков:
| Na: | 22.99 u |
| Класс: | + 35.45 из |
| Всего: | 58,44 u |
С точностью до двух знаков после запятой формула массы NaCl равна 58,44 ед.
Когда ионное соединение имеет более одного аниона или катиона, вы должны помнить, что использовать правильное кратное атомной массы для рассматриваемого элемента. Для формулы массы фторида кальция (CaF 2 ) мы должны умножить массу атома фтора на 2, чтобы учесть два атома фтора в химической формуле:
| Ca: | 1 × 40.08 | 40.08 u |
| Ф: | 2 × 19,00 = | + 38.00 из |
| Всего: | 78.08 u |
Формульная масса CaF 2 равна 78,08 ед.
Для ионных соединений с многоатомными ионами сумма должна включать количество и массу каждого атома в формуле для многоатомного иона.Например, нитрат калия (KNO 3 ) имеет один атом калия, один атом азота и три атома кислорода:
| К: | 1 × 39,10 | 39,10 и |
| №: | 1 × 14,00 | + 14.00 из |
| О: | 3 × 16,00 = | + 48.00 u |
| Всего: | 101.10 u |
Формульная масса KNO 3 составляет 101,10 ед.
Примечание
Нитрат калия является ключевым ингредиентом пороха и используется в клинических условиях как мочегонное средство.
Если формула содержит более одной многоатомной единицы в химической формуле, как в Ca (NO 3 ) 2 , не забудьте умножить атомную массу каждого атома в скобках на нижний индекс вне скобок.Это необходимо, потому что нижний индекс относится к полному многоатомному иону . Таким образом, для Ca (NO 3 ) 2 нижний индекс 2 означает два полных нитрат-иона, поэтому мы должны суммировать массы двух (1 × 2) атомов азота и шести (3 × 2) атомов кислорода, а также масса одного атома кальция:
| Ca: | 1 × 40,08 | 40.08 u |
| №: | 2 × 14.00 = | + 28.00 из |
| О: | 6 × 16,00 = | + 96.00 из |
| Всего: | 164.08 u |
Ключом к вычислению формулы массы ионного соединения является правильный подсчет каждого атома в формуле и соответствующее умножение атомных масс его атомов.
Пример 9
Используйте атомные массы (округленные до двух знаков после запятой) с внутренней стороны обложки этой книги, чтобы определить формулу массы для каждого ионного соединения.
- FeCl 3
- (NH 4 ) 3 PO 4
Решение
Fe: 55.85 u Класс: 3 × 35,45 = + 106.35 u Всего: 162.20 u Формульная масса FeCl 3 составляет 162,20 ед.
Когда мы распределяем индекс 3 через круглые скобки, содержащий формулу для иона аммония, мы видим, что у нас есть 3 атома азота и 12 атомов водорода.Таким образом, выставляем сумму так:
№: 3 × 14,00 = 42,00 u H: 12 × 1,00 = + 12.00 из П: + 30.97 u О: 4 × 16,00 = + 64.00 из Всего: 148.97 u Формула массы для (NH 4 ) 3 PO 4 составляет 148,97 ед.
Упражнение по развитию навыков
Используйте атомные массы (округленные до двух десятичных знаков) с внутренней стороны обложки этой книги, чтобы определить формулу массы для каждого ионного соединения.
Для вашего здоровья: увлажняет
Некоторые ионные соединения содержат воду (H 2 O), входящую в их формульную единицу.Эти соединения, называемые гидратами , имеют характерное количество водных единиц, связанных с каждой формульной единицей соединения. Гидраты — это твердые вещества, а не жидкости или растворы, несмотря на содержащуюся в них воду.
Чтобы написать химическую формулу гидрата, запишите количество единиц воды на формульную единицу соединения после его химической формулы. Две химические формулы разделены точкой с вертикальным центром. Гидрат сульфата меди (II) имеет пять единиц воды, связанных с каждой формульной единицей, поэтому он записывается как CuSO 4 · 5H 2 O.Название этого соединения — пентагидрат сульфата меди (II) с префиксом пента- , указывающим на присутствие пяти единиц воды на формульную единицу сульфата меди (II).
Гидраты находят различное применение в индустрии здравоохранения. Полугидрат сульфата кальция (CaSO 4 · ½H 2 O), известный как Парижский гипс, используется для изготовления слепков для сломанных костей. Английская соль (MgSO 4 · 7H 2 O) используется как соль для купания и слабительное средство. Гексагидрат хлорида алюминия является активным ингредиентом антиперспирантов.В прилагаемой таблице перечислены некоторые полезные гидраты.
Таблица 3.4 Названия и формулы некоторых широко используемых гидратов
| Формула | Имя | использует |
|---|---|---|
| AlCl 3 · 6H 2 O | гексагидрат хлорида алюминия | антиперспирант |
| CaSO 4 · ½H 2 O | полугидрат сульфата кальция (гипс) | слепки (для переломов и отливок) |
| CaSO 4 · 2H 2 O | дигидрат сульфата кальция (гипс) | гипсокартон |
| CoCl 2 · 6H 2 O | гексагидрат хлорида кобальта (II) | осушитель, индикатор влажности |
| CuSO 4 · 5H 2 O | Пентагидрат сульфата меди (II) | фунгицид, альгицид, гербицид |
| MgSO 4 · 7H 2 O | Гептагидрат сульфата магния (английская соль) | слабительное, соль для купания |
| Na 2 CO 3 · 10H 2 O | декагидрат карбоната натрия (сода стиральная) | добавка для стирки / очиститель |
Упражнения по обзору концепции
Какая связь между атомной массой и формульной массой?
Как индексы используются для определения формулы массы, если в химической формуле присутствует более одного многоатомного иона?
ответов
Формульная масса — это сумма атомных масс атомов в формуле.
Нижний индекс в круглых скобках определяет общее количество атомов в формуле.
Ключевые вынос
- Формульные массы ионных соединений можно определить по массам атомов в их формулах.
Формула центра масс
Центр масс — это точка равновесия объекта или группы объектов. Центр масс может быть найден для любого одно-, двух- или трехмерного объекта, поэтому единицы измерения — метры ( м ) в каждом измерении. Приведенная здесь формула предназначена для центра масс в одном измерении.
X = центр масс ( м )
м i = масса части объекта ( кг )
x i = положение части объекта ( м )
Формула центра масс Вопросы:
1) Минутная стрелка часов состоит из стрелки и круга, соединенных тонким куском металла с незначительной массой.Стрела имеет массу 15,0 г , а круг имеет массу 60,0 г . Если круг находится в позиции 0,000 м , а стрелка находится в позиции 0,100 м , где находится центр масс?
Ответ: Центр масс минутной стрелки можно найти по формуле:
X = 0,020 м
Центр масс 0,020 м от окружности.
2) К подвесному светильнику прикреплены следующие светильники: i) огонь 0,10 кг в позиции 0,00 м , ii) огонь 0,20 кг в позиции 0,20 м , iii) 0,80 кг на позиции 0,80 м , и iv) огонь 0,10 кг на позиции 1,0 м . Где центр масс?
Ответ: Центр масс минутной стрелки можно найти по формуле:
Х = 0.65 кв.м
Центр масс находится в позиции 0,65 м .
.Формула молярной массы — шаги для определения молярной массы с решенными примерами.
Моль — это единица счета, определяющая количество атомов, молекул, ионов или формульных единиц в конкретном химическом соединении. Он похож на другие счетные единицы, такие как пара (2) и дюжина (12). Один моль соединения содержит число Авогадро (6,02214076 × 10 23 моль) молекул или формульных единиц. Молярная масса соединения определяет массу 1 моля этого конкретного вещества и количество граммов на моль соединения.Другими словами, молярная масса — это общая масса всех атомов в граммах, составляющих моль конкретной молекулы. Следовательно, единицы измерения молярной массы — граммы / моль. Как найти молярную массу соединения?Шаг 1. Воспользуйтесь химической формулой, чтобы определить количество атомов каждого элемента в соединении.
Шаг 2. Умножьте атомный вес каждого элемента на количество атомов, присутствующих в соединении.
Шаг 3. Сложите все и задайте единицы измерения — граммы / моль.
Пример. 1 Какова молярная масса карбоната натрия, Na 2 CO 3 ?
Раствор Так как карбонат натрия содержит два атома натрия, один атом углерода и три атома кислорода. Молекулярная масса будет
.Na: 2 x 23,0 = 46
С: 1 х 12,0 = 12
O: 3 x 16 = 48
Когда мы складываем общие значения, то есть 46 + 12 + 48 = 106
Следовательно, молярная масса Na2CO3 составляет 106 г / моль.
Пример 2 . Определить молярную массу нитрата кальция, Са (NO 3 ) 2 ?
Раствор: Так как нитрат кальция содержит один атом кальция, два атома азота и шесть атомов кислорода.
Ca: 1 x 40,1 = 40,1
N: 2 x 14,0 = 28
O: 6 x 16,0 = 96
Если сложить все, 40,1 + 14 + 16 = 164,1
Следовательно, молярная масса Ca (NO3) 2 составляет 164,1 г / моль.
Обратите внимание, что нижний индекс два после скобок указывает на наличие 2 нитрат-иона (NO3-).Умножьте количество атомов на нижние индексы вне скобок. Индексы за пределами () влияют только на атомы внутри (), но не на ион Са.
Для решения дополнительных примеров и практических вопросов о молярной массе посетите сайт Byju’s.com
.