16. Опишите объемные дефекты и условия их образования.
Дефектами
кристалла называют всякое
нарушение трансляционной симметрии
кристалла— идеальной
периодичности кристаллической
решётки. Различают несколько видов
дефектов по размерности. А
именно,бывают нульмерные (точечные),
одномерные (линейные), двумерные
(плоские) и трёхмерные (объемные)
дефекты. Объемные дефекты представляют
собой искажения решетки, вызванные
наличием пор, трещин, раковин и других
макронарушений непрерывности
кристаллической решетки. Происхождение —
нарушение режимов роста кристалла,
распад пересыщенного твердого раствора,
загрязнение образцов. В некоторых
случаях (например, при дисперсионном
твердении) объемные дефекты специально
вводят в материал, для модификации его
физических свойств. Объемные дефекты
имеют относительно большие размеры,
несоизмеримые с атомным диаметром, во
всех трех измерениях.

17. Укажите основные этапы технологии получения сварных заготовок.
Заготовки
машиностроительного производства,
имеющие форму и размеры близкие к форме
деталей машин, получают методами
обработки давлением, порошковой
металлургии, литья и сварки. Для получения
заготовок из стали и цветных металлов
с деформированной макроструктурой
применяют методы обработки давлением:
ковку, объемную и листовую штамповку.
Ковку применяют для изготовления
заготовок в единичном производстве
путем пластической деформации профилей
или слитков. Заготовки, полученные
объемной штамповкой, отличаются более
высокой точностью размеров и качеством
поверхностного слоя по сравнению с
коваными поковками. Листовой штамповкой
изготавливают самые разнообразные
плоские и пространственные изделия
минимальной массой (от долей граммов
до десятков килограммов) с высокой
точностью размеров и качеством
поверхности. Методами порошковой
металлургии получают заготовки, которые
по размерам и форме близки к размерам
и форме деталей, поэтому при изготовлении
изделий требуется небольшой объем
механической обработки.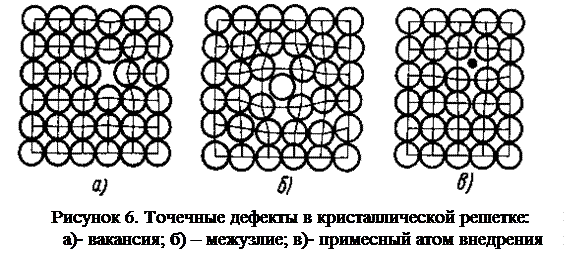
18.Раскройте
основные положения теории сплавов. Сплав –
это вещество, получаемое в результате
затвердевания жидкого расплава,
состоящего из двух и более элементов,
или спеканием порошков методом порошковой
металлургии. Металлический сплав – это
вещество, обладающее металлическими
свойствами, полученное путем сплавления
металла с металлом или металла с
неметаллом.Согласно теории сплавов,
сплавы делятся на:1Механические смеси
2 Твердые растворы (внедрения, замещения,
вычитания)3 Химические соединения.
При образовании сплавов в виде м е
х а н и ч е с к о й с м е с и атомы
каждого компонента формируют свои
кристаллические решетки и образуют
смесь кристаллов двух или нескольких
чистых компонентов.
 В
случае образования химического соединения
только металлическими элементами
образуется металлическая связь, а при
образовании соединения металла с
неметаллом – ионная.
В
случае образования химического соединения
только металлическими элементами
образуется металлическая связь, а при
образовании соединения металла с
неметаллом – ионная.ЗАДАЧИ (Дефекты кристаллического строения металлов)
содержание .. 20 21 22 23
Задача 1. Расположите элементы Al, Nb, Ni и Sn в ряд в порядке предположительного возрастания энергии образования вакансий. Дайте необходимые пояснения.
Решение: Энергии образования вакансий Ео можно приближенно оценить по энергии активации самодиффузии которая приближенно пропорциональна Тпл. Поэтому ряд в порядке предположительного возрастания энергии образования вакансий:
Ответ: Sn→Al→Ni→Nb.
Задача 2. При температуре вблизи точки плавления равновесная концентрация вакансий в магнии равна 7,2·10-4. Приближенно оцените равновесную концентрацию вакансий в магнии при комнатной температуре.
Решение: Для магния При температуре вблизи точки плавления С1=7,2·10-4. Равновесную концентрацию вакансий при комнатной температуре
Ответ: 1,22∙10-10.
Задача 3. Приближенно оцените энергию образования вакансии в ГЦК металле, если экспериментально определенная равновесная концентрация вакансий при 927 °С равна 1∙10-5.
Решение: Т.к. и то
Ответ: 1,2 эВ.
Задача 4. Оцените,
на сколько порядков изменится равновесная концентрация вакансий в золоте
при повышении температуры с 600 до 1000 °С, если при 600 °С эта
концентрация равна 9,1∙10
Решение: Т.к. и то
Отсюда а C2=3,5∙10-4.
Ответ: 3,5∙10-4.
Задача 5. В меди, закаленной с 600 °С, содержится 1,1∙10-5 % (ат.) вакансий. Какую температуру закалки следует выбрать, чтобы концентрация вакансий возросла на два порядка?
Решение: Т.к. а
и то
Ответ: ~950°С.
Задача 6. Металл
содержит равномерно распределенной примеси замещения. Определите среднее
расстояние между примесными атомами в единицах периода ГЦК. и ОЦК.
решетки.
Определите среднее
расстояние между примесными атомами в единицах периода ГЦК. и ОЦК.
решетки.
Решение: С=0,1 ат.%=10-3. Для
примитивной решетки (1 атом на 1 элементарную ячейку) примесь замещения
повторяется через 10 периодов решетки, т.е через lприм =
10а. Т.к. к ГЦК 4 атома на 1 элементарную ячейку, а а ОЦК – 2, то l
Ответ: 6,3 и 7,9 a.
Задача 7. Экспериментальные определения относительной концентрации вакансий в меди дали значения 8∙10-5 при 980° С и 16∙10-5 при 1060°С. По этим данным рассчитайте энергию образования и энтропию образования вакансии в меди.
Решение: Т.к.
и система двух уравнений с двумя неизвестными — энергия образования Eo и энтропию образования S вакансии:
Прологарифмируем оба уравнения и вычтем
из первого второе. Отсюда получим
Отсюда получим
Энтропия
Ответ: 0,81 эв и -1,3k
Задача 8. У кристалла закиси железа FехО постоянная решетки a = 4,30 Å, а плотность равна 5,72 г/см3. Каков состав кристалла (т. е. значение в формуле FexO)? Определите ваши предположения о структуре этого кристалла. Решение: FехО имеет решетку типа NaCl, a = 4,30 Å=0,43 нм. На 1 элементарную ячейку приходится по 4 иона Fe и O.
При составе FeO плотность
Часть позиций ионов Fe+2 – вакансии, и формула закиси железа FexO. Найдем значение x их выражения (55,85+16)/(55,85+16)=1-0,047. Отсюда x=0,94.
Ответ: x=0,94.
Задача 9. Кристалл вюстита (приблизительный состав FexO) имеет структуры типа NaCl и содержит 76,08 вес.%. Было найдено, что его плотность равна 5,613 г/см3, а период решетки a=4,2816Å. Содержит ли этот кристалл вакансии по железу или межузельные ионы кислорода? Какова плотность вакансий (или межузельных атомов)?
Решение: При составе FeO вес.% Fe равен
55,85/(55,85+16)=0,7773 или 77.73 вес.%. Т.к. ρ<ρ0 (см.пред.
задачу), кристалл содержит вакансии по Fe (т.к. rFe+2
< rO-2),
а не межузельные ионы кислорода. Нехватка ионов Fe составляет n =
(77,73-76,08)/77,73 = 0,0212 или 2,12%.Т.е состав FexO – Fe0,98O.
В 1 элементарной ячейке по 4 иона Fe,
т. е. нехватка ионов Fe (или
доля вакансий по Fe)
на 1 элементарную ячейку равно 4n=0,0848.
Плотность вакансий по Fe составляет 4n/a3 = 0,0848/4,28168 ∙10-24 см3=
6,2∙1021 см-3.
е. нехватка ионов Fe (или
доля вакансий по Fe)
на 1 элементарную ячейку равно 4n=0,0848.
Плотность вакансий по Fe составляет 4n/a3 = 0,0848/4,28168 ∙10-24 см3=
6,2∙1021 см-3.
Ответ: плотность вакансий по железу 6,2∙1021 см-3.
Задача 10. Если концентрация вакансий в алюминии при его температуре плавления составляет 9,4∙10-4 и если после закалки алюминия от температуры плавления вакансии конденсируются в диски на плотно упакованных плоскостях и образуют петли Франка, определите плотность создающихся дислокаций при радиусе петель а) 50 Å и б) 500 Å.
Решение: Если концентрация
вакансий n=9,4∙10-4,
а параметр решетки алюминия a=4,05∙10—8 см,
то петли Франка образуются в плотноупакованной плоскости (111) с
межплоскостным расстоянием d111= a/. При радиусе петли R1=50 Å=50∙10—8 см объем
вакансионного диска V1=πR12d111 ,
а длина петли L1=2πR1.
При этом объем всего металла V0=V1/n.
Отсюда плотность дислокаций ρ1=L1/V0=2n/R1d111 =
2∙9,4∙10-4∙/50∙10-8 см∙4,05∙10—8 см =
1,3∙1011 см-2.
При радиусе петли R2=500 Å=500∙10—8 см,
аналогично ρ2=1,3∙1010 см-2.
При радиусе петли R1=50 Å=50∙10—8 см объем
вакансионного диска V1=πR12d111 ,
а длина петли L1=2πR1.
При этом объем всего металла V0=V1/n.
Отсюда плотность дислокаций ρ1=L1/V0=2n/R1d111 =
2∙9,4∙10-4∙/50∙10-8 см∙4,05∙10—8 см =
1,3∙1011 см-2.
При радиусе петли R2=500 Å=500∙10—8 см,
аналогично ρ2=1,3∙1010 см-2.
Ответ: 1,3∙1011 см-2 и 1,3∙1010 см-2.
Задача 11. Стержень
из золота нагревается до температуры плавления, при которой концентрация
вакансий составляет 7,2·10-4 от
числа узлов решетки. Затем этот стержень закаливают так, что все
вакансии, генерированные при температуре плавления, оказываются
захваченными в металле. Если отжигать этот стержень при постоянной, чуть
более высокой температуре, то наблюдается сокращение его размеров по
мере уменьшения концентрации вакансий до ее равновесного, очень низкого
значения. Если величина всего сжатия равна 1,1∙10 -4,
то какова будет величина изменения параметра решетки в процессе этого
отжига?
Затем этот стержень закаливают так, что все
вакансии, генерированные при температуре плавления, оказываются
захваченными в металле. Если отжигать этот стержень при постоянной, чуть
более высокой температуре, то наблюдается сокращение его размеров по
мере уменьшения концентрации вакансий до ее равновесного, очень низкого
значения. Если величина всего сжатия равна 1,1∙10 -4,
то какова будет величина изменения параметра решетки в процессе этого
отжига?
Решение: Концентрация
вакансий nв/N=7,2·10—4,
сжатие ΔV/V=1,1∙10 -4.
Изменение длины стержня ΔL/L=1/3 ∙ ΔV/V.
При нагревании изменение длины ΔL/L связано
как с появлением вакансий в объеме, так из-за изменения параметра
решетки Δa/a:
ΔL/L=nв/3N +
Δa/a. Отсюда
относительное изменение параметра
решетки Δa/a = ΔL/L-1/3 ∙ nв/N =
(1,1-7,2/3)·10-4=-1,3·10-4.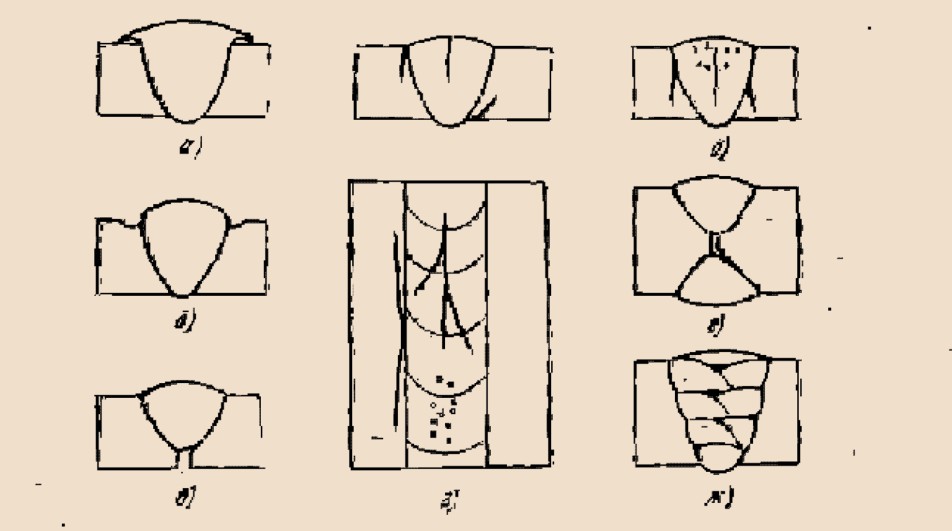 Т.е.
параметр решетки уменьшается при нагреве и растет при охлаждении.
Т.е.
параметр решетки уменьшается при нагреве и растет при охлаждении.
Ответ: относительное увеличение = 1,3∙10-4.
Задача 12. Оценить равновесную концентрацию вакансий в серебре в точке плавления 961 °С, зная модуль сдвига G = 2,8∙103 кгс/мм2 и период решетки а = 4,078 Å.
Решение: кгс/мм2 = 28∙103 Н/мм2, а=4,078 Å=4,078·10—7 мм. Энергия образования вакансии Ев=αвGb3, где αв≈1/4. Вектор Бюргерса полной дислокации а/2 <110> в ГЦК решетке равен b= а/.Отсюда Ев = 1,678·10-19 Дж = 1,05 эВ. Равновесную концентрацию вакансий в серебре в точке плавления
.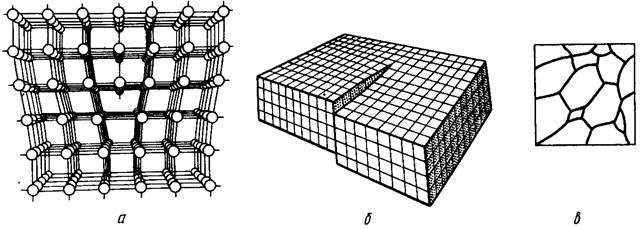
Ответ: 0,52·10-4.
Задача 13. В поликристалле зерно размером d = 10 мкм содержит избыток вакансий 1∙10-4. Оценить перемещение Δх границ, если все вакансии стекут на границы. Решетка ГЦК с периодом a =4·10—8 см. Считать зерно шаром.
Решение: Объем шара V=4/3 πR3=1/6 πd3. Изменение объема шара связано с избытком вакансий и Изменение объема шара Отсюда Отсюда перемещение границ Δх= Δd/2= nв/N d/6π = 0,53·10-4 мкм = 0,53·10—8см. Т.к. a =4·10—8 см, то Δх=0,13a
Ответ: 0,13a
Задача 14. Резкая
закалка меди от точки плавления может уменьшить ее плотность на 0,02 %
за счет увеличения концентрации вакансий. При какой относительной и
абсолютной погрешности измерений длины и массы (или силы) это изменение
можно надежно обнаружить: а) прямым измерением плотности; б)
гидростатическим взвешиванием. Перечислить побочные источники ошибки при
этих измерениях.
При какой относительной и
абсолютной погрешности измерений длины и массы (или силы) это изменение
можно надежно обнаружить: а) прямым измерением плотности; б)
гидростатическим взвешиванием. Перечислить побочные источники ошибки при
этих измерениях.
Решение: Дано Δρ/ρ0=0,02 %=2·10-4.
а) Прямым измерением
плотности. Т.к. масса образца не меняется, то меняется его объем
(размеры) и Δρ/ρ0~3 ΔL/L.
При точности 10% относительная погрешность определения длины ΔL/L=1/3 ·1/10
· Δρ/ρ0 =
0,7·10-6 или
0,00007%. При бесконтактном измерении длины (чтобы не смять образец)
ошибка должна быть не менее длины волны ΔL~λ=0,6
мкм. При ΔL/L=0,7·10-6 длина
обраца должна быть не менее L =
ΔL/0,7·10-6= 0,6
мкм/0,7·10-6=0,85·106 мкм
= 0,85 м. Побочные
источники ошибок:
Побочные
источники ошибок:
1 ΔТ, т.к. из-за колебания температуры и Т.К.Р. изменяется размер;
2 Размер печи и секционное регулирования Т;
3 Чистота образца не хуже 99,999%, чтобы не было из-за испарения примесей;
4 Исключить прогиб образца, он должен лежать на теплопроводящей плите из инертного материала;
5 Отсутствие поглощения газов, нагрев в инертной атмосфере специальной очистки.
б) Гидростатическим взвешиванием. Изменение плотности по изменению веса (силы). Относительная погрешность определения силы ~ 0,002 % при точности 10%. При взвешивании с погрешностью ±1 мг вес образца должен быть не менее 1 мг/ 2·10-5 = 0,5 кг.
Задача 15. Вектор
Бюргерса дислокации b в
металле обычно совпадает с кратчайшим вектором трансляции, а плоскость
скольжения Р —
с плоскостью плотнейшей упаковки. Перечислить возможные системы
скольжения в решетке ГЦК. (Считать +b и —b за
один вектор).
Перечислить возможные системы
скольжения в решетке ГЦК. (Считать +b и —b за
один вектор).
Решение: В ГЦК решетке плоскость плотнейшей упаковки – {111}. Направление с кратчайшим вектором трансляции (вектор Бюргерса) – ½ <110>. Для каждой из четырех различно ориентированных плоскостей {111} – (111), (Τ11), (1Τ1), (11Τ) из шести направлений скольжения <110> имеется по три направлений скольжения. Например в плоскости (111) — вектор Бюргерса b = ½ a [0IĪ] или ½ a [Ī0I] или ½ a [101]. В ГЦК решетке все семейства скольжения одинаковы — семейство скольжения <110>{111}, которое (если считать +b и —b за один вектор) содержит 12 систем скольжения – по 3 вектора Бюргерса в каждой из 4 плоскостей сколжения.
Задача 16. В
решетках с неплотной упаковкой скольжение часто возможно по плоскостям
нескольких семейств с наиболее плотной упаковкой. В a-железе
работают первые три из числа наиболее плотноупакованных плоскостей,
содержащих вектор Бюргерса. Перечислить семейства скольжения в a-железе.
Указать число систем скольжения в каждом семействе.
В
решетках с неплотной упаковкой скольжение часто возможно по плоскостям
нескольких семейств с наиболее плотной упаковкой. В a-железе
работают первые три из числа наиболее плотноупакованных плоскостей,
содержащих вектор Бюргерса. Перечислить семейства скольжения в a-железе.
Указать число систем скольжения в каждом семействе.
Рис. 4.1. К
задаче 16. Плоскости и направления скольжения в a-Fe:
а – плоскость семейства {110}, б – {112}, в — {123}
Решение: в a-Fe скольжение
идет вдоль направления <111>, которое соответствует наименьшему для
полной дислокации вектору Бюргерса b=0,5a[111].
Плоскость {110} – наиболее плотноупакованная, а плоскость {112} –
главная плоскость дефекта упаковки. Скольжение в плоскости {123}
проявляется при высоких температурах или при малых скоростях деформации
и любых температурах.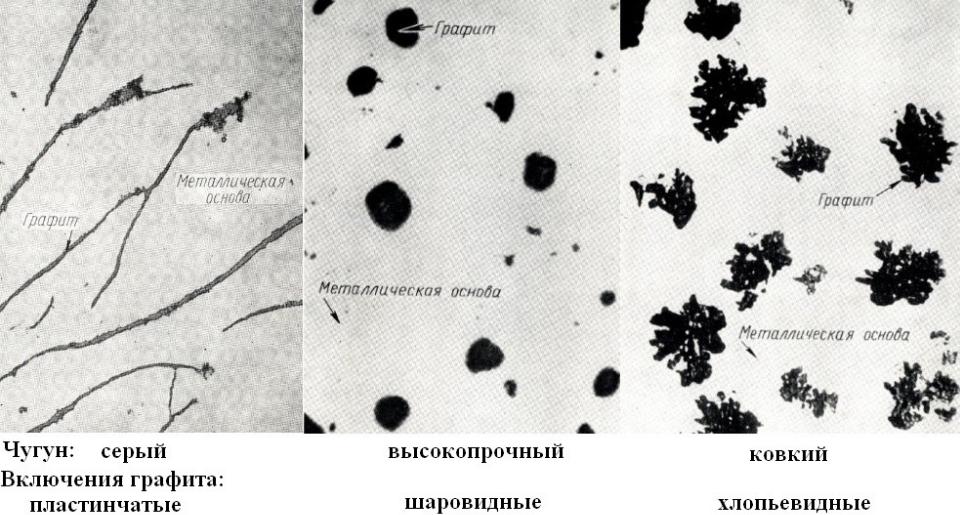 Для каждого из 4-х направлений скольжения типа
<111> расположено по 12 плоскостей, входящих в совокупность {110}, {112}
и {123}, образуя 48 систем скольжения.
Для каждого из 4-х направлений скольжения типа
<111> расположено по 12 плоскостей, входящих в совокупность {110}, {112}
и {123}, образуя 48 систем скольжения.
Задача 17. Показать, что дислокация не может обрываться внутри кристалла. (Указание: Предположим, что дислокация обрывается внутри кристалла. Прямоугольный контур Бюргерса, составленный из ребер призмы, будет замкнут на всех поверхностях, через которые дислокация не проходит; на поверхности, через которую дислокация входит в призму, контур будет не замкнут. Показать, что в этом есть противоречие.)
Решение: Вектор
Бюргерса не зависит от того. На сколько контур Бюргерса удален от
дислокации. Чем дальше от дислокации расположен этот контур, тем меньше
упругие смещения атомов в совершенной области, но тем длиннее контур, и
сумма всех упругих смещений, накопившихся при его обходе, неизменна. Вектор Бюргерса одинаков вдоль всей линии дислокации, т.е. является
инвариантом дислокации.
Вектор Бюргерса одинаков вдоль всей линии дислокации, т.е. является
инвариантом дислокации.
Если дислокация кончается в точке С, то обходя по плоскости скольжения вокруг тоски С (из зоны, где сдвиг b прошел, в зону, где его не было) мы пересекаем какую-то линию разрыва смещения b, т.е. такую же дислокацию. Поэтому дислокация либо образует замкнутый контур, либо заканчивается на некоторой поверхности – границе зерна или границе фаз.
Задача 18. Вектор Бюргерса дислокационной петли одинаков во всех точках. Означает ли это, что и характер дислокации одинаков во всех участках петли?
Решение: Дислокацию кроме вектора Бюргерса b характеризуется еще вектором оси (или линией дислокации) l. Таким образом, дислокация – тензорный объект. Линия дислокации – это граница зоны сдвига, всегда замкнутая линия. В общем случае в плоскости скольжения линия дислокации – кривая. Отдельные малые части этой кривой имеют разную ориентацию линии дислокации l и направления сдвига b, такая дислокация называется смешанная, с разной долей составляющих краевой и винтовой компонентов.
Задача 19. Оценить (в километрах) суммарную длину всех дислокаций в 1 см3 отожженного металла с плотностью дислокаций 108 см-2.
Решение: Плотность дислокаций ρд=108 см-2 , объем металл V=1 см3. Т.к. ρд=Σlд / V, то суммарную длину всех дислокаций Σlд=Vρд= 1 см3 ∙ 108 см-2 = 108 см = 1000 км.
Ответ: 1000 км
Задача 20. Устойчив или неустойчив ряд параллельных винтовых дислокаций в плоскости скольжения?
Решение: Решетка вокруг винтовой дислокации испытывает чисто сдвиговую деформацию. На расстоянии r от оси дислокации касательное напряжение Две параллельных винтовых дислокации действуют друг на друга с силой
Знак (+) соответствует параллельным (одноименным) дислокациям – взаимное отталкивание. Знак (-) соответствует антипараллельным (разноименным) дислокациям — взаимное притяжение (до аннигиляции).
Задача 21. Рассмотрите взаимодействие между двумя краевыми дислокациями с параллельными плоскостями скольжения в кристалле меди, если одна из дислокаций закреплена. Определить силы скольжения и переползания при х=70 Å и у=30 Å.
Решение: При х=70 Å и у=30 Å и параметре решетки меди a=3,61 Å, G=4,55 · 1010 Н/м2, μ=0,35. Межатомное расстояние равно |b|= a/=2,55 Å. Напряжение скольжения = 237 Н/мм2. Сила скольжения на единицу длины
Сила переползания на единицу длины
= 0,022 G, Å = 1,02 · 10-6 Н/мм.
Ответ: 6,07∙10-7 Н/мм и 1,02 · 10-6 Н/мм.
Задача 22. Докажите, что сила взаимодействия параллельных краевой и винтовой дислокаций равна нулю.
Решение:Винтовая дислокация А2В2 создает только сдвиговые напряжения τв, параллельные оси винтовой дислокации. Таким образом τв ┴ bкр. Параллельные винтовая и краевая дислокации не взаимодействуют никак, т.к. в их полях нет ни одной общей компоненты. Краевая дислокация не создает никакого напряжения, действующих на винтовую, и обратно.
Задача 23. По аналогии с ГЦК изобразить дефект упаковки в ГПУ решетке.
Решение:
В решетке ГПУ чередование плотноупакованных слоев при нарушении укладки будет следующим:
Дефект укладки создает прослойку с чередованием слоев АВСА, свойственную для 3-х слойной ГЦК решетки. Вне этой прослойки чередование слоев характерно для 2-х слойной ГПУ решетки — …АВАВ…
Задача 24. Оцените критическое напряжение течения для меди с равномерно распределенными в ней сферическими частицами SiO2 радиусом 10 нм при объемной доле этих частиц, равной 0,1%. (Модуль сдвига G для меди равно 42,4 кН/мм2).
Решение: Радиус сферических частиц r=10 нм c объемной долеq этих частиц f=0,1%=10-3. Для меди a=0,361 нм, G=42,4 кН/мм2. В ГЦК решетке b= a/2=0,26 нм. Объемная доля частиц f=, отсюда
λ=D(π/6f). Критическое напряжение течения
τкр=τо+Δ τдисп= G/30 + Gb/ λ = G ∙ 0,60 = 25,5 кН/мм2.
Ответ: 25,5 кН/мм2.
Задача 25. Оценить минимальное число дислокаций, пробег которых через кристалл никеля приводит к образованию ступеньки на поверхности кристалла, различимой в световом микроскопе. (Период решетки никеля a=0,352 нм, разрешение светового микроскопа — около 0,25 мкм).
Решение: Для никеля a=0,352 нм, Δl=0,25 мкм. В ГЦК решетке b= a/2=0,254 нм ≈ 0,25 нм. Минимальное число дислокаций Nmin= Δl/b = 0,25 мкм / 0,25 нм = 1000 дислокаций.
Ответ: 103.
Задача 26. Оценить температуру конденсации атмосфер Коттрелла в железе с 0,01 % (по массе) N, если энергия взаимодействия краевой дислокации с атомом азота U = 0,5 эВ. Как изменится эта температура после очистки железа до 0,001 % (по массе) Ν?
Решение: Для С1=0,01 % (по массе)=10-4, С2=0,001 % (по массе)=10-5, Е=0,5 эв. Температуру конденсации атмосфер Коттрелла Тк=Е/k lnC-1, т.к. C= C1exp(-E/kT). Для С1=0,01 % (по массе)= 0,01 ат.% (АFe/АN)= 0,01 ат.% (55,85/14) = 0,0399 ат.%. Отсюда Тк1=0,5∙1,6∙10-19 дж / 1,38∙10-23 Дж/К ln C1-1=741 oK = 468 oC. Аналогично, для С2=0,001 % (по массе) Тк2 = 572 oK = 299 oC ≈ 300 oC.
Ответ: 468 oC и 300 oC.
Задача 27. Оценить величину слоя конденсации атмосфер при полном осаждений на дислокациях всего углерода из мартенсита с 0,20% С, если плотность дислокаций ρ=1012 см-2. Какой концентрации углерода достаточно для получения сплошной одноатомной цепочки углерода на всех дислокациях?
Решение: В a-железе параметр решетки равен a=0,2866 нм = 0,2866 ∙ 10—7 см. Сплошная одноатомная цепочка на всех дислокациях при конденсации атомов углерода образуется при концентрации углерода в атомных долях С= ρд a2 = 1012 см-2 ∙ 0,28662 ∙ 10-14 см2= 8,2 10-4 = 8,2 10-2 ат.% = 8,2 10-2 (АN/АFe) % (по массе) =8,2 10-2 ∙(12/55,85) = 1,8 10-2 % (по массе). При осаждений 0,20 %С величина слоя составит 0,20% / 0,018% ≈ 11 атомных слоев.
Ответ: 1,8 10-2 % (по массе) и ≈ 11 атомных слоев углерода.
Задача 28. Начертите и определите структуры решеток совпадения, получающихся в ОЦК-решетке при повороте на 36,9° вокруг оси (100).
Решение:
В ОЦК решетке при повороте на φ=36,9о вокруг оси (100) степень несовпадения узлов Σ=5 . При таких спецориентировках может возникнуть «сверхрешетка», общая для обеих зерен (темные атомы). Узлами такой «сверхрешетки» в плоскости границы будут атомы А и В. Общие для обеих зерен. Для описания таких границ вводится объемная решетка совпадающих узлов (РСУ). Размер ячейки РСУ характеризуется параметром:
Σ=(объем ячейки РСУ) / объем исходной ячейки = 5.
Задача 29. Два ГЦК-кристалла повернуты по отношению друг к другу на 1/2° вокруг оси [112]. Параметр решетки а = 4 Å. Если граница между ними представляет собой симметричную наклонную границу, состоящую из краевых дислокаций, а угол наклона равен 1/2°, то:
а) укажите, что представляет собой плоскость границы;
б) какова суммарная длина дислокаций на единицу площади этой границы?
в) вычислите угол, при котором индивидуальные дислокации, составляющие границу, становятся неразличимыми;
Решение: Для ГЦК решетки а = 4 Å угол разориентировки φ=1/2°=0,0087 рад.
а) Плоскость границы – плоскость типа {110};
б) Связь угла разориентировки φ и расстоянием между дислокациями D в малоугловой симметричной наклонную границе
b/2= D sin φ, или при малых углах D= b/φ.
Т.к. b = a/2,
то расстояние между дислокациями D= a/2φ=4
Å/2∙0,0087
=
398 Å ≈ 400 Å. Если часть линии дислокации равна l=100
Å, то площадь такого участка границы S=l D =
100∙400 Å2 = 4∙104 Å.
При этом суммарная длина дислокаций на единицу площади этой границы ρ = l/S =
100 Å / 4∙104 Å2 =
1 /400 Å=1/400∙10—8 см=2,5∙10-5 см-1.
в) Индивидуальные дислокации неразличимы, если они расположены осень близко одна от другой и теряют свою индивидуальность. Если считать D≈5a, то φ≈ b/5a = a/2∙a = /10 рад ≈ 9,9°.
Ответ: а) {110}; б) 3,1∙105 см-1; в) ≈8о.
Задача 30. Два кристалла имеют простую кубическую решетку с периодом a и общую ось [100]. На ячейку решетки совпадений приходится Σ = 5 узлов кристаллической решетки. Граница проходит по плоскости (010) решетки совпадений. При отклонении зерен от этого положения появляются зернограничные дислокации. В каком диапазоне углов разворота решеток шаг этих дислокаций будет не менее 20a?
Решение: Для простой кубической решетки b = а. Связь угла разориентировки φ и расстоянием между дислокациями D в малоугловой симметричной наклонную границе
b/2= D sinφ, или при малых углах sinφ≈φ и D=b/φ. Отсюда ±Δω=φ= b/D = а / 20а = 0,05 рад = 2,86о.
Ответ: 2,86о
Задача 31. Определите кристаллографические индексы плоскости, в которой находится симметричная малоугловая граница наклона в никеле.
Решение: Ni – ГЦК металл, плоскость скольжения — плотноупакованная плоскость {111}. Полная дислокация с вектором Бюргерса b = а/2 <011>. Вектор Бюргерса b ┴ плоскости границы. Граница совпадает (параллельна) с неполной плоскостью (экстраплоскостью) – (IĪ0), перпендикулярной плоскости (111).
Ответ: Плоскость типа {110}
Задача 32. Определите расстояние между дислокациями в симметричной малоугловой границе наклона в никеле, если угол разориентировки субзерен равен 12′.
Решение: Для никеля a=0,352 нм. В ГЦК решетке b= a/2=0,254нм. Угол разориентировки субзерен φ=12’=0,0035 рад. Расстоянием между дислокациями D в малоугловой симметричной наклонную границе b/2= D sin φ, или при малых углах D= b/φ=0,254 нм / 0,0035 = 72,6 нм ≈ 70 нм.
Ответ: ≈ 70 нм.
содержание .. 20 21 22 23
виды дефектов, устранение, заварка. ужимина
Технология получения изделий из металла литьем известна человечеству более четырех тысячелетий. Металлические предметы — оружие, инструменты, украшения, утварь — составляли существенную часть рукотворного окружения человека.
Дефекты литьяИ с первых же отливок мастеров-металлургов начали преследовать дефекты литья. В древности способы борьбы с дефектами при литье находили интуитивно. Современная металлургия применят для этого научный подход.
Классификация дефектов отливок
В современной металлургии существует несколько классификаций брака при литье.
В зависимости от степени изменения и возможности исправления виды дефектов подразделяют на:
- Условный брак. Отливка имеет недостатки, которые не ухудшают ее рабочие качества. Отливка идет в дальнейшую обработку
- Исправимый брак. Дефекты существенны, но поддаются коррекции тем или иным производственным способом. Например, наплавкой. После исправления брака литья деталь также идет в дальнейшую обработку.
- Окончательный брак. Ремонту не подлежит, поскольку это невыполнимо или очень дорого.
Дефекты литья также делятся по месту их обнаружения. Брак при литье, обнаруженный внутри участка называют внутренним.
Внутренний брак литья
Если же дефект обнаружен при дальнейшей обработке — это внешний брак.
По внешнему проявлению различают следующие основные виды дефектов отливок:
Пригар
Это слой формовочных материалов, спекшихся с металлом, прочно присоединенный к поверхности отливки.
Приливы
Это увеличение размеров отливок, не предусмотренное проектом. Разделяются на
- Заливы.- Возникают по линии стыковки частей формы. Возникают из-за несоблюдения размеров моделей и некачественным соединением частей опок
- Подутость, или распор — получаются из-за давления расплава на рыхлую смесь.
- Нарост возникает вследствие размыва формы потоком расплава при заливке.
- Просечки (гребешки, заусенцы) возникают из-за попадания расплава в повреждения формы или стержня.
Дефекты поверхности
Дефекты при литье часто проявляется в виде пороков поверхности. Сюда относятся
Внешние дефекты литья
- Засоры. Массы зерен земли или шлаков. Вызваны ошибками в проектировании форм, непродуманным расположением литников, несоблюдением технологии складирования и перевозки опок.
- Ужимины возникают при сырой формовке, когда слой земли разрывается в месте конденсации жидкости и в образовавшуюся пустоту затекает расплав.
- Спаи, или неслитины, возникают в зоне контакта слоев охладившегося расплава. Из-за недостаточной температуры эти потоки не могут правильно сплавиться.
- Плены возникают при окислении легирующих добавок.
- Морщинистость, или складчатость, заключается в появлении на поверхности разнонаправленных складок из-за скопления значительных объемов углерода.
- Выпот выглядит как большое количество лопнувших пузырьков и вызывается взрывообразным выделением скоплений графита
- Корольки — дефекты, вызванные разбрызгиванием расплава во время заливки. Шарик металла кристаллизуется и не сплавляется с отливкой.
- Коробление отливки возникает вследствие внутренних напряжений из-за неравномерного остывания
Трещины
Еще один часто встречающийся порок литья — это трещины. Они бывают:
Трещины — деффект литья
- Горячие. Возникают при температуре кристаллизации из-за усадочных напряжений. Приобретают неровный вид.
- Холодные. Возникают при более низких температурах, имеют ровный, прямой профиль.
- Межкристаллические. Свойственны легированным сталям в зонах неметаллических включений.
Газовые дефекты
- Ситовидная пористость — это множество мелких пузырьков в теле детали
- Газовые раковины – каверны большего размера, возникшие из-за выхода и объединения мелких пузырьков.
Изменение структуры металла
Встречается при отливке чугуна, на поверхности детали формируется тонкое включение чугуна другого вида.
Внутренние дефекты
Усадочная пористость
Усадочные пороки возникают ввиду сжатия металла при смене им фазового состояния с жидкого на твердое.
Причины возникновения дефектов
Основные причины возникновения брака при литье
- Несоблюдение технологии литья: режима заливки и охлаждения, состава шихты и земли, порядка изготовления форм и т.п.
- Усадка металла при кристаллизации
- Ошибки при проектировании формы в целом и литниковой системы в особенности
- Недостаточная газопроводимость формы и нарушение вентиляции отливки
Дефект при усадки металла при кристаллизации
При условии соблюдения норм проектирования, состава смесей и технологических режимов литья производство получит качественную отливку, сведя вероятность брака литья к минимуму.
Способы исправления литейного брака
Для исправления поверхностных дефектов применяется механическая обработка — токарная, фрезерная или зачистка.
Фрезерная обработка брака литья
Если при этом размеры детали сократились больше допустимого, применяется наплавка тонкого слоя металла, доводящего размеры до требуемых и, как правило, улучшающего свойства заготовки.
Ультразвуковой неразрушающий метод контроля
Внутренний брак обнаруживается методами неразрушающего контроля. Иногда, если причина образования дефектов — внутренние напряжения, их удается снять путем нагрева и охлаждения по специальной методике. К сожалению, чаще внутренний брак литья исправлению не подлежат.
Объемный анализ | Классификация объемного анализа
Аналитический метод, в котором концентрация вещества в растворе оценивается путем добавления точно такого же количества эквивалентов другого вещества, присутствующего в растворе известной концентрации, называется объемным анализом.Это основной принцип титрования. Другое название объемного анализа — титриметрический анализ. Вещество, раствор которого используется для оценки концентрации неизвестного раствора, называется титрантом.Титрат — это вещество, концентрацию которого необходимо оценить.
Объемный анализ можно разделить на три типа:
Основная цель простого титрования — найти концентрацию неизвестный раствор с помощью другого раствора известной концентрации. Простое титрование снова можно разделить на четыре различных типа:
Кислотно-основное титрование Этот тип титрования используется для определения концентрации кислоты в растворе (или наоборот).Расчетное количество кислоты в растворе можно определить, добавив раствор стандартного основания (или наоборот). Подходящий индикатор добавляется по каплям в раствор, концентрацию которого необходимо оценить. Это помогает определить точку эквивалентности.
Кислотно-щелочной индикатор дает разные цвета различным соединениям. Индикатор выбирается при конкретном титровании на основе диапазона pH индикатора и изменения pH вблизи точки эквивалентности.
Mn + 8H + + 5e — → Mn 2+ + 4H 2 O
Fe 2+ → Fe 3+ + e — ] × 5
Mn + 8H + + 5Fe 2+ → Mn 2+ + 5Fe 3+ + 4H 2 O
(n = 5) (n = 1)
Подкисленный KCr2O7 также можно использовать вместо KmnO 4 .Другими видами окислительно-восстановительного титрования являются йодиметрия, йодометрия и т.д.
I 2 + 2Na 2 S 2 O 3 → 2NaI + Na 2 S 4 O 6
Это, как известно, косвенный метод оценки йод.Здесь окислитель вступает в реакцию с избытком твердого KI. Окислитель окисляет I — до I 2 . Следующим шагом является взаимодействие высвобожденного I 2 с раствором Na 2 S 2 O 3 .
Титрование осаждением
При титровании этой формы соединение с очень низкой растворимостью образуется за счет объединения катионов и анионов. Можно выделить твердый остаток.
AgNO 3 + NaCl → AgCl¯ (белый) + NaNO 3
BaCI 2 + h3SO4 → BaSO 4 ¯ (белый) + 2HCI
CuSO 4 + 4NH 4 OH → [Cu (NH 3 ) 4 ] SO4 + 4h3O
AgNO 3 + 2KCN → K [Ag (CN) 2 ] + KNO 3
Для работы обратного титрования должны быть выполнены определенные условия:
Теперь из колбы извлекается определенный объем «А» (взятые эквиваленты «А» должны быть больше, чем эквиваленты чистого «С» в пробе), а затем выполняется простое титрование с использованием «В». выполнено.
Этот тип титрования выполняется для определения процентного состава смеси щелочных или кислотной смеси. Чтобы определить процентный состав смеси щелочных металлов, рассмотрим твердую смесь NaOH, Na 2 CO 3 и некоторые инертные примеси массой w g.Цель состоит в том, чтобы определить процентный состав этой щелочной смеси. Также предоставляется кислотный реагент (HCl) известной концентрации M1, который может реагировать с пробой щелочи. Смесь сначала растворяют в воде, чтобы получить щелочной раствор, а затем в раствор добавляют два индикатора, а именно фенолфталеин и метиловый оранжевый. Щелочной раствор титруют стандартной HCl. NaOH 2 CO 3 — слабое основание, а NaOH — сильное. Таким образом, очевидно, что NaOH сначала полностью реагирует с HCl, а NaOH 2 CO 3 реагирует только после того, как NaOH полностью нейтрализуется.NaOH + HCl → NaCI + H 2 O… .. (i) После того, как NaOH полностью прореагировал, Na2CO3 начинает реакцию с HCl в два этапа, что показано как
Na 2 CO 3 + HCl → NaHCO 3 + NaCI ……. (ii)
NaHCO 3 + HCl → NaCI + CO 2 + H 2 O …… (iii)
При добавлении HCl в щелочной раствор щелочь нейтрализуется. Это приводит к снижению pH раствора. Вначале pH снижается быстро, так как сильное основание (NaOH) полностью нейтрализуется.Тогда как когда Na 2 CO 3 полностью превращается в NaHCO 3 , раствор остается слабоосновным. Это связано с наличием NaHCO 3 (который слабее по сравнению с Na 2 CO 3 ). Именно в этот момент можно заметить, что фенолфталеин меняет цвет, так как для его изменения требуется слабощелочной раствор.
МЕРЫ ПРЕДОСТОРОЖНОСТИ
сварочных дефектов | Эддифи
- Интернет-магазин
- Служба поддержки клиентов
- О нас
- Карьера
- Свяжитесь с нами
- FR
- CN
- ES
- Продукты
- Приложения
- Отрасли промышленности
- Ресурсы
- Академия Эддифи
- Блог
Приложения
Поиск по активам
Поиск по типу дефекта
- Самолеты и космические аппараты
- Болты и резьбы
- Теплообменники
- Оффшор
- Трубопроводы
- Железная дорога
- суда
- Танки
- Трубы
- Турбины
- Суда
- Дефекты отливки
- Составные дефекты
- Коррозия
- Коррозия под изоляцией (CUI) и противопожарная защита (CUF)
- Трещины
- Дефекты трубок теплообменника
- Картирование коррозии фазированных решеток
- Контроль сварных швов с фазированной решеткой
- Коррозионное растрескивание под напряжением
- Дефекты сварки
О компании Eddyfi Technologies
- О нас
- Наши бренды
- Управленческая команда
- Довольных клиентов
- Новости
- События
Отрасли промышленности
- Академические исследования и обучение
- Аэрокосмическая промышленность
- Энергия
- Продукты питания и напитки
- Тяжелая промышленность и горнодобывающая промышленность
- Морское и судоходство
- Городское водоснабжение и канализация
- Морские и подводные работы
- Производство электроэнергии
- Железнодорожный и автомобильный
- Безопасность и оборона
Ресурсы
- Замечания по применению
- Программное обеспечение
- Технологии
- Видео и вебинары
- Литература
Программное обеспечение
- Эддифи Лифт
- Eddyfi Lyft Pro
- Эддифи Магнифи
- Eddyfi Magnifi GO
- Эддифи Магнифи R
- Eddyfi SurfacePro 3D
- Eddyfi TubePro
- Инуктун ИКОНА
- Inuktun ICON Диагностика
- M2M Приобрести
- Программное обеспечение захвата M2M
- Silverwing CMAP
- Карта пола Среброкрыла
- Серебряное Крыло RMS2
- Silverwing SIMS
- Silverwing Swift GO & Scorpion 2
- Телетест TeleCheck
- Teletest Wavescan
- TSC Ассистент
Технологии
- Полевые измерения переменного тока (ACFM®)
- Вихретоковая матрица (ECA)
- Вихретоковый контроль (ECT)
- Внутренняя поворотная система контроля (IRIS)
- UT большого радиуса действия (LRUT) / Guided Wave
- Утечка магнитного потока (MFL)
- Проверка резервуара на утечку магнитного потока (MFL)
- Массив ближнего поля (NFA)
- Тестирование ближнего поля (NFT)
- Ультразвуковой контроль фазированных решеток (PAUT)
- Импульсный вихретоковый (PEC)
- Удаленный визуальный осмотр (RVI)
- Испытания в дистанционном поле (RFT)
- Тангенциальная вихретоковая решетка (TECA ™)
- Метод полной фокусировки (TFM)
титрование | Определение, типы и факты
Титрование , процесс химического анализа, в котором количество некоторого компонента образца определяется путем добавления к измеряемому образцу точно известного количества другого вещества, с которым желаемый компонент вступает в реакцию в определенном , известная пропорция.Процесс обычно осуществляется путем постепенного добавления стандартного раствора (т.е. раствора известной концентрации) титрующего реагента или титранта из бюретки, по существу, длинной градуированной измерительной трубки с запорным краном и подающей трубкой на ее нижнем конце. . Добавление прекращается при достижении точки эквивалентности.
эксперимент по титрованиюСтаршеклассники проводят эксперимент по титрованию.
© Spencer Grant / age fotostockПодробнее по этой теме
Белок: электрометрическое титрование
При добавлении отмеренных объемов соляной кислоты к раствору белка в бессолевой воде pH снижается пропорционально…
В точке эквивалентности титрования к пробе добавлено точно эквивалентное количество титранта. Экспериментальная точка, в которой завершение реакции отмечается некоторым сигналом, называется конечной точкой. Этот сигнал может быть изменением цвета индикатора или изменением некоторых электрических свойств, которые измеряются во время титрования. Разница между конечной точкой и точкой эквивалентности — это ошибка титрования, которая сохраняется как можно меньше за счет правильного выбора сигнала конечной точки и метода его обнаружения.
Для многих реакций титрования можно найти подходящий визуальный цветной индикатор, который будет указывать на конечную точку в точке эквивалентности или очень близко к ней. Такие титрования, классифицируемые в соответствии с природой химической реакции, происходящей между образцом и титрантом, включают: кислотно-основное титрование, титрование осаждения, титрование комплексообразования и окислительно-восстановительное (окислительно-восстановительное) титрование. При кислотно-основном титровании (т. Е. Титровании кислоты основанием или наоборот) индикатор представляет собой вещество, которое может существовать в двух формах, кислотной форме и основной форме, которые различаются по цвету.Например, лакмус имеет синий цвет в щелочном растворе и красный в кислотном растворе. Фенолфталеин бесцветен в кислотном растворе и красный в щелочном растворе. Доступен широкий выбор кислотно-основных индикаторов, различающихся не только по цвету двух форм, но и по их чувствительности к кислоте или основанию.
титрованиеПолевой геолог, исследующий реакции титрования.
Ryan Mathieu / AlamyОсаждение титрования можно проиллюстрировать на примере определения содержания хлоридов в образце титрованием нитратом серебра, при котором хлорид осаждается в виде хлорида серебра.Присутствие первого небольшого избытка иона серебра (т.е. конечной точки) может быть отмечено появлением окрашенного осадка. Один из способов сделать это — использовать хромат калия в качестве индикатора. Хромат калия реагирует с первым небольшим избытком иона серебра с образованием красного осадка хромата серебра. Другой метод включает использование индикатора адсорбции, действие индикатора основано на образовании на поверхности осадка адсорбированного слоя индикаторной соли серебра, который образуется только при наличии избытка иона серебра.
Получите эксклюзивный доступ к контенту из нашего первого издания 1768 с вашей подпиской. Подпишитесь сегодняНаиболее важные титрования, основанные на реакциях комплексообразования, включают титрование ионов металлов с помощью реагента динатрий этилендиаминтетраацетат (соль эдетовой кислоты или ЭДТА). Индикаторы представляют собой красители, которые обладают свойством образовывать окрашенный комплекс с ионом металла. В процессе титрования реагент сначала реагирует с ионами металлов, не входящими в комплекс, и, наконец, в конечной точке он реагирует с комплексом металл-индикатор.Изменение цвета соответствует превращению комплекса металл-краситель в свободный краситель.
При окислительно-восстановительном (окислительно-восстановительном) титровании действие индикатора аналогично другим видам визуального цветного титрования. В непосредственной близости от конечной точки индикатор подвергается окислению или восстановлению, в зависимости от того, является ли титрант окислителем или восстановителем. Окисленная и восстановленная формы индикатора имеют совершенно разные цвета.
В качестве альтернативы для многих титров конечную точку можно определить с помощью электрических измерений.Эти титры можно классифицировать по измеряемой электрической величине. Потенциометрическое титрование включает измерение разности потенциалов между двумя электродами ячейки; кондуктометрическое титрование, электрическая проводимость или сопротивление; амперометрическое титрование, электрический ток, протекающий в процессе титрования; и кулонометрическим титрованием — общее количество электричества, прошедшего во время титрования. В четырех только что упомянутых титрованиях, за исключением кулонометрического титрования, конечная точка обозначается значительным изменением измеряемой электрической величины.При кулонометрическом титровании измеряется количество электричества, необходимое для проведения известной реакции, и по закону Фарадея рассчитывается количество присутствующего материала.
электрометрическое титрование глицинаЭлектрометрическое титрование глицина.
Encyclopædia Britannica, Inc.Оценка объемных измерений на
- Ресурс исследования
- Исследовать
- Искусство и гуманитарные науки
- Бизнес
- Инженерная технология
- Иностранный язык
- История
- Математика
- Наука
- Социальная наука
Лучшие подкатегории
- Продвинутая математика
- Алгебра
- Базовая математика
- Исчисление
- Геометрия
- Линейная алгебра
- Предалгебра
- Предварительный расчет
- Статистика и вероятность
- Тригонометрия
- другое →
Лучшие подкатегории
- Астрономия
- Астрофизика
- Биология
- Химия
- Науки о Земле
- Наука об окружающей среде
- Науки о здоровье
- Физика
- другое →
Лучшие подкатегории
- Антропология
- Закон
- Политология
- Психология
- Социология
- другое →
Лучшие подкатегории
- Бухгалтерский учет
- Экономика
- Финансы
- Менеджмент
- другое →
Лучшие подкатегории
- Аэрокосмическая техника
- Биоинженерия
- Химическая инженерия
- Гражданское строительство
- Компьютерные науки
- Электротехника
- Промышленное проектирование
- Машиностроение
- Веб-дизайн
- другое →
Лучшие подкатегории
- Архитектура
- Связь
- Английский
- Гендерные исследования
- Музыка
- Исполнительское искусство
- Философия
- Религиоведение
