низкая плотность, высокая температура плавления и коррозионная стойкость
Космический металл, материал будущего, превращающий мечту в реальность — всё это о титане, серебристо-белом, прочном и лёгком. Занимая девятое место по распространённости в природе, он отлично зарекомендовал себя в аэрокосмической и нефтехимической промышленности, машиностроении и медицине. Чудо-металл даже открыт был необычно, а изучение его свойств помогло человечеству выйти на новый уровень развития.
История открытия металла
Всё началось в 1791 году, когда, независимо друг от друга, одновременно У. Грегор (Англия) и М. Г. Клапрот (Германия) получили двуокись титана, но не сумели выделить из неё чистое вещество. Минералог и, по совместительству, сельский священник Грегор изучал чёрный железистый песок, найденный в окрестностях своего прихода. Результатом стало извлечение соединения титана — блестящих крупиц, которые названием «менакин» (от минерала менаканит) увековечили родные места англичанина.
Примерно в это же время химик Клапрот, изучая красные пески, привезённые из Венгрии, нашёл в минерале рутиле новое вещество и назвал его «титан». А, спустя несколько лет, доказал, что рутил и менакеновая земля — одинаковые соединения. В 1825 году шведским химиком Берцелиусом был получен первый образец металлического титана, но это не позволило продвинуться в исследовании свойств, так как примеси делали образец хрупким и неподходящим для механической обработки.
Только в 1925 году голландские химики ван Аркел и де Бур, применив термическое разложение иодида титана, не нашедшее широкого использования, получили вещество с 99,9% чистотой. Такой металл обладал пластичностью, его можно было раскатывать в листы, проволоку и фольгу. Это позволило начать полномасштабное изучение физических и химических свойств, привлечь внимание инженеров и строителей, наметить сферы применения. А уже в 1940 году появился кролловский процесс восстановления четырёххлористого титана магнием, успешно используемый и до сих пор.
Теории происхождения названия
Существует две теории возникновения наименования:
- Первая, подчёркивающая основные свойства металла титана — лёгкость и прочность, связана с именем персонажа германской легенды — эльфийской царицы Титании.
- Другая теория отсылает к древнегреческой мифологии, где титанами называли могучих братьев — божеств второго поколения, детей богов Урана и Геи. Отголоски этого слышатся и в названии элемента урана.
Нахождение титана в природе
Титан занимает почётное четвёртое место по содержанию в земной коре среди важных для человека металлов, уступая только железу, магнию и алюминию. Максимальное его количество сосредоточено в нижнем, базальтовом слое, немного меньше — в гранитном. Принимая во внимание высокую химическую активность, найти титан в чистом виде не представляется возможным. Наиболее распространены четырёхвалентные оксиды, которые концентрируются в рудах коры выветривания и в морской глине.
Сегодня насчитывают до 75 титановых минералов, а учёные периодически заявляют об открытии всё новых форм и соединений. Для промышленной переработки наибольшее значение имеют:
- Ильменит.
- Лейкоксен (продукт изменения ильменита).
- Рутил.
- Титанит (сфен).
- Перовскит.
- Анатаз.
- Титаномагнетит.
- Брукит.
Титан — слабый мигрант, он может переноситься только в виде механических обломков каменной породы или при перемещениях коллоидных илистых слоёв водоёмов. Для биосферы характерно содержание максимальных количеств этого металла в морских водорослях, у животных он обнаружен в шерсти и роговых тканях, в организме человека присутствует в щитовидной железе, селезёнке, надпочечниках и плаценте.
Месторождения космического материала
Самыми распространёнными являются залежи ильменита, они составляют порядка 800 млн тонн. Запасы рутиловых руд значительно меньше, но при сохранении роста добычи все они могут обеспечить человечество ещё на 100 лет. По запасам титана Россия уступает только Китаю и насчитывает 20 разведанных месторождений. Большинство из них — комплексные, где добывают также железо, фосфор, ванадий и цирконий.
Запасы рутиловых руд значительно меньше, но при сохранении роста добычи все они могут обеспечить человечество ещё на 100 лет. По запасам титана Россия уступает только Китаю и насчитывает 20 разведанных месторождений. Большинство из них — комплексные, где добывают также железо, фосфор, ванадий и цирконий.
Обширные залежи располагаются на территории ЮАР, Украины, Канады, США, Бразилии, Австралии, Швеции, Норвегии, Египта, Казахстана, Индии и Южной Кореи. Они различаются содержанием металла в рудах и объёмами добычи, геологические изыскания не прекращаются. Даже на Луне были обнаружены запасы титаносодержащих руд, некоторые из них в десятки раз богаче крупных месторождений Земли. Это позволяет надеяться на снижение рыночных цен металла и расширение сферы использования.
Физические свойства элемента
Titanium — химический элемент периодической таблицы Менделеева, находится в IV группе четвёртого периода. Имеет атомный номер 22, молярную массу 47,867, обозначается символом Ti и проявляет степени окисления от 2 до 4, наиболее устойчивы его четырёхвалентные соединения. При нормальном давлении температура плавления титана равна 1670 ± 2 °C, он относится к цветным тугоплавким металлам и по внешнему виду напоминает сталь.
Имеет атомный номер 22, молярную массу 47,867, обозначается символом Ti и проявляет степени окисления от 2 до 4, наиболее устойчивы его четырёхвалентные соединения. При нормальном давлении температура плавления титана равна 1670 ± 2 °C, он относится к цветным тугоплавким металлам и по внешнему виду напоминает сталь.
Твёрдость, пластичность и предел текучести — важные параметры для любого металла, которые определяют сферу применения. Титан в 12 раз прочнее алюминия, в 4 раза меди и железа. А ещё он гораздо легче их всех (плотность титана всего 4,54 г/см 3) и свободно обрабатывается методами сварки, клёпки, ковки и проката. К важным особенностям относятся низкие показатели теплопроводности и электропроводности, которые остаются неизменными даже при высоких температурах.
Титан проявляет парамагнитные свойства: не намагничивается в магнитном поле, подобно никелю и железу, и не выталкивается, как серебро и золото.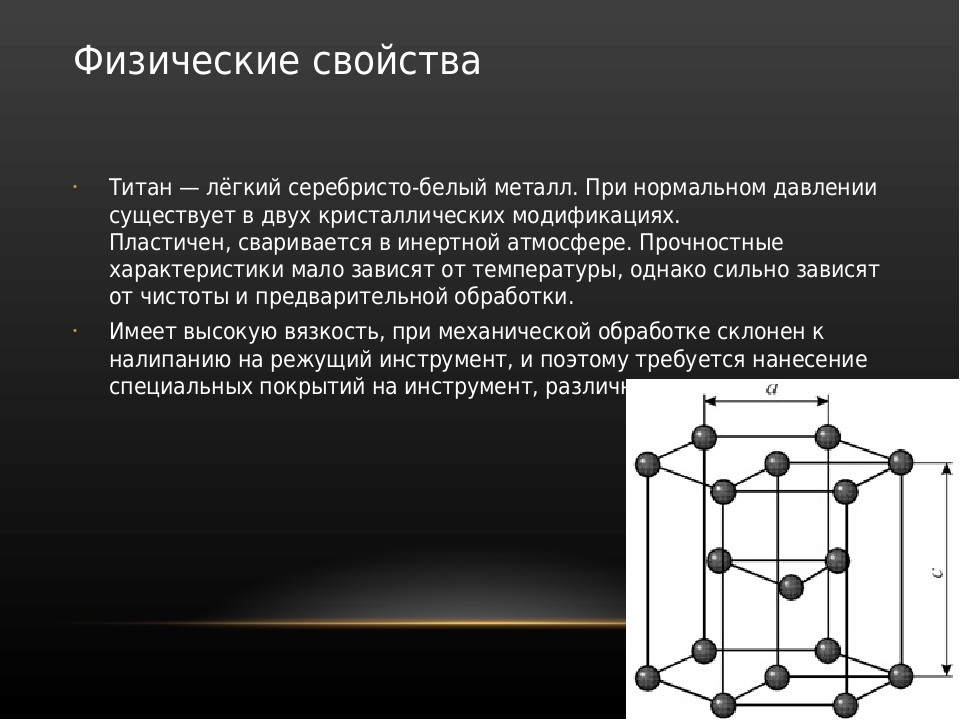
Химические свойства
Высокая коррозийная стойкость объясняется тем, что в нормальных условиях на поверхности металла присутствует оксидная плёнка. Однако в виде порошка, тонкой стружки или проволоки он способен самовоспламеняться и взрываться. Титан устойчив к водным растворам хлора и многим разбавленным щелочам и кислотам, кроме плавиковой, ортофосфорной и серной. Сварку и плавку производят в вакууме, потому что при даже незначительном нагреве проявляется одно из главных свойств титана — активное поглощение газов окружающей атмосферы.
Реакция с водородом, которая начинается при 60 °C, обратима, полученные гидриды при нагревании снова разлагаются. На воздухе при температуре 1200 °C титан пылает ярким белым пламенем, и только он способен гореть в атмосфере азота при температуре выше 400 °C с образованием нитридов. Для взаимодействия с галогенами необходимыми условиями являются отсутствие влаги и наличие катализатора — высокой температуры. При реакции с углеродом получается сверхтвёрдый карбид. С большинством металлов титан образует высокопрочные конструкционные или жаростойкие сплавы и интерметаллические соединения, часто применяется в качестве важного легирующего компонента.
На воздухе при температуре 1200 °C титан пылает ярким белым пламенем, и только он способен гореть в атмосфере азота при температуре выше 400 °C с образованием нитридов. Для взаимодействия с галогенами необходимыми условиями являются отсутствие влаги и наличие катализатора — высокой температуры. При реакции с углеродом получается сверхтвёрдый карбид. С большинством металлов титан образует высокопрочные конструкционные или жаростойкие сплавы и интерметаллические соединения, часто применяется в качестве важного легирующего компонента.
Способ получения из сырья
Исходное сырьё — двуокись титана, содержащая мало посторонних примесей. Для этого нужен рутиловый концентрат, получаемый обогащением руды. Но его мировые запасы невелики, и чаще применяют титановый шлак (синтетический рутил), который получают термической обработкой — обогащением ильменитовых концентратов в электродуговой печи. В результате железо в виде чугуна собирается на дне специальной ванны, и остаётся порошок серого цвета — шлак, содержащий оксид титана.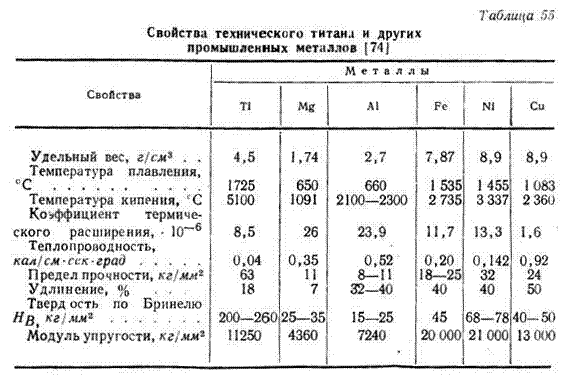
Потом их очищают и в специальных реакторах восстанавливают магнием при 950 °C. На стенках образуется спёкшаяся пористая масса, титановая губка, которую для сепарации от соединений магния прокаливают в вакууме. Чтобы изготовить слитки титана используют плавку полученной губки в вакуумно-дуговых печах. Это предохраняет металл от окисления и способствует окончательному освобождению от примесей. Готовые слитки с чистотой до 99,7% используют для обработки давлением (прокатка, штамповка, ковка).
Основные сферы применения
Сложно описать все области жизни, где нашлось место титану, но среди основных направлений можно отметить:
- Главные потребители — аэрокосмическая отрасль и ракетостроение. Высокая температура плавления и лёгкость являются неоценимыми преимуществами титана при использовании в качестве «летающего» конструкционного материала.
 Для самолёта, например, это элероны и лонжероны, поворотные узлы крыльев, трубопроводы и шпангоуты. Глубоко символично, что в 1980 году установленный в Москве памятник Ю. А. Гагарину сделан из этого космического металла.
Для самолёта, например, это элероны и лонжероны, поворотные узлы крыльев, трубопроводы и шпангоуты. Глубоко символично, что в 1980 году установленный в Москве памятник Ю. А. Гагарину сделан из этого космического металла. - Судостроение тоже нуждается в лёгких и коррозионно-стойких материалах. В конце 70-х годов ХХ века практически весь годовой объем выпуска титана в Советском Союзе пошёл на создание ядерной подводной лодки, где он служил основным конструкционным материалом. Результатом стали снижение на одну треть веса субмарины, её парамагнетизм, максимальные показатели глубины погружения и скорости под водой.
- Титановые пластины применяют в бронежилетах. Вес лёгкого бронежилета — 4 кг, тяжёлого — 10,5 кг. Даже одна такая полоса толщиной всего 5 мм надёжно защищает от пистолетных и ружейных пуль.
- Металл незаменим для нужд химической промышленности ввиду антикоррозийной стойкости в большинстве агрессивных сред и при высоких температурах: приборы и трубопроводы, ёмкости хранения и перегонки, фильтры и запорная арматура.

- Для придания сталям твёрдости и жаропрочности его используют как легирующую добавку.
- Сплавы титана служат для изготовления режущих и хирургических инструментов, ювелирных изделий. Металл не отторгается человеческим телом, поэтому его применяют в медицине для создания имплантатов.
- Издавна здания в европейских городах покрывались цинковыми листами. В ХХ веке для этих нужд был создан экологически чистый и долговечный материал цинк-титан. Его отличная пластичность помогает изготавливать кровли практически всех контуров и формировать любые нестандартные конструкции фасадов.
- Производство стройматериалов, красок, резины, пластмасс, бумаги и пищевых добавок трудно представить без соединений титана. Они востребованы в электротехнике, их можно найти в составе тугоплавких стёкол и керамических деталей, в опорах буровых платформ, работающих в экстремальных морских условиях, и корпусах домашних компьютеров.
Сфера применения титана постоянно расширяется, её сдерживают сложность и энергоёмкость процесса получения чистого вещества. Отчасти поэтому традиционные железо и алюминий сегодня ещё прочно удерживают позиции. Титан — дорогое удовольствие. Цена металла в виде концентрата в сотни раз меньше стоимости готовой продукции, например, листового проката. Сегодня такие расходы доступны далеко не всем, поэтому применение титана определяет уровень экономического развития и обороноспособности государства.
Отчасти поэтому традиционные железо и алюминий сегодня ещё прочно удерживают позиции. Титан — дорогое удовольствие. Цена металла в виде концентрата в сотни раз меньше стоимости готовой продукции, например, листового проката. Сегодня такие расходы доступны далеко не всем, поэтому применение титана определяет уровень экономического развития и обороноспособности государства.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РФ
%PDF-1.6 % 937 0 obj >]/Pages 898 0 R/QITE_DocInfo 934 0 R/Type/Catalog>> endobj 654 0 obj >stream 2015-01-14T13:32:09+06:00Microsoft® Word 20102015-01-15T10:17:22+06:002015-01-15T10:17:22+06:00application/pdf
 adobe.com/pdf/1.3/pdfAdobe PDF Schema
adobe.com/pdf/1.3/pdfAdobe PDF Schemack20TFfv%P=»5zE~74Yj-`(e@?
свойства и применение, сплавы (карбид, оксид)
Титан и сплавы на его основе широко используются в самых разных сферах. Прежде всего, титановые сплавы нашли широкое применение в строительстве различной техники благодаря своей высокой коррозийной стойкости, механической прочности, небольшой плотности, жаропрочности и множеству других характеристик. Рассматривая свойства и применение титана, нельзя не отметить его довольно высокую стоимость. Однако она в полной мере компенсируется характеристиками и долговечностью материала.
Прежде всего, титановые сплавы нашли широкое применение в строительстве различной техники благодаря своей высокой коррозийной стойкости, механической прочности, небольшой плотности, жаропрочности и множеству других характеристик. Рассматривая свойства и применение титана, нельзя не отметить его довольно высокую стоимость. Однако она в полной мере компенсируется характеристиками и долговечностью материала.
Титан имеет высокую прочность и температуру плавления, отличается от других металлов долговечностью.
Основные свойства титана
Титан находится в IV группе четвертого периода периодической системы химических элементов. В самых устойчивых и наиболее важных соединениях элемент является четырехвалентным. Внешне титан напоминает сталь. Является переходным элементом. Температура плавления достигает почти 1700°, а кипения – 3300°. Что касается такого свойства, как скрытая теплота плавления и испарения, то у титана она практически в 2 раза превышает аналогичный показатель для железа.
Имеет 2 аллотропические модификации:
- Низкотемпературную, которая способна существовать до температуры в 882,5°.
- Высокотемпературную, устойчивую от температуры в 882,5° до температуры плавления.
Таблица характеристик титана и его сплавов.
Такие свойства, как удельная теплоемкость и плотность, располагают титан между двумя материалами с наиболее широким конструкционным использованием: железом и алюминием. Механическая прочность титана почти в 2 раза превышает эту характеристику у чистого железа и практически в 6 раз у алюминия. Однако свойства титана таковы, что он способен поглощать в больших количествах водород, кислород и азот, что негативно отражается на пластических характеристиках материала.
Материал характеризуется очень низкой теплопроводностью. Для сравнения, у железа она выше в 4 раза, а у алюминия в 12. Что касается такого свойства, как коэффициент термического расширения, то при комнатной температуре он имеет относительно низкое значение и возрастает с увеличением температуры.
Титан имеет малые модули упругости. При повышении температуры до 350° они начинают уменьшаться практически по линейному закону. Именно этот момент является существенным недостатком материала.
Титан характеризуется довольно большим значением удельного электросопротивления. Оно может колебаться в достаточно широких пределах и зависит от содержания примесей.
Титан является парамагнитным материалом. Для таких веществ характерно снижение магнитной восприимчивости в процессе нагревания. Однако титан является исключением – при повышении температуры его магнитная восприимчивость значительно возрастает.
Читайте также:
Как сделать сварочный стол своими руками.
Можно ли сделать точечную сварку для аккумуляторов 18650 своими руками.
Об изготовлении буржуйки в гараж читайте здесь.
Сферы применения титана
Медицинские инструменты из титанового сплава отличаются высокой коррозионной прочностью, биологической стойкостью и пластичностью.
Свойства материала обеспечивают довольно широкий спектр сфер его применения. Так, в больших объемах сплавы титана используются в строении судов и различной техники. Налажено применение материала в качестве легирующей добавки к сталям высокого качества и в качестве раскислителя. Сплавы с никелем нашли применение в технике и медицине. Такие соединения имеют уникальные свойства, в частности, они обладают памятью формы.
Налажено применение компактного титана в производстве деталей электровакуумных приборов, использующихся в условиях высоких температур. Свойства технического титана позволяют использовать его в производстве клапанов, трубопроводов, насосов, арматуры и других изделий, создаваемых для эксплуатации в агрессивных условиях.
Сплавы характеризуются недостаточной теплопрочностью, однако имеют высокую коррозийную стойкость. Это позволяет использовать различные сплавы на основе титана в химической сфере. К примеру, материал применяется в изготовлении насосов для прокачки серной и соляной кислоты. На сегодняшний день только сплавы на основе этого материала можно использовать в производстве разного рода оборудования для хлорной промышленности.
На сегодняшний день только сплавы на основе этого материала можно использовать в производстве разного рода оборудования для хлорной промышленности.
Использование титана в транспортной промышленности
Сплавы на основе этого материала используются при изготовлении бронетанковой части. А замена разнообразных конструкционных элементов, которые используются в транспортной промышленности, позволяет снижать расход топлива, увеличивать полезную грузоподъемность, повышать предел усталости изделий и улучшать множество других характеристик.
При производстве оборудования для химической промышленности из титана самое важное свойство – коррозионная стойкость металла.
Материал хорошо подходит для использования в строительстве железнодорожного транспорта. Одна из главных задач, которую нужно решить на железных дорогах, связана со снижением мертвого груза. Использование прутков и листов из титана позволяет существенно снизить общую массу состава, уменьшить размеры букс и шеек, сэкономить в тяге.
Вес имеет довольно существенное значение и для прицепного транспорта. Использование титана вместо стали при производстве колес и осей тоже позволяет существенно повысить полезную грузоподъемность.
Свойства материала делают возможным его использование в автомобилестроении. Материал характеризуется оптимальным сочетанием прочностных и весовых свойств для систем отведения отработанных газов и витых пружин. Применение титана и его сплавов позволяет существенно снизить объем отработанных газов, уменьшить затраты топлива и расширить применение лома и производственных отходов путем их переплава. Материал и содержащие его сплавы имеет множество преимуществ по сравнению с прочими используемыми решениями.
Главной задачей разработки новых деталей и конструкций является уменьшение их массы, от которой в той или иной степени зависит движение самого транспортного средства. Снижение веса движущихся узлов и частей делает потенциально возможным сокращение затрат топлива. Детали из титана неоднократно доказывали свою надежность. Они довольно широко применяются в авиакосмической промышленности и конструкциях гоночных автомобилей.
Они довольно широко применяются в авиакосмической промышленности и конструкциях гоночных автомобилей.
Использование этого материала позволяет не только уменьшить вес деталей, но и решить вопрос снижения объема отработанных газов.
Использование титана и его сплавов в сфере строительства
В строительстве широко используется сплав титана с цинком. Этот сплав характеризуется высокими механическими показателями и устойчивостью к коррозии, отличается высокой жесткостью и пластичностью. В составе сплава содержится до 0,2% легирующих добавок, выполняющих функции модификаторов структуры. Благодаря алюминию и меди обеспечивается требуемая пластичность. Кроме того, использование меди позволяет повысить предельную прочность материала на растяжение, а сочетание химических элементов способствует снижению коэффициента расширения. Сплав применяется и для производства длинных лент и листов с хорошими эстетическими характеристиками.
Титан часто используется в космических технологиях благодаря его легкости, прочности и тугоплавкости.
Среди главных качеств сплава титана с цинком, важных конкретно для строительства, можно отметить такие химические и физические свойства, как высокая устойчивость к коррозии, хороший внешний вид и безопасность для человеческого здоровья и окружающей среды.
Материал отличается хорошей пластичностью, без проблем поддается глубокой вытяжке, что позволяет использовать его в кровельных работах. У сплава нет никаких проблем с пайкой. Именно поэтому различные объемные конструкции и нестандартные архитектурные элементы вроде куполов и шпилей изготавливаются из цинк-титана, а не меди или оцинкованной стали. В решении подобных задач данный сплав является незаменимым.
Сфера использования сплава очень широка. Его применяют в фасадных и кровельных работах, из него изготавливаются изделия различной конфигурации и практически любой сложности, он широко применяется в производстве разнообразных декоративных изделий типа водостоков, отливов, кровельных коньков и т.д.
Этот сплав отличается очень продолжительным сроком службы. Более столетия он не будет требовать покраски и частых текущих ремонтных работ. Также среди существенных преимуществ материала следует выделить его способность восстанавливаться. Несущественные повреждения в виде царапин от веток, птиц и т.п. через какое-то время устраняются сами по себе.
Более столетия он не будет требовать покраски и частых текущих ремонтных работ. Также среди существенных преимуществ материала следует выделить его способность восстанавливаться. Несущественные повреждения в виде царапин от веток, птиц и т.п. через какое-то время устраняются сами по себе.
Требования к строительным материалам становятся все более серьезными и строгими. Исследовательские компании ряда стран изучали почву вокруг зданий, построенных с использованием сплава цинка и титана. Результаты исследований подтвердили, что материал является полностью безопасным. Он не имеет канцерогенных свойств и не вредит человеческому здоровью. Цинк-титан является негорючим стройматериалом, что дополнительно повышает безопасность.
С учетом всех перечисленных положительных характеристик такой строительный материал в эксплуатации приблизительно в 2 раза дешевле, чем кровельная медь.
У сплава две степени окисления. С течением времени он меняет цвет и теряет металлический блеск. Сначала цинк-титан становится светло-серым, а еще через некоторое время приобретает благородный темно-серый оттенок. В настоящее время материал намеренно подвергается химическому старению.
С течением времени он меняет цвет и теряет металлический блеск. Сначала цинк-титан становится светло-серым, а еще через некоторое время приобретает благородный темно-серый оттенок. В настоящее время материал намеренно подвергается химическому старению.
Использование титана и его сплавов в медицине
Титан отлично совместим с человеческой тканью, поэтому активно применяется в области эндопротезирования.
Титан нашел широкое применение и в медицинской сфере. Среди преимуществ, которые позволили ему стать таким популярным, нужно отметить высокую прочность и устойчивость к коррозии. Кроме того, ни у одного из пациентов не было выявлено аллергии на титан.
В медицине применяются коммерчески чистый титан и сплав Ti6-4Eli. С его использованием изготавливаются хирургические инструменты, разнообразные внешние и внутренние протезы, вплоть до сердечных клапанов. Из титана производятся инвалидные коляски, костыли и прочие приспособления.
Ряд исследований и экспериментов подтверждает отличную биологическую совместимость материала и его сплавов с живой человеческой тканью. =>>
=>>
v
История открытия:
Открытие TiO2 сделали практически одновременно и независимо друг от друга англичанин У. Грегор и немецкий химик М. Г. Клапрот. У. Грегор, исследуя состав магнитного железистого песка (Крид, Корнуолл, Англия, 1789), выделил новую «землю» (оксид) неизвестного металла, которую назвал менакеновой. В 1795 г. немецкий химик Клапрот открыл в минерале рутиле новый элемент и назвал его титаном, позднее установил, что рутил и менакеновая земля — оксиды одного и того же элемента. Первый образец металлического титана получил в 1825 году Й. Я. Берцелиус. Чистый образец Ti получили голландцы А. ван Аркел и И. де Бур в 1925 термическим разложением паров иодида титана TiI4
Физические свойства:
Титан — легкий серебристо-белый металл. Пластичен, сваривается в инертной атмосфере.
Имеет высокую вязкость, при механической обработке склонен к налипанию на режущий инструмент, и поэтому требуется нанесение специальных покрытий на инструмент, различных смазок.
Химические свойства:
При обычной температуре покрывается защитной пассивирующей пленкой оксида, коррозионностоек, но при измельчении в порошок горит на воздухе. Титановая пыль может взрываться (температура вспышки 400°С).
При нагревании на воздухе до 1200°C титан сгорает с образованием оксидных фаз переменного состава TiOx.
Титан устойчив к разбавленным растворам многих кислот и щелочей (кроме HF, H3PO4 и концентрированной H2SO4), однако легко реагирует даже со слабыми кислотами в присутствии комплексообразователей, например, с плавиковой кислотой HF образует комплексный анион [TiF6]2-.
При нагревании титан взаимодействует с галогенами. С азотом выше 400°C титан образует нитрид TiNx(x=0,58-1,00). При взаимодействии титана с углеродом образуется карбид титана TiCx (x=0,49-1,00).
Титан поглощает водород, образуя соединения переменного состава TiHx. При нагревании эти гидриды разлагаются с выделением H2.
Титан образует сплавы со многими металлами.
В соединениях титан проявляет степени окисления +2, +3 и +4. Наиболее устойчива степень окисления +4.
Важнейшие соединения:
Диоксид титана, ТiO2. Белый порошок, желтый в нагретом состоянии, плотностъ 3,9-4,25 г/см3. Амфотерен. В концентрированной Н2SO4 растворяется лишь при длительном нагревании. При сплавлении с содой Na2CO3 или поташом K2CO3 оксид TiO2 образует титанаты:
TiO2 + K2CO3 = K2TiO3 + CO2
Гидроксид титана(IV), TiO(OH)2*xH2O, осаждается из растворов солей титана, его осторожным прокаливанием получают оксид TiO2. Гидроксид титана(IV) амфотерен.
Тетрахлорид титана, TiCl4, при обычных условиях — желтоватая, сильно дымящая на воздухе жидкость, что объясняется сильным гидролизом TiCl4 парами воды и образованием мельчайших капелек HCl и взвеси гидроксида титана. Кипящей водой гидролизуется до титановой кислоты(??). Для хлорида титана(IV) характерно образование продуктов присоединения, например TiCl4*6NH3, TiCl4*8NH3, TiCl4*PCl3 и т.д. При растворении хлорида титана(IV) в НСl образуется комплексная кислота H2[TiCl6], неизвестная в свободном состоянии; её соли Me2[TiCl6] хорошо кристаллизуются и устойчивы на воздухе.
Восстановлением TiCl4 водородом, алюминием, кремнием, другими сильными восстановителями, получены трихлорид и дихлорид титана TiCl3 и TiCl2 — твердые вещества с сильными восстановительными свойствами.
Нитрид титана — представляет собой фазу внедрения с широкой областью гомогенности, кристаллы с кубической гранецентрированной решеткой. Получение — азотированием титана при 1200 °C или другими способами. Применяется как жаропрочный материал, для создания износостойких покрытий.
Применение:
В виде сплавов. Металл применяется в химической промышленности (реакторы, трубопроводы, насосы), лёгких сплавах, остеопротезах. Является важнейшим конструкционным материалом в авиа-, ракето-, кораблестроении.
Титан является легирующей добавкой в некоторых марках стали.
Нитинол (никель-титан) — сплав, обладающий памятью формы, применяется в медицине и технике.
Алюминиды титана являются очень стойкими к окислению и жаропрочными, что в свою очередь определило их использование в авиации и автомобилестроении в качестве конструкционных материалов.
В виде соединений Белый диоксид титана используется в красках (например, титановые белила), а также при производстве бумаги, пластиков. Пищевая добавка E171.
Титанорганические соединения (напр. тетрабутоксититан) применяются в качестве катализатора и отвердителя в химической и лакокрасочной промышленности.
Неорганические соединения титана применяются в химической электронной, стекловолоконной промышленности в качестве добавки.
Матигоров А.В.
ХФ ТюмГУ
Источники:
???
Титан | Химические свойства
Титан
Чистый титан — химически активный переходный элемент, в соединениях имеет степени окисления +4, реже +3 и +2. При обычной температуре и вплоть до 500-550 °С покрывается защитной пленкой оксида TiO2, благодаря этому коррозионностоек.
С кислородом воздуха заметно взаимодействует при температуре выше 600 °С с образованием ТiO2. Тонкая титановая стружка при недостаточной смазке может загораться в процессе механической обработки. При достаточной концентрации кислорода в окружающей среде и повреждении окисной пленки путем удара или трения возможно загорание металла при комнатной температуре и в сравнительно крупных кусках.
Оксидная пленка не защищает титан в жидком состоянии от дальнейшего взаимодействия с кислородом (в отличие, например, от алюминия), и поэтому его плавка и сварка должны проводиться в вакууме, в атмосфере нейтрального газа или под флюсом. Титан обладает способностью поглощать атмосферные газы и водород, образуя хрупкие сплавы, непригодные для практическое использования; при наличии активированной поверхности поглощение водорода происходит уже при комнатной температуре с небольшой скоростью, которая значительно возрастает при 400 °С и выше. Растворимость водорода в титане является обратимой, и этот газ можно удалить почти полностью отжигом в вакууме.
С азотом титан реагирует при температуре выше 700 °С, причем получаются нитриды типа TiN; в виде тонкого порошка или проволоки титан может гореть в атмосфере азота. Скорость диффузии азота и кислорода в титане значительно ниже, чем водорода. Получаемый в результате взаимодействия с этими газами слой отличается повышенными твердостью и хрупкостью и должен удаляться с поверхности титановых изделий путем травления или механической обработки. Титан энергично взаимодействует с сухими галогенами, по отношению к влажным галогенам устойчив, так как влага играет роль ингибитора.
Металл устойчив в азотной кислоте всех концентраций (за исключением красной дымящейся, вызывающей коррозионное растрескивание титана, причем реакция иногда идет со взрывом), в слабых растворах серной кислоты (до 5% по массе). Соляная, плавиковая, концентрированная серная, а также горячие органических кислоты: щавелевая, муравьиная и трихлоруксусная реагируют с титаном.
Титан коррозионно устойчив в атмосферном воздухе, морской воде и морской атмосфере, во влажном хлоре, хлорной воде, горячих и холодных растворах хлоридов, в различных технологических растворах и реагентах, применяемых в химической, нефтяной, бумагоделательной и других отраслях промышленности, а также в гидрометаллургии. Титан образует с С, В, Se, Si металлоподобные соединения, отличающиеся тугоплавкостью и высокой твердостью. Карбид TiC (tпл 3140 °С) получают нагреванием смеси TiO2 с сажей при 1900-2000 °С в атмосфере водорода; нитрид TiN (tпл 2950 °С) — нагреванием порошка Титан в азоте при температуре выше 700 °С. Известны силициды TiSi2
Механические свойства титановых сплавов таблица. Титан и титановые сплавы
Титан и сплавы на его основе обладают высокой коррозионной стойкостью и удельной прочностью. Недостатками титана являются его активное взаимодействие с атмосферными газами, склонность к водородной хрупкости. Титан плохо обрабатывается резанием, удовлетворительно – давлением, сваривается в защитной атмосфере. Широко распространено вакуумное литье.
Титан имеет две модификации: низкотемпературную (до 882 С) – β титан с ГПУ решеткой, высокотемпературную -β-титан с ОЦК решеткой.
Легирующие элементы влияют на эксплуатационные свойства титана следующим образом:
Fe, Аl,Mn,Cr,Sn,V,Si– повышают его проность, но снижают пластичность и вязкость;
Al,Zr,Mo– увеличивают жаропрочность;
Mo,Zr,Nb,Ta,Pb– увеличивают коррозионную стойкость.
Классификация титановых сплавов . Структура промышленных сплавов титана – это твердые растворы легирующих элементов вαи β модификациях титана. Сплавы титана в зависимости от их стабильной структуры (после отжига) при комнатной температуре подразделяют на три основные группы:α– сплавы; (α+β)-сплавы и β-сплавы.
Титановые сплавы классифицируют также по технологии производства (деформируемые, литейные, порошковые), по физико-химическим, в том числе механическим, свойствам (высокопрочные, обычной прочности, высокопластичные, жаропрочные, коррозионностойкие).
Деформируемые титановые сплавы . Большинство титановых сплавов легировано алюминием, повышающим жесткость, прочность, жаропрочность и жаростойкость материала.
α – титановые сплавы термической обработкой не упрочняются. Широкое применение нашел сплав ВТ5-1, обладающий хорошей свариваемостью, жаропрочностью, кислотостойкостью, пластичностью при криогенных температурах. Обрабатывается давлением в горячем состоянии, термически стабилен до 450 С. Добавки олова в сплав улучшают его технологичесмкие и механические свойства.
Из сплава ВТ5-1 изготавливают листы, поковки, трубы, проволоку, профили.
(α+ β)- титановые сплавы упрочняются термической обработкой, состоящей из закалки и старения. Они хуже свариваются.
Типичным представителем этой группы является сплав ВТ6, характеризующийся оптимальным сочетанием технологических и механических свойств. Уменьш
Каковы свойства титана? (с иллюстрациями)
Основные физические свойства титана как металлического химического элемента включают его немагнитные свойства, низкую плотность и жесткое отношение прочности к массе. Впервые он был обнаружен в Англии в 1791 году преподобным Уильямом Грегором, который также был минерологом, который первоначально назвал этот металл манакканитом в честь прихода Маннаккана в Корнуолле, Англия, где он его обнаружил. Титановая руда часто встречается в земной коре в виде минералов, таких как ильменит или титанат железа, FeTiO 3 , и рутил, более известный как диоксид титана, TiO 2 .
Титановое кольцо.Химические свойства титана включают его коррозионную стойкость, что делает его пригодным для использования в медицинских инструментах, так как он не взаимодействует химически с тканями человека. Его устойчивость ко многим формам кислот делает его полезным в промышленных применениях, где перерабатываются едкие химические вещества.Титан также является одним из немногих элементов, которые могут гореть в отсутствие кислорода. В атмосфере чистого азота он будет реагировать при температуре 1470 ° по Фаренгейту (800 ° Цельсия) с образованием нитрида титана, TiN.
Диоксид титана используется в некоторых молочных продуктах, в том числе в молоке, для усиления белого цвета.Диоксид титана — широко используемое соединение металла, применяемое в виде пигмента в красках, лосьонах для загара и пищевых красителях. Подавляющая часть титановой руды, которая добывается во всем мире, превращается в чистую форму TiO 2 , в то время как остальная часть легирована такими металлами, как ванадий и алюминий, для использования в конструкционных поверхностях, где она весит на 40% меньше, чем усиленная углеродом стали.
Минеральные свойства оксидов соединений титана привели к трудностям очистки после их открытия. Чистый титан на уровне 99,9% металла был выделен только 119 лет спустя Мэтью Хантером в 1910 году, металлургом из Новой Зеландии, который назвал этот метод очистки процессом Хантера.Дополнительные методы очистки металла были открыты в 1936 году, а к 1948 году его мировое производство выросло до трех тонн в год. Вскоре это число резко увеличилось из-за уникальных свойств титана, а мировое производство в 2011 году оценивается в 223 000 метрических тонн.
Высокие механические свойства титана делают его незаменимым в конструкциях планеров самолетов, в которых широко используется металл, и, начиная с 2006 года, мировые цены на титан в авиастроении начали быстро расти.Отчасти это связано с тем, что очистка металла стоит дорого, а очистка стоит в пять раз дороже, чем алюминий. Стоимость изготовления слитков металлического титана и готовых металлических изделий в 10 раз выше стоимости алюминия. Спрос на чистый титан на мировом рынке также в 10 000 раз меньше, чем на рынке стали, что способствует колебаниям цен. По состоянию на 2005 год странами, стремящимися стать крупнейшими переработчиками титана, были Япония и Китай, за которыми следуют Россия и Соединенные Штаты.
Титан не вступает в реакцию с тканями человека, поэтому его часто используют для имплантации зубов.История Разработок и приложений | Центр обработки титана
- 888-771-9449
- Продукты
- Титановый стержень
- Титановый лист
- Титановая труба
- Титановая пластина
- Резьбовой стержень и проволока
- Титановая трубка
- Титановые отводы
- Титановые фланцы
- Титановые заглушки
- Резьбовые фитинги и заглушки
- Услуги
- Пильный лист
- Ленточнопильный станок
- Гидроабразивная резка
- Стрижка
- марки титана
- CP Титановая направляющая
- CP Титановый лист данных
- CP Grade 1 Свойства
- CP Grade 2 Свойства
- CP Grade 3 Свойства
- CP Grade 4 Свойства
- Титановая направляющая из сплава
- Grade 5 / 6Al-4V Свойства
- Марка 7 / Ti-0.15Pd Недвижимость
- Grade 12 Properties
- Grade 23 / 6Al-4V Eli Properties
- Цирконий
- Технические данные
- История титана
- Использование титана
- Фрезерный Титан
- Титан против стали и алюминия
- Условия покупки
- Политика качества и заявление о миссии Условия продажи
- (PDF)
- О нас
- Главный офис
- Расположение офисов продаж
- Карьера
- Блог
- Бизнес, сертифицированный WBENC
- AS9100: 2016 и ISO9001: 2015
- Ответ на COVID-19
- Свяжитесь с нами
- Запросить цену
- Продукты
- — Титановый стержень
- — Титановый лист
- — Титановая труба
- — Титановая пластина
- — Резьбовой стержень и проволока
- — Титановые трубки
- — Титановые отводы
- — Титановые фланцы
- — титановые заглушки
- — Резьбовые фитинги и заглушки
- Услуги
- — Распил листовой
- — Ленточнопильный станок
- — Гидроабразивная резка
- — Стрижка
- марки титана
- — Титановая направляющая CP
- — Лист технических данных CP Titanium
- — CP Grade 1 Свойства
- — CP Grade 2 Свойства
- — CP Grade 3 Свойства
- — CP Grade 4 Свойства
- — Титановый сплав
Потрясающие возможности применения титана в повседневной жизни
Значительно длинный список применений титана показывает, почему это один из самых востребованных металлов в различных отраслях промышленности.От изготовления ювелирных изделий и медицинского оборудования до авиационной и морской техники — титан используется повсеместно.
Титан — это химический элемент, который в чистом виде обычно характеризуется блеском и металлически-белым цветом. Он получил свое название от греческого слова titanos , относящегося к титанам из греческой мифологии. Титан в изобилии присутствует на Солнце и в метеоритах и является девятым по содержанию элементом земной коры.
Хотите написать для нас? Что ж, мы ищем хороших писателей, которые хотят распространять информацию.Свяжитесь с нами, и мы поговорим …
Давайте работать вместе!
В 1946 году, через 155 лет после его открытия, Уильям Джастин Кролл показал, что можно производить титан путем восстановления тетрахлорида титана магнием. С течением времени этот элемент приобрел широкую известность, и большая заслуга в этом принадлежит его использованию, которое, похоже, со временем увеличивается.
Свойства титана
| атомный номер: 22 | Атомная масса: 47.867 (1) |
| Точка плавления: 3034 ° F | Точка кипения: 5949 ° F |
| Прочный и легкий | Коррозионностойкий |
Если сегодня титан считается таким полезным, то именно благодаря этим свойствам он может похвастаться. Он прочный, как сталь, но очень легкий. Фактически, он известен своим превосходным соотношением прочности и веса. Металл устойчив к коррозии при более высоких температурах из-за образовавшегося на нем защитного оксидного покрытия.
Применение титана
В основном этот элемент используется из его сплавов. Из общего объема титана, производимого в промышленных масштабах, примерно 65 процентов используется для изготовления сплавов путем смешивания его со сталью. Благодаря своей превосходной прочности, его добавляют в различные металлы, включая сталь, для повышения их прочности и устойчивости к коррозии. Также известно, что сплав легче.Например, сплав титана и стали будет весить меньше, чем вес чистой стали.
Титановые кольца
»Обладая прочностью и устойчивостью к вмятинам, титан довольно популярен в ювелирной промышленности. На самом деле, титановые кольца и ремешки стали модным явлением в последнее время и уступили место своим золотым и серебряным аналогам. Металл также используется для производства небольших искусственных драгоценных камней, которые относительно мягче настоящих драгоценных камней.
»В оправе очков используются сплавы титана, что делает их очень прочными, легкими и долговечными. Сегодня даже ноутбуки и сотовые телефоны изготавливают из титана.
»Будучи легким и прочным, титан также используется в производстве огнестрельного оружия, где он заменил сталь и алюминий как наиболее предпочтительный металл.
Гольф-клубы
»В спорте титан используется для изготовления разнообразного спортивного оборудования, такого как клюшки для гольфа, теннисные ракетки, биты для крикета, хоккейные клюшки, решетки для шлема, рамы велосипедов и т. Д.Помимо гоночных велосипедов, он также используется в гоночных велосипедах и автомобилях, поскольку обеспечивает прочность и долговечность без увеличения веса машины.
»Диоксид титана, одно из важнейших соединений этого элемента, в основном используется при производстве белой краски. Кроме того, он также используется в производстве зубной пасты, бумаги и пластика.
Хотите написать для нас? Что ж, мы ищем хороших писателей, которые хотят распространять информацию. Свяжитесь с нами, и мы поговорим…
Давайте работать вместе!
»Относительно новой записью в длинном списке применений титана является титановая посуда и изделия из металла, которые со временем становятся все более популярными. В частности, титановая посуда, а также палатки и фонари из этого металла очень популярны среди туристов.
»Благодаря своей непрозрачности он широко используется в промышленности, например, для ультразвуковой сварки и пайки волной припоя.
»Поскольку тетрахлорид титана выделяет густые пары во влажном воздухе, он используется для письма на небе, которое осуществляется путем выделения соединения с самолета, а также для дымовых завес.
Тазобедренный сустав
Зубные имплантаты
»В области медицины титан используется для изготовления кардиостимуляторов, заменителей тазобедренных и коленных суставов, костылей, зубных имплантатов, хирургических инструментов, а также костных пластин и винтов. Человек, использующий титановые зубные имплантаты, может пройти МРТ, поскольку эти имплантаты не магнитные.
»Титан также используется для производства самолетов и космических аппаратов, т.е.е., рама и детали двигателя этих машин. Из первых применений титана в области аэрокосмической техники его использование при производстве SR-71 «Blackbird» в 1960-х годах было самым популярным. Фактически, это был первый случай, когда он широко использовался в самолетах. Со временем его применение в этой области расширилось в разы, и недавние примеры самолетов, в которых широко использовался титан, включают такие, как Boeing и Airbus.
»Прочность этого металла и его способность противостоять соленой воде делают его чрезвычайно популярным компонентом морской техники.Он широко используется для изготовления гребных валов и других подобных элементов корабля, которые длительное время подвергаются воздействию соленой воды. Эта коррозионная стойкость также делает титан важным компонентом опреснительных установок, в которых соленая вода превращается в пресную.
Архитектурные чудеса из титана
В последнее время титан также стал популярным в области архитектурной инженерии благодаря своей превосходной прочности и относительно меньшему весу.Интересно, что его металлический белый цвет, который тесно связан с исследованием космоса, способствовал его использованию в нескольких памятниках; один из самых ярких примеров — 350-футовый памятник покорителям космоса в Москве.
Памятник покорителям космоса
350-футовый памятник покорителям космоса, покрытый титаном, был построен в 1964 году возле Выставки достижений народного хозяйства (ныне Всероссийский выставочный центр) в Москве в честь выдающихся достижений советского народа. в сфере освоения космоса.
Памятник Юрию Гагарину
Мемориал Юрию Гагарину — титановая статуя советского космонавта высотой 131 фут, возведенная в честь того, что он стал первым человеком в космосе, — еще одно архитектурное чудо, построенное из этого металла.
Как ни удивительно это может звучать, но обнаруживаемое количество титана также содержится в нашем организме. Считается, что мы принимаем примерно 0,8 мг одного и того же вещества каждый день, и то же самое проходит через организм, не всасываясь.В человеческом организме титан не токсичен и не реагирует, а это означает, что он не причинит нам вреда, даже если бы существовал в относительно больших количествах; это также объясняет, почему он широко используется в ряде медицинских процедур.

 Для самолёта, например, это элероны и лонжероны, поворотные узлы крыльев, трубопроводы и шпангоуты. Глубоко символично, что в 1980 году установленный в Москве памятник Ю. А. Гагарину сделан из этого космического металла.
Для самолёта, например, это элероны и лонжероны, поворотные узлы крыльев, трубопроводы и шпангоуты. Глубоко символично, что в 1980 году установленный в Москве памятник Ю. А. Гагарину сделан из этого космического металла.