Титановый порошок: титан и Ti сплавы. Марки и составы титанового порошка
Производство
Порошки титана и его сплавов получают в АО «ПОЛЕМА» восстановлением оксидов металлов гидридом кальция, — способом, разработанным в 50-ых годах прошлого века в ЦНИИЧМ им. И.П.Бардина. Выбор гидрида кальция в качестве восстановителя объясняется высокой активностью кальция, позволяющей восстанавливать практически все окислы металлов и неметаллов независимо от их термодинамической активности. При этом не образуются твердые растворы и химические соединения кальция с восстановленными металлами.
Применение
Восстановленные порошки титана и сплавов имеет неправильную (иррегулярную) форму и развитую поверхность частиц, благодаря чему отлично формуются при сравнительно низких давлениях прессования в жестких матрицах, а также методом гидростатического прессования в эластичных оболочках. Порошки хорошо прокатываются в ленту и спекаются в вакууме или нейтральной атмосфере.
Порошки титана и сплавов на основе титана применяются в производстве коррозионностойких фильтров тонкой очистки технических жидкостей в виде пористого проката, в медицине для изготовления имплантов, в пищевой промышленности для изготовления регенерируемых фильтров в системах очистки питьевой и минеральной воды, соков и напитков, в производстве пиротехнических средств высокой надежности, пористых нераспыляемых геттеров (газопоглотителей) с высокой сорбционной емкостью и скоростью сорбции, а также для изготовления композитов с алюминием и другими металлами, деталей часовых механизмов и кислотостойкого оборудования. Порошки применяются также для плазменного и микроплазменного напыления покрытий.
1. Титановые порошки
Марки и химический состав
| Марки | Ti |
Примеси, масс. %, не более %, не более |
|||||
| N | C | H |
Fe+Ni |
Si | Cl | ||
| ПТК-1 | основа | 0,07 | 0,05 | 0,35 | 0,35 | 0,10 | 0,003 |
| ПТК-2 | основа | 0,20 | 0,05 | 0,35 | 0,35 | 1,00 | 0,003 |
| ПТС-1 | 0,08 | 0,05 | 0,35 | 0,40 | 0,10 | 0,004 | |
| ПТС-2 | основа | 0,20 | 0,05 | 0,35 | 0,40 | 1,00 | 0,004 |
| ПТМ-1 | основа | 0,08 | 0,05 | 0,35 | 0,40 | 0,10 | 0,004 |
|
ПТМ-2 ПТМ(А)-2 |
основа | 0,08 | 0,05 | 0,35 | 0,40 | 0,10 | 0,004 |
| ПТОМ-1 | основа | 0,08 | 0,05 | 0,40 | 0,40 | 0,10 | 0,004 |
| ПТОМ-2 | основа | 0,20 | 0,05 | 0,40 | 0,40 | 1,00 | 0,004 |
|
№ примера |
Ti |
Примеси, масс. % % |
|||||||||
| C | O | N | Ca | Fe | Ni | Si | Al | Mg | |||
| 1 | основа | 0,046 | 0,25 | 0,08 | 0,002 | 0,22 | 0,050 | 0,17 | 0,040 | 0,01 | <0,01 |
| 2 | основа | 0,024 | 0,30 | 0,060 | 0,002 | 0,18 | 0,040 | 0,057 | 0,038 | 0,05 | <0,01 |
| 3 | основа | 0,045 | 0,28 | 0,050 | 0,003 | 0,30 | 0,030 | 0,040 | 0,032 | <0,02 | <0,02 |
Размер частиц, насыпная плотность и уплотняемость порошков
|
Марки |
Гранулометрический состав, масс. %, по фракциям, мкм %, по фракциям, мкм |
Насыпная плотность, г/см3 * | Уплотняемость, г/см3, при давлении МПа * | ||||
| +280 | +100 | +45(40) | -45(40) | 200 | 600 | ||
| ПТК | ≤ 5,0 | Баланс (остальное) | ≤ 10 | 0,89 | 2,70 | 3,50 | |
| ПТС | ≤ 1,0 | Не опр. | ≥ 25 (35) | Баланс | 2,60 | 3,24 | |
| ПТМ | 0,0 | ≤ 2,0 | ≥ 15(25) | Баланс | 1,02 | 2,44 | 3,35 |
| ПТОМ | 0,0 | ≤ 1,0 | ≤ 5,0 (5,0) | Баланс | 1,36 | 2,72 | 3,48 |
* Средние значения (справочные данные)
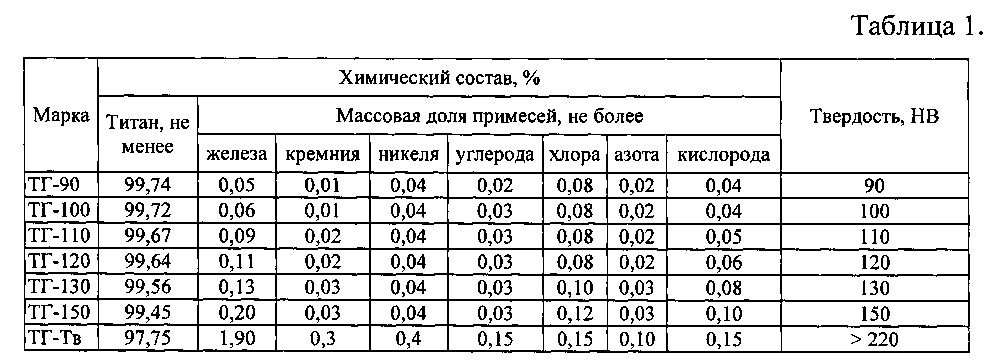
Спецификацией (ТУ) устанавливается норма насыпной плотности для порошка ПТК: 0,6-1,0 г/см
 рис. 1
рис. 2
рис. 1
рис. 2*рис. 1: ПТМ. Распределение частиц по размерам.
*pис. 2: Форма частиц порошка.
По согласованию с заказчиком допускается другие требования к химическому и гранулометрическому составам. В частности, для плазменного напыления покрытий изготавливается титановый порошок фракций 40-100, 40-140, 63-160 мкм.
2.Порошок ПТ51Ц49 (Ti51Zr49) сплава
| Ti | Zr | Примеси, масс. % не более | |||||||
| C | N | O | Ni | Mg | Fe | Si | Al | ||
| 50,5-53,0 | остальное | 0,10 | 0,10 | 0,50 | 0,14 | 0,014 | 0,10 | 0,10 | 0,10 |
-
Размер частиц порошка (основная фракция) менее 100 мкм.

По согласованию с клиентом могут быть установлены другие требования к химическому составу и размеру частиц порошка.
Распределение компонентов в сплаве Ti51Zr49 мас.%
| Ti | Zr | Примеси, масс. % | |||||||
| C | N | O | Ni | Mg | Fe | Si | Al | ||
| 50,8 | остальное | 0,096 | 0,053 | 0,22 | 0,057 | 0,01 | 0,022 | 0,055 | 0,025 |
3. Порошок ПТФ (Ti70V30) сплава
Порошок ПТФ (Ti70V30) сплава
| Марка | Массовая доля элементов, % | Примеси, %, не более | Насыпная плотность, г/см3, не более | |||||
| Ti | V | N | C | H | Ca | O | ||
| ПТФ |
65 не менее |
25-32 | 0,30 | 0,10 | 0,60 | 0,20 | 0,50 | 1,2 |
-
Размер частиц порошка (основная фракция) менее 100 мкм.

| Ti | V | Примеси, масс. % | ||||
| N | C | H | Ca | O | ||
| основа | 28,83 | 0,046 | 0,042 | 0,29 | 0,20 | 0,28 |
4. Другие порошковые сплавы с титаном:
ПВ-Н55Т45 (Ni55Ti45), ПВ-Т88Н12 (Ti88Ni12), ПВ-Т65Ю35 (Ti65Al35)
Порошки данного класса применяются преимущественно для нанесения покрытий и изготовления деталей методом ПМ
Преимущества
- Высокоразвитая поверхность частиц порошков, обеспечивающая уникальные физико-химические свойства материалов и изделий из них для применения в различных областях техники, медицине и пищевой промышленности в качестве фильтров, сорбционных насосов (газопоглотителей), пиротехнических систем, имплантов и композитов
- Отличная прессуемость порошков
- Высокая структурная однородность порошковых сплавов и интерметаллидов с титаном
Титановые сплавы Википедия
У этого термина существуют и другие значения, см. Титан.
Титан.| Титан | |
|---|---|
| ← Скандий | Ванадий → | |
Стержень, состоящий из титановых кристаллов высокой чистоты | |
| Название, символ, номер | Тита́н / Titanium (Ti), 22 |
| Атомная масса (молярная масса) | 47,867(1)[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d2 4s2 |
| Радиус атома | 147 пм |
| Ковалентный радиус | 132 пм |
| Радиус иона | (+4e)68 (+2e)94 пм |
| Электроотрицательность | 1,54 (шкала Полинга) |
| Электродный потенциал | −1,63 |
| Степени окисления | 2, 3, 4 |
| Энергия ионизации (первый электрон) | 657,8 (6,8281[2]) кДж/моль (эВ) |
Плотность (при н. у.) у.) | 4,54 г/см³ |
| Температура плавления | 1670 °C 1943 K |
| Температура кипения | 3560 K |
| Уд. теплота плавления | 18,8 кДж/моль |
| Уд. теплота испарения | 422,6 кДж/моль |
| Молярная теплоёмкость | 25,1[3] Дж/(K·моль) |
| Молярный объём | 10,6 см³/моль |
| Структура решётки | гексагональная плотноупакованная (α-Ti) |
| Параметры решётки | a=2,951 с=4,697 (α-Ti) |
| Отношение c/a | 1,587 |
| Температура Дебая | 380 K |
| Теплопроводность | (300 K) 21,9 Вт/(м·К) |
| Номер CAS | 7440-32-6 |
Тита́н — химический элемент с атомным номером 22[4]. Принадлежит к 4-й группе периодической таблицы химических элементов (по устаревшей короткой форме периодической системы принадлежит к побочной подгруппе IV группы, или к группе IVB), находится в четвёртом периоде таблицы. Атомная масса элемента 47,867(1) а. е. м.[1]. Обозначается символом Ti. Простое вещество титан — лёгкий прочный металл серебристо-белого цвета. Обладает высокой коррозионной стойкостью.
Атомная масса элемента 47,867(1) а. е. м.[1]. Обозначается символом Ti. Простое вещество титан — лёгкий прочный металл серебристо-белого цвета. Обладает высокой коррозионной стойкостью.
История
Открытие диоксида титана (TiO2) сделали практически одновременно и независимо друг от друга англичанин У. Грегор и немецкий химик М. Г. Клапрот. У. Грегор, исследуя состав магнитного железистого песка (Крид, Корнуолл, Англия, 1791), выделил новую «землю» (оксид) неизвестного металла, которую назвал менакеновой. В 1795 году немецкий химик Клапрот открыл в минерале рутиле новый элемент и назвал его титаном. Спустя два года Клапрот установил, что рутил и менакеновая земля — оксиды одного и того же элемента, за которым и осталось название «титан», предложенное Клапротом. Через 10 лет открытие титана состоялось в третий раз: французский учёный Л. Воклен обнаружил титан в анатазе и доказал, что рутил и анатаз — идентичные оксиды титана.
Первый образец металлического титана получил в 1825 году швед Й. Я. Берцелиус. Из-за высокой химической активности титана и сложности его очистки чистый образец Ti получили голландцы А. ван Аркел и И. де Бур в 1925 году термическим разложением паров иодида титана TiI4.
Я. Берцелиус. Из-за высокой химической активности титана и сложности его очистки чистый образец Ti получили голландцы А. ван Аркел и И. де Бур в 1925 году термическим разложением паров иодида титана TiI4.
Титан не находил промышленного применения, пока люксембуржец Г. Кролл (англ.)русск. в 1940 году не запатентовал простой магниетермический метод восстановления металлического титана из тетрахлорида; этот метод (процесс Кролла (англ.)русск.) до настоящего времени остаётся одним из основных в промышленном получении титана.
Происхождение названия
Металл получил своё название в честь титанов, персонажей древнегреческой мифологии, детей Геи. Название элементу дал Мартин Клапрот в соответствии со своими взглядами на химическую номенклатуру в противовес французской химической школе, где элемент старались называть по его химическим свойствам. Поскольку немецкий исследователь сам отметил невозможность определения свойств нового элемента только по его оксиду, он подобрал для него имя из мифологии, по аналогии с открытым им ранее ураном.
Нахождение в природе
Титан находится на 10-м месте по распространённости в природе. Содержание в земной коре — 0,57 % по массе, в морской воде — 0,001 мг/л[5]. В ультраосновных породах 300 г/т, в основных — 9 кг/т, в кислых 2,3 кг/т, в глинах и сланцах 4,5 кг/т. В земной коре титан почти всегда четырёхвалентен и присутствует только в кислородных соединениях. В свободном виде не встречается. Титан в условиях выветривания и осаждения имеет геохимическое сродство с Al2O3. Он концентрируется в бокситах коры выветривания и в морских глинистых осадках. Перенос титана осуществляется в виде механических обломков минералов и в виде коллоидов. До 30 % TiO2 по весу накапливается в некоторых глинах. Минералы титана устойчивы к выветриванию и образуют крупные концентрации в россыпях. Известно более 100 минералов, содержащих титан. Важнейшие из них: рутил TiO2, ильменит FeTiO3, титаномагнетит FeTiO3 + Fe3O4, перовскит CaTiO3, титанит (сфен) CaTiSiO5. Различают коренные руды титана — ильменит-титаномагнетитовые и россыпные — рутил-ильменит-цирконовые[3].
Различают коренные руды титана — ильменит-титаномагнетитовые и россыпные — рутил-ильменит-цирконовые[3].
Месторождения
Крупные коренные месторождения титана находятся на территории ЮАР, России, Украины, Канады, США, Китая, Норвегии, Швеции, Египта, Австралии, Индии, Южной Кореи, Казахстана; россыпные месторождения имеются в Бразилии, Индии, США, Сьерра-Леоне, Австралии[3][6]. В странах СНГ ведущее место по разведанным запасам титановых руд занимает РФ (58,5 %) и Украина (40,2 %)[7]. Крупнейшее месторождение в России — Ярегское.
Запасы и добыча
Основные руды: ильменит (FeTiO3), рутил (TiO2), титанит (CaTiSiO5).
По данным на 2002 год, 90 % добываемого титана использовалось на производство диоксида титана TiO2. Мировое производство диоксида титана составляло 4,5 млн т. в год. Подтверждённые запасы диоксида титана (без России) составляют около 800 млн т. На 2006 год, по оценке Геологической службы США, в пересчёте на диоксид титана и без учёта России, запасы ильменитовых руд составляют 603—673 млн т. , а рутиловых — 49,7—52,7 млн т[8]. Таким образом, при нынешних темпах добычи мировых разведанных запасов титана (без учёта России) хватит более чем на 150 лет.
, а рутиловых — 49,7—52,7 млн т[8]. Таким образом, при нынешних темпах добычи мировых разведанных запасов титана (без учёта России) хватит более чем на 150 лет.
Россия обладает вторыми в мире, после Китая, запасами титана. Минерально-сырьевую базу титана России составляют 20 месторождений (из них 11 коренных и 9 россыпных), достаточно равномерно рассредоточенных по территории страны. Самое крупное из разведанных месторождений (Ярегское) находится в 25 км от города Ухта (Республика Коми). Запасы месторождения оцениваются в 2 миллиарда тонн руды со средним содержанием диоксида титана около 10 %[9].
Крупнейший в мире производитель титана — российская компания «ВСМПО-АВИСМА»[10].
Получение
Как правило, исходным материалом для производства титана и его соединений служит диоксид титана со сравнительно небольшим количеством примесей. В частности, это может быть рутиловый концентрат, получаемый при обогащении титановых руд. Однако запасы рутила в мире весьма ограничены, и чаще применяют так называемый синтетический рутил или титановый шлак, получаемые при переработке ильменитовых концентратов.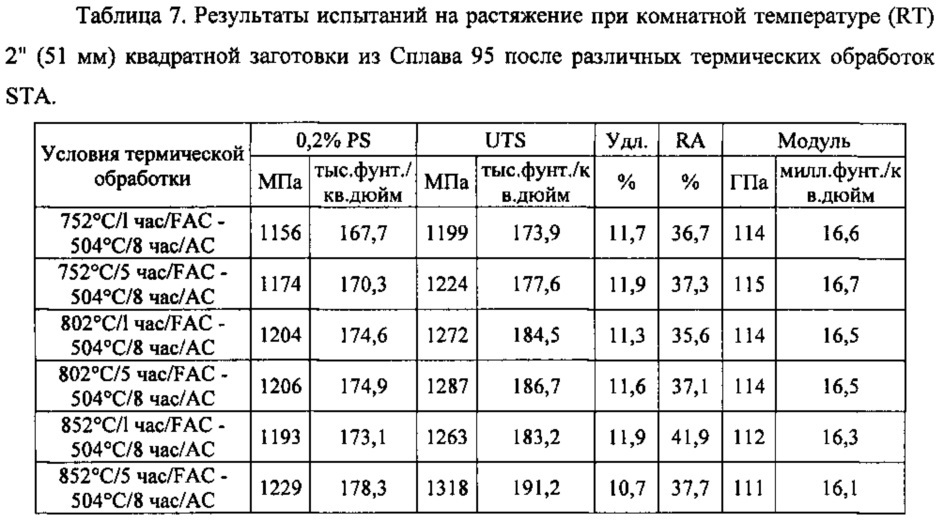 Для получения титанового шлака ильменитовый концентрат восстанавливают в электродуговой печи, при этом железо отделяется в металлическую фазу (чугун), а невосстановленные оксиды титана и примесей образуют шлаковую фазу. Богатый шлак перерабатывают хлоридным или сернокислотным способом.
Для получения титанового шлака ильменитовый концентрат восстанавливают в электродуговой печи, при этом железо отделяется в металлическую фазу (чугун), а невосстановленные оксиды титана и примесей образуют шлаковую фазу. Богатый шлак перерабатывают хлоридным или сернокислотным способом.
Концентрат титановых руд подвергают сернокислотной или пирометаллургической переработке. Продукт сернокислотной обработки — порошок диоксида титана TiO2. Пирометаллургическим методом руду спекают с коксом и обрабатывают хлором, получая пары тетрахлорида титана TiCl4:
- TiO2+2C+2Cl2→TiCl4+2CO{\displaystyle {\mathsf {TiO_{2}+2C+2Cl_{2}\rightarrow TiCl_{4}+2CO}}}
Образующиеся пары TiCl4 при 850 °C восстанавливают магнием:
- TiCl4+2Mg→2MgCl2+Ti{\displaystyle {\mathsf {TiCl_{4}+2Mg\rightarrow 2MgCl_{2}+Ti}}}
Кроме этого, в настоящее время начинает получать популярность так называемый процесс FFC Cambridge, названный по именам его разработчиков Дерека Фрэя, Тома Фартинга и Джорджа Чена из Кембриджского университета, где он был создан. Этот электрохимический процесс позволяет осуществлять прямое непрерывное восстановление титана из оксида в расплаве смеси хлорида кальция и негашёной извести (оксида кальция). В этом процессе используется электролитическая ванна, наполненная смесью хлорида кальция и извести, с графитовым расходуемым (либо нейтральным) анодом и катодом, изготовленным из подлежащего восстановлению оксида. При пропускании через ванну тока температура быстро достигает ~1000—1100 °C, и расплав оксида кальция разлагается на аноде на кислород и металлический кальций:
Этот электрохимический процесс позволяет осуществлять прямое непрерывное восстановление титана из оксида в расплаве смеси хлорида кальция и негашёной извести (оксида кальция). В этом процессе используется электролитическая ванна, наполненная смесью хлорида кальция и извести, с графитовым расходуемым (либо нейтральным) анодом и катодом, изготовленным из подлежащего восстановлению оксида. При пропускании через ванну тока температура быстро достигает ~1000—1100 °C, и расплав оксида кальция разлагается на аноде на кислород и металлический кальций:
- 2CaO→2Ca+O2{\displaystyle {\mathsf {2CaO\rightarrow 2Ca+O_{2}}}}
Полученный кислород окисляет анод (в случае использования графита), а кальций мигрирует в расплаве к катоду, где и восстанавливает титан из его оксида:
- O2+C→CO2{\displaystyle {\mathsf {O_{2}+C\rightarrow CO_{2}}}}
- TiO2+2Ca→Ti+2CaO{\displaystyle {\mathsf {TiO_{2}+2Ca\rightarrow Ti+2CaO}}}
Образующийся оксид кальция вновь диссоциирует на кислород и металлический кальций, и процесс повторяется вплоть до полного преобразования катода в титановую губку либо исчерпания оксида кальция. Хлорид кальция в данном процессе используется как электролит для придания электропроводности расплаву и подвижности активным ионам кальция и кислорода. При использовании инертного анода (например, диоксида олова), вместо углекислого газа на аноде выделяется молекулярный кислород, что меньше загрязняет окружающую среду, однако процесс в таком случае становится менее стабильным, и, кроме того, в некоторых условиях более энергетически выгодным становится разложение хлорида, а не оксида кальция, что приводит к высвобождению молекулярного хлора.
Хлорид кальция в данном процессе используется как электролит для придания электропроводности расплаву и подвижности активным ионам кальция и кислорода. При использовании инертного анода (например, диоксида олова), вместо углекислого газа на аноде выделяется молекулярный кислород, что меньше загрязняет окружающую среду, однако процесс в таком случае становится менее стабильным, и, кроме того, в некоторых условиях более энергетически выгодным становится разложение хлорида, а не оксида кальция, что приводит к высвобождению молекулярного хлора.
Полученную титановую «губку» переплавляют и очищают. Рафинируют титан иодидным способом или электролизом, выделяя Ti из TiCl4. Для получения титановых слитков применяют дуговую, электронно-лучевую или плазменную переработку.
Физические свойства
Титан — лёгкий серебристо-белый металл. При нормальном давлении существует в двух кристаллических модификациях: низкотемпературный α-Ti с гексагональной плотноупакованной решёткой (гексагональная сингония, пространственная группа C6mmc, параметры ячейки a = 0,2953 нм, c = 0,4729 нм, Z = 2) и высокотемпературный β-Ti с кубической объёмно-центрированной упаковкой (кубическая сингония, пространственная группа Im3m, параметры ячейки a = 0,3269 нм, Z = 2), температура перехода α↔β 883 °C, теплота перехода ΔH=3,8 кДж/моль[3] (87,4 кДж/кг[11]). Большинство металлов при растворении в титане стабилизируют β-фазу и снижают температуру перехода α↔β[3]. При давлении выше 9 ГПа и температуре выше 900 °C титан переходит в гексагональную фазу (ω-Ti)[11]. Плотность α-Ti и β-Ti соответственно равна 4,505 г/см³ (при 20 °C) и 4,32 г/см³ (при 900 °C)[3]. Атомная плотность α-титана 5,67⋅1022 ат/см³[12][13].
Большинство металлов при растворении в титане стабилизируют β-фазу и снижают температуру перехода α↔β[3]. При давлении выше 9 ГПа и температуре выше 900 °C титан переходит в гексагональную фазу (ω-Ti)[11]. Плотность α-Ti и β-Ti соответственно равна 4,505 г/см³ (при 20 °C) и 4,32 г/см³ (при 900 °C)[3]. Атомная плотность α-титана 5,67⋅1022 ат/см³[12][13].
Температура плавления титана при нормальном давлении равна 1670 ± 2 °C, или 1943 ± 2 К (принята в качестве одной из вторичных калибровочных точек температурной шкалы ITS-90 (англ.)русск.)[2]. Температура кипения 3287 °C[2]. При достаточно низкой температуре (-80 °C)[2] , титан становится довольно хрупким. Молярная теплоёмкость при нормальных условиях Cp = 25,060 кДж/(моль·K), что соответствует удельной теплоёмкости 0,523 кДж/(кг·K)[2]. Теплота плавления 15 кДж/моль[11], теплота испарения 410 кДж/моль[11]. Характеристическая дебаевская температура 430 К[11]. Теплопроводность 21,9 Вт/(м·К) при 20 °C[11]. Температурный коэффициент линейного расширения 9,2·10−6 К−1 в интервале от −120 до +860 °C[11]. Молярная энтропия α-титана S0 = 30,7 кДж/(моль·К)[2]. Для титана в газовой фазе энтальпия формирования ΔH0
Характеристическая дебаевская температура 430 К[11]. Теплопроводность 21,9 Вт/(м·К) при 20 °C[11]. Температурный коэффициент линейного расширения 9,2·10−6 К−1 в интервале от −120 до +860 °C[11]. Молярная энтропия α-титана S0 = 30,7 кДж/(моль·К)[2]. Для титана в газовой фазе энтальпия формирования ΔH0
f = 473,0 кДж/моль, энергия Гиббса ΔG0
f = 428,4 кДж/моль, молярная энтропия S0 = 180,3 кДж/(моль·К), теплоёмкость при постоянном давлении Cp = 24,4 кДж/(моль·K)[2]
Удельное электрическое сопротивление при 20 °C составляет 0,58 мкОм·м[11] (по другим данным 0,42 мкОм·м[3]), при 800 °C 1,80 мкОм·м[3]. Температурный коэффициент сопротивления 0,003 К−1 в диапазоне 0…20 °C[11].
Пластичен, сваривается в инертной атмосфере. Прочностные характеристики мало зависят от температуры, однако сильно зависят от чистоты и предварительной обработки[3]. Для технического титана твёрдость по Виккерсу составляет 790—800 МПа, модуль нормальной упругости 103 ГПа, модуль сдвига 39,2 ГПа[11]. У высокочистого предварительно отожжённого в вакууме титана предел текучести 140—170 МПа, относительное удлинение 55—70 %, твёрдость по Бринеллю 716 МПа[3].
Для технического титана твёрдость по Виккерсу составляет 790—800 МПа, модуль нормальной упругости 103 ГПа, модуль сдвига 39,2 ГПа[11]. У высокочистого предварительно отожжённого в вакууме титана предел текучести 140—170 МПа, относительное удлинение 55—70 %, твёрдость по Бринеллю 716 МПа[3].
Имеет высокую вязкость, при механической обработке склонен к налипанию на режущий инструмент, и поэтому требуется нанесение специальных покрытий на инструмент, различных смазок.
При обычной температуре покрывается защитной пассивирующей плёнкой оксида TiO2, благодаря этому коррозионностоек в большинстве сред (кроме щелочной).
Температура перехода в сверхпроводящее состояние 0,387 К. При температурах выше 73 кельвин титан парамагнитен. Магнитная восприимчивость при 20 °C составляет 3,2·10−6[3]. Постоянная Холла α-титана равна +1,82·10−13[3].
Изотопы
Известны изотопы титана с массовыми числами от 38 до 63 (количество протонов 22, нейтронов от 16 до 41), и 2 ядерных изомера.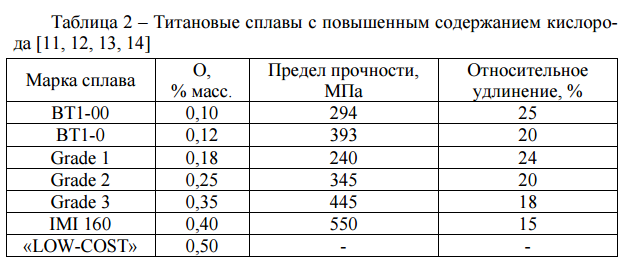
Природный титан состоит из смеси пяти стабильных изотопов: 46Ti (изотопная распространенность 7,95 %), 47Ti (7,75 %), 48Ti (73,45 %), 49Ti (5,51 %), 50Ti (5,34 %).
Среди искусственных изотопов самые долгоживущие 44Ti (период полураспада 60 лет) и 45Ti (период полураспада 184 минуты).
Химические свойства
Устойчив к коррозии благодаря оксидной плёнке, но при измельчении в порошок, а также в тонкой стружке или проволоке титан пирофорен[3]. Титановая пыль имеет свойство взрываться. Температура вспышки — 400 °C. Титановая стружка пожароопасна.
Титан устойчив к разбавленным растворам многих кислот и щелочей (кроме HF, H3PO4 и концентрированной H2SO4). Титан устойчив к влажному хлору и водным растворам хлора[2].
Легко реагирует даже со слабыми кислотами в присутствии комплексообразователей, например, с плавиковой кислотой HF он взаимодействует благодаря образованию комплексного аниона [TiF6]2−. Титан наиболее подвержен коррозии в органических средах, так как в присутствии воды на поверхности титанового изделия образуется плотная пассивная плёнка из оксидов и гидрида титана. Наиболее заметное повышение коррозионной стойкости титана заметно при повышении содержания воды в агрессивной среде с 0,5 до 8,0 %, что подтверждается электрохимическими исследованиями электродных потенциалов титана в растворах кислот и щелочей в смешанных водно-органических средах[14].
Титан наиболее подвержен коррозии в органических средах, так как в присутствии воды на поверхности титанового изделия образуется плотная пассивная плёнка из оксидов и гидрида титана. Наиболее заметное повышение коррозионной стойкости титана заметно при повышении содержания воды в агрессивной среде с 0,5 до 8,0 %, что подтверждается электрохимическими исследованиями электродных потенциалов титана в растворах кислот и щелочей в смешанных водно-органических средах[14].
При нагревании на воздухе до 1200 °C Ti загорается ярким белым пламенем с образованием оксидных фаз переменного состава TiOx. Из растворов солей титана осаждается гидроксид TiO(OH)2·xH2O, осторожным прокаливанием которого получают оксид TiO2. Гидроксид TiO(OH)2·xH2O и диоксид TiO2амфотерны.
TiO2 взаимодействует с серной кислотой при длительном кипячении. При сплавлении с содой Na2CO3 или поташом K2CO3 оксид TiO2 образует титанаты:
- TiO2+K2CO3→K2TiO3+CO2{\displaystyle {\mathsf {TiO_{2}+K_{2}CO_{3}\rightarrow K_{2}TiO_{3}+CO_{2}}}}
При нагревании Ti взаимодействует с галогенами (например, с хлором — при 550 °C[2]). Тетрахлорид титана TiCl4 при обычных условиях — бесцветная жидкость, сильно дымящая на воздухе, что объясняется гидролизом TiCl4, содержащимися в воздухе парами воды и образованием мельчайших капелек HCl и взвеси гидроксида титана.
Тетрахлорид титана TiCl4 при обычных условиях — бесцветная жидкость, сильно дымящая на воздухе, что объясняется гидролизом TiCl4, содержащимися в воздухе парами воды и образованием мельчайших капелек HCl и взвеси гидроксида титана.
Восстановлением TiCl4водородом, алюминием, кремнием, другими сильными восстановителями, получен трихлорид и дихлорид титана TiCl3 и TiCl2 — твёрдые вещества, обладающие сильными восстановительными свойствами. Ti взаимодействует с Br2 и I2.
С азотом N2 выше 400 °C титан образует нитрид TiNx (x = 0.58—1.00). Титан — единственный элемент, который горит в атмосфере азота[2].
При взаимодействии титана с углеродом образуется карбид титана TiCx (x = 0.49—1.00).
При нагревании Ti поглощает H2 с образованием соединения переменного состава TiHx (x = 2.00—2.98). При нагревании эти гидриды разлагаются с выделением H2.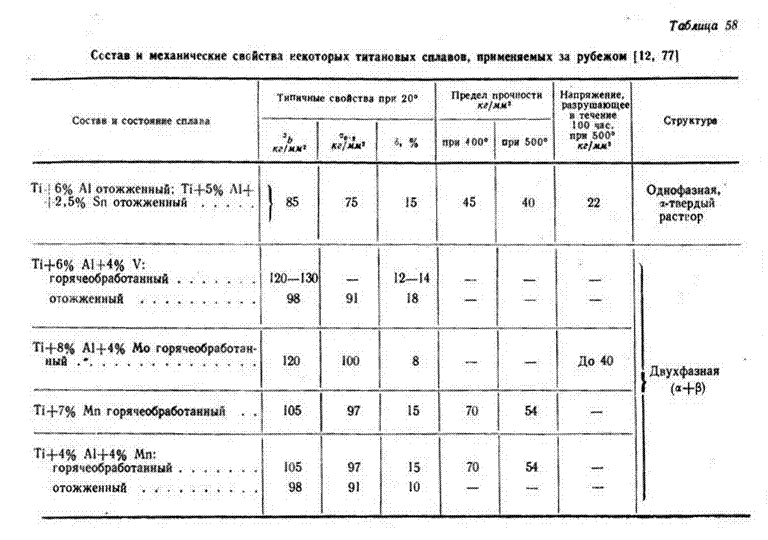
Титан образует сплавы и интерметаллические соединения со многими металлами.
Применение
В чистом виде и в виде сплавов
Часы из титанового сплава Заготовка титанового шпангоута истребителя F-15 до и после прессования на штамповочном прессе компании Alcoa усилием 45 тыс. тонн, май 1985Использование металлического титана во многих отраслях промышленности обусловлено тем, что его прочность примерно равна прочности стали при том, что он на 45 % легче. Титан на 60 % тяжелее алюминия, но прочнее его примерно вдвое[2].
- Титан в виде сплавов является важнейшим конструкционным материалом в авиа- и ракетостроении, в кораблестроении.
- Металл применяется в химической промышленности (реакторы, трубопроводы, насосы, трубопроводная арматура), военной промышленности (бронежилеты, броня и противопожарные перегородки в авиации, корпуса подводных лодок), промышленных процессах (опреснительных установках, процессах целлюлозы и бумаги), автомобильной промышленности, сельскохозяйственной промышленности, пищевой промышленности, спортивных товарах, ювелирных изделиях, мобильных телефонах, лёгких сплавах и т.
 д.
д. - Титан является физиологически инертным[2], благодаря чему применяется в медицине (протезы, остеопротезы, зубные имплантаты), в стоматологических и эндодонтических инструментах, украшениях для пирсинга.
- Титановое литьё выполняют в вакуумных печах в графитовые формы. Также используется вакуумное литьё по выплавляемым моделям. Из-за технологических трудностей в художественном литье используется ограниченно. Первой в мировой практике монументальной литой скульптурой из титана является памятник Юрию Гагарину на площади его имени в Москве[15].
- Титан является легирующей добавкой во многих легированных сталях и большинстве спецсплавов[каких?].
- Нитинол (никель-титан) — сплав, обладающий памятью формы, применяемый в медицине и технике.
- Алюминиды титана являются очень стойкими к окислению и жаропрочными, что, в свою очередь, определило их использование в авиации и автомобилестроении в качестве конструкционных материалов.

- Титан является одним из наиболее распространённых геттерных материалов, используемых в высоковакуумных насосах.
Существует множество титановых сплавов с различными металлами. Легирующие элементы разделяют на три группы, в зависимости от их влияния на температуру полиморфного превращения: на бета-стабилизаторы, альфа-стабилизаторы и нейтральные упрочнители. Первые понижают температуру превращения, вторые повышают, третьи не влияют на неё, но приводят к растворному упрочнению матрицы. Примеры альфа-стабилизаторов: алюминий, кислород, углерод, азот. Бета-стабилизаторы: молибден, ванадий, железо, хром, никель. Нейтральные упрочнители: цирконий, олово, кремний. Бета-стабилизаторы, в свою очередь, делятся на бета-изоморфные и бета-эвтектоидообразующие.
Самым распространённым титановым сплавом является сплав Ti-6Al-4V (англ.)русск. (в российской классификации — ВТ6), содержащий около 6 % алюминия и около 4 % ванадия. По соотношению кристаллических фаз он классифицируется как (α+β)-сплав.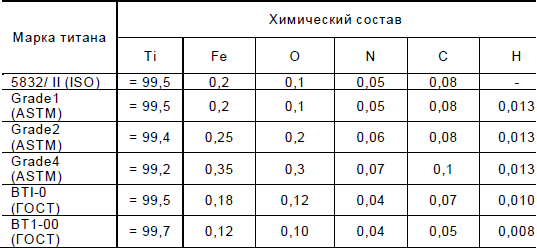 На его производство идёт до 50 % добываемого титана[3].
На его производство идёт до 50 % добываемого титана[3].
Ферротитан (сплав титана с железом, содержащий 18—25 % титана) используют в чёрной металлургии для раскисления стали и удаления растворённых в ней нежелательных примесей (сера, азот, кислород)[3].
В 1980-х годах около 60-65 % добываемого в мире титана использовалось в строительстве летательных аппаратов и ракет, 15 % — в химическом машиностроении, 10 % — в энергетике, 8 % — в строительстве судов и для опреснителей воды[3].
В виде соединений
- Белый диоксид титана (TiO2) используется в красках (например, титановые белила), а также при производстве бумаги и пластика. Пищевая добавка E171.
- Титанорганические соединения (например, тетрабутоксититан) применяются в качестве катализатора и отвердителя в химической и лакокрасочной промышленности.
- Неорганические соединения титана применяются в химической электронной, стекловолоконной промышленности в качестве добавки или покрытий.

- Карбид титана, диборид титана, карбонитрид титана — важные компоненты сверхтвёрдых материалов для обработки металлов.
- Нитрид титана применяется для покрытия инструментов, куполов церквей и при производстве бижутерии, так как имеет цвет, похожий на золото.
- Титанат бария BaTiO3, титанат свинца PbTiO3 и ряд других титанатов — сегнетоэлектрики.
- Тетрахлорид титана используется для иридизации стекла и для создания дымовых завес[2].
Анализ рынков потребления
В 2005 компания Titanium Corporation опубликовала следующую оценку потребления титана в мире:
- 60 % — краска;
- 20 % — пластик;
- 13 % — бумага;
- 7 % — машиностроение.
Цены
Цена титана составляет $5,9-6,0 за килограмм, в зависимости от чистоты[16].
Чистота и марка чернового титана (титановой губки) обычно определяется по его твёрдости, которая зависит от содержания примесей.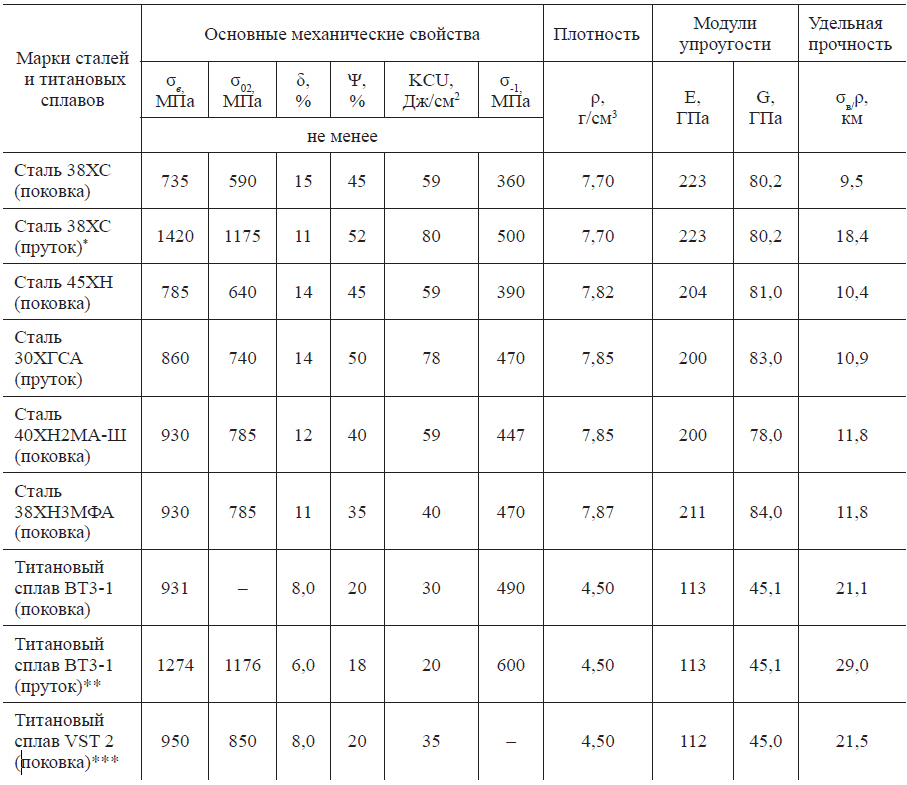
Физиологическое действие
Титан считается физиологически инертным, благодаря чему применяется в протезировании как металл, непосредственно контактирующий с тканями организма. Однако титановая пыль может быть канцерогенной[2]. Как было сказано выше, титан применяется также в стоматологии. Отличительная черта применения титана заключается не только в прочности, но и способности самого металла сращиваться с костью, что даёт возможность обеспечить квазимонолитность основы зуба.
Примечания
- ↑ 1 2 Meija J. et al. Atomic weights of the elements 2013 (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. — 2016. — Vol. 88, no. 3. — P. 265—291. — doi:10.1515/pac-2015-0305.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 CRC Handbook of Chemistry and Physics / D.
 R. Lide (Ed.). — 90th edition. — CRC Press; Taylor and Francis, 2009. — 2828 p. — ISBN 1420090844.
R. Lide (Ed.). — 90th edition. — CRC Press; Taylor and Francis, 2009. — 2828 p. — ISBN 1420090844. - ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 Раков И. Э. Титан // Химическая энциклопедия : в 5 т. / Гл. ред. Н. С. Зефиров. — М.: Большая Российская энциклопедия, 1995. — Т. 4: Полимерные—Трипсин. — С. 590—592. — 639 с. — 40 000 экз. — ISBN 5-85270-039-8.
- ↑ Таблица Менделеева на сайте ИЮПАК.
- ↑ Riley J.P., Skirrow G. Chemical Oceanography V. 1, 1965.
- ↑ Месторождение титана.
- ↑ Месторождение титана.
- ↑ Ильменит, рутил, титаномагнетит — 2006 г.
 (неопр.) (недоступная ссылка). Дата обращения: 17 ноября 2007. Архивировано 28 декабря 2007 года.
(неопр.) (недоступная ссылка). Дата обращения: 17 ноября 2007. Архивировано 28 декабря 2007 года. - ↑ Титан (неопр.). Информационно-аналитический центр «Минерал». Дата обращения: 19 ноября 2010.
- ↑ Корпорация ВСМПО-АВИСМА
- ↑ 1 2 3 4 5 6 7 8 9 10 Бердоносов С. С. Титан // Физическая энциклопедия : [в 5 т.] / Гл. ред. А. М. Прохоров. — М.: Большая российская энциклопедия, 1994. — Т. 4: Пойнтинга — Робертсона — Стримеры. — С. 116. — 704 с. — 40 000 экз. — ISBN 5-85270-087-8.
- ↑ Стрельченко С. С., Лебедев В. В. Соединения A3B5: Справочник. М.: Металлургия, 1984. 144 с.
- ↑ Свойства элементов: В 2 ч.
 Ч. 1. Физические свойства: Справочник/ Под ред. Г. В. Самсонова. М.: Металлургия, 1976. 600 с.
Ч. 1. Физические свойства: Справочник/ Под ред. Г. В. Самсонова. М.: Металлургия, 1976. 600 с. - ↑ Влияние воды на процесс пассивации титана — 26 Февраля 2015 — Химия и химическая технология в жизни (неопр.) (недоступная ссылка). www.chemfive.ru. Дата обращения: 21 октября 2015. Архивировано 14 августа 2016 года.
- ↑ Искусство литья в XX веке
- ↑ На мировом рынке титана за последние два месяца цены стабилизировались (обзор)
Ссылки
Титан и его сплавы — Студопедия
Важнейшее преимущество титана и титановых сплавов перед другими конструкционными материалами – это высокая удельная прочность и жаропрочность в сочетании с хорошей коррозионной стойкостью, практическое отсутствие хладноломкости наряду с высокой удельной прочностью. Кроме того, титан и его сплавы, несмотря на плохую обрабатываемость резанием, хорошо свариваются, обрабатываются давлением в холодном и горячем состоянии, термически упрочняются, что имеет важное значение для их применения в ряде отраслей техники. Это относится в первую очередь к авиа-, ракето- и судостроению, химическому, пищевому и транспортному машиностроению.
Это относится в первую очередь к авиа-, ракето- и судостроению, химическому, пищевому и транспортному машиностроению.
Титан – металл серебристо-белого цвета с плотностью ρ = 4,505 г/см3 и температурой плавления 1672 °С. Титан может находиться в двух полиморфических модификациях: Tiα до 882 ºС с гексагональной плотноупакованной решеткой и высокотемпературной Tiβ выше этой температуры с объёмноцентрированной кубической решеткой до температуры плавления. Имеет высокие механические свойства σВ = 300 МПа, δ = 40 %, не имеет температурного порога хладноломкости, парамагнитен. Титан легкий, прочный, тугоплавкий, коррозионностойкий за счет возникновения оксидной пленки TiO2.
Механические свойства титана определяются составом: чем в нем меньше примесей, тем ниже прочность и выше пластичность (рис. 15.1). Характерная особенность титана – необычайно высокая чувствительность к примесям атмосферных газов: кислороду, азоту, водороду и углероду, которые образуют с титаном твердые растворы внедрения и промежуточные фазы: оксиды, нитриды, гидриды, карбиды, повышая его характеристики прочности и снижая пластичность.
Рис. 15.1. Влияние примеси кислорода на механические свойства титана
Кроме того, ухудшается обработка давлением, свариваемость и коррозионная стойкость. Поэтому содержание этих примесей ограничивается сотыми и тысячными долями процента.
Полиморфизм титана, хорошая сплавляемость с другими металлами дает широкие возможности получения сплавов на основе титана с самыми разными механическими свойствами благодаря легированию, термической обработке, деформационному упрочнению.
Элементы, легирующие титан, подразделяются на:
· повышающие температуру полиморфного превращения и расширяющие область существования α-модификации: Al, Ga, La, C, O, N;
· понижающие температуру полиморфного превращения и расширяющие область существования β-модификации: Mo, V, Nb, Ta, Hf, W, Cr, Mn, Fe, Co и другие.
Алюминий является основным легирующим элементом для титана и содержится почти во всех промышленных сплавах. Он повышает удельную прочность сплава, жаропрочность, модуль упругости, уменьшает склонность к водородной хрупкости. Из-за уменьшения технологической пластичности содержание Al ограничивается 7 %.
Из-за уменьшения технологической пластичности содержание Al ограничивается 7 %.
Для повышения рабочих характеристик жаропрочных сплавов с высоким содержанием алюминия главным образом используют добавки ванадия, молибдена и вольфрама.
Цирконий повышает термическую стабильность, увеличивает предел ползучести, прочность при низких и средних температурах, уменьшает склонность к хладноломкости и улучшает свариваемость.
Рис. 15.2. Твердость сплавов титана с различным содержанием хрома после отжига
при температуре 600 ºС (1) и охлаждения из β-области с различными скоростями:
резкая закалка в растворе щелочи (2), закалка в воде (3), охлаждение на воздухе (4)
Хром считается одной из наиболее перспективных легирующих добавок к титану наряду с молибденом. Сплавы титана с хромом отличаются превосходным сочетанием прочности и пластичности (рис. 15.2).
Ниобий повышает стабильность поверхности, увеличивает жаростойкость при высоких температурах.
В связи с определенным характером действия на титан различных легирующих элементов промышленные сплавы по типу структуры могут быть подразделены на три группы: титановые сплавы на основе
Tiα, сплавы на основе Tiβ и двухфазные (α+β)-титановые сплавы.
Промышленные титановые сплавы с (α+β)-структурой целесообразно подразделить на три группы: псевдо-α-сплавы с небольшим количеством β-фазы (Tiβ) со свойствами, близкими к α-сплавам (Tiα), типичные (α+β)-сплавы и псевдо-β-сплавы. Псевдо-β-сплавы представляют собой сплавы на основе Tiβ. В отожженном состоянии их физико-механические и технологические свойства типичны для β-сплавов, однако β-фаза у этих сплавов термически нестабильна.
По уровню характеристик прочности титановые сплавы классифицируют на высокопластичные и малопрочные, среднепрочные и высокопрочные, жаропрочные, коррозионностойкие.
По способности упрочняться с помощью термической обработки – на упрочняемые и не упрочняемые. По технологии производства – на деформируемые и литейные.
Деформируемые титановые сплавы с α-структурой характеризуются невысокой прочностью и не упрочняются при термической обработке. Они хорошо свариваются и имеют высокие механические свойства при криогенных температурах (ВТ5–1, ОТ4–0, ОТ4, ВТ20, ВТ18, ВТ–6, ВТ14, ВТ3–1, ВТ25 и др.).
Двухфазные (α+β)-сплавы характеризуются хорошим сочетанием механических и технологических свойств. По структуре после закалки в них образуется структура мартенситного типа. Увеличение количества β-фазы в сплавах переходного класса до 50 % обеспечивает им самую высокую прочность как в отожженном, так и в закалённом состояниях.
Однофазные β-сплавы имеют наиболее высокую коррозионную стойкость. Сплавы с β-структурой реже применяются в промышленности и их легируют ванадием, молибденом и ниобием.
Литейные титановые сплавы (ВТЛ1, ВТ14Л, ВТ5Л и др.) имеют небольшой температурный интервал кристаллизации, высокую жидкотекучесть и хорошую плотность отливки. Титановые сплавы этой категории склонны к поглощению газов, поэтому разливку надо проводить в вакууме или в среде нейтральных газов. Для получения отливок используют чугунные или стальные формы, а также оболочковые и керамические формы.
Для фасонного литья применяют сплавы, близкие по химическому составу некоторым деформируемым сплавам (ВТ5Л, ВТ14Л), а также специальные литейные сплавы.
Деление конструкционных титановых сплавов по типу структуры и характеристик прочности, их химический состав приведены в таблице15.1.
Таблица 15.1
Классификация промышленных титановых сплавов
и их механические свойства
| Тип сплава | Марка сплава | Средний химический состав, % | Уровень прочности | Механич. свойства | Технология получения | |
| σВ, МПа | δ, % | |||||
| α-сплавы | ВТ1–0 | 99,28 % Ti | М.п.* | 350–500 | деформируемый | |
| ВТ5 | 5 % А1 | С.п. | 750–900 | |||
| ВТ5–1 | 5 % А1; 2,5 % Sn | С.п. | 750–900 | |||
| ВТ5Л | 5 % А1 | М.п. | 700–900 | литейный | ||
| Псевдо-α-сплавы | ОТ4–1 | 1,5 % А1; 1 % Мn | М.п.. | 600–750 | деформируемый | |
| АТ–2 | 2 % Zr; 1 % Мо | М.п. | 600–750 | |||
| ВТ20 | 6 % А1; 1 % Мо; 1 %V | С.п. | 950–1150 | |||
| ТС5 | 5 % А1; 2 % Zr; 3 %Sn; 2 % V | В.п. | 950–110 | |||
| ВТ20Л | 6 % А1; 2 % Zr; 1 % Мо | С.п. | ≥1000 | ≤4 | литейный | |
| (α+β)-сплавы | ВТ6С | 5 % А1; 4 % V | С.п. | 850–1000 | деформируемый | |
| ВТЗ–1 | 6 % А1; 2,5 % Мо; 2 % Сr; 0,3 % Si; 0,5 % Fe | В.п. | 1000–1200 | |||
| ВТ14 | 4,5 % А1; 3 % Мо; 1 % V | В.п. | 900–1070 | |||
| ВТ22 | 5 % А1; 5 % Мо; 5 % V; 1 % (Fе, Сr) | В.п. | 1100–1250 | |||
| ВТ14Л | 5 % А1; 3 % Мо; 1 % V; 0,5 % (Cr, Fe) | В.п. | литейный | |||
| Псевдо-β-сплавы | ВТ–15 | 3 %А1; 7 % Мо; 11 % Сr | В.п. | 1350–1500 | деформируемый | |
| ТС6 | 3 % А1; 5 % Мо; 6 %V–11 % Сr | В.п. | 1400–1500 | |||
| β-сплавы | 33 %Мо | С.п. | 800–850 | деформируемый, коррозионност. |
* – М.п. – малопрочные (высокопластичные), С.п. – среднепрочные,
В.п. – высокопрочные
Титановые сплавы подвергаются следующим видам термической обработки: отжигу для снятия напряжений, рекристаллизационному отжигу, упрочняющей термической и химико-термической обработке.
Упрочняющая термическая обработка (α+β)-сплавов состоит из закалки с температур нагрева до β- или (α+β)-области с последующим искусственным старением. После закалки образуется α’-фаза (мартенситная фаза) игольчатого строения, представляющая собой пересыщенный твердый раствор легирующих элементов в α-фазе. При старении из α’-фазы выделяется β-фаза, понижающая твердость сплава, или интерметаллидная фаза, вызывающая охрупчивание.
При закалке из β-области структура сплавов состоит из переохлажденного β’-твердого раствора. При старении из такого раствора выделяется мелкодисперсная α-фаза, повышающая прочность и твердость сплава.
Для повышения жаростойкости детали из титановых сплавов подвергают различным видам диффузионной металлизации, а для повышения износостойкости – азотированию.
Сплав титана и железа — Морской флот
Одним из наиболее важных направлений в современной черной металлургии является не наращивание объема производства материалов, как это было ранее, а повышение качества выпускаемой продукции при сравнительно невысоких темпах увеличения объема производства. То есть приоритетным является производство конструкционных материалов с меньшей металлоемкостью, но с высоким значением механических свойств, что достигается путем введения в сплав различных легирующих элементов. Нередко такие элементы вводятся в чистом виде, однако чаще в виде ферросплавов, представляющих собой сплавы железа с легирующими элементами. Одним из наиболее эффективных и распространенных ферросплавов является ферротитан.
Ферротитан – это легирующий сплав титана и железа, где минимальное содержание титана по массе – 20%, а максимальное – 75%. Ферротитан получаются путем переплава или восстановления. Стоит отметить, что сплав может иметь в своем составе алюминий, медь, кремний и некоторые примеси, но в небольших количествах. Ферротитан бывает нескольких марок, каждая из которых различна по наличию примесей: ФТи25, ФТи70С05, ФТи30, ФТи70С08, ФТи70С1, ФТи70С05Сн03, ФТи57С7 и ФТи35С8.
Ферротитан наиболее распространен в сталелитейной промышленности. Он используется для раскислений и легирования сталей. Благодаря тем свойствам, которыми сплав обладает, продукция становится очень устойчивой к коррозии, поэтому нередко ферротитан применяется для производства нержавеющей стали.
Кроме того, сплав применяется при выплавке наиболее ответственных конструкционных сталей с целью конечного раскисления и дегазации. Применяется ферротитани для изготовления сварочных электродов.
Ферротитан входит в группу ферросплавов, которые используются для легирования и раскисления стали. Ферротитан содержит до 35 или более 60 % титана, 1-7 % аллюминия, 1-4,5 % кремния, до 3 % меди, остальное составляет железо и его примеси.
Ферротитан используется в широком производстве для стали легирования, ее дегазации и раскисления. Стали, которые содержат ферротитан, отличаются повышенными механическими свойствами. Ферротитан связывает углерод в карбид титана. За счет этого и проявления своих свойств в жароупорных и нержавеющих сталях, улучшается свариваемость стали и ее сопротивляемость коррозии.
Ферротитан может содержать от 20 до 75% титана. В состав сплава входит железо, за счет которого снижается температура плавления и облегчается усвоение более тугоплавкого титана.
Ферротитан – это промежуточный сплав. Он используется при производстве нержавеющей стали. При добавлении в сталь ферротитана она начинает приобретать особые свойства и становится устойчивой к коррозии. При легировании тонны стали необходим совсем небольшой расход титана около 0,5-2%.
Получают ферротитан двумя способами. Первый – внепечной алюминотермический способ – это плавление ильменитового концентрата и титановых отходов. В этом случае получается низкопроцентный ферротитан. Второй способ – это сплавление в электрической печи железных и титановых отходов, получается высокопроцентный ферротитан.
Ферротитан — это ферросплав, основным компонентом которого является титан. Другие химические элементы — алюминий, кремний, углерод, фосфор, сера, медь, вольфрам, молибден, олово, а для марки ФТи70С08 также марганец и хром, присутствуют в ферротитане в небольших концентрациях, предельное значение которых для каждой из марок материала определяются требованиями ГОСТ 4761-91.
Согласно предусмотренному государственным стандартом сортаменту, выделяют шесть основных марок ферротитана, содержание титана в которых может изменяться в пределах от 28 до 75%. Существует также деление на фракции в зависимости от величины частиц ферротитана. Минимальный размер — до 3,2мм, максимальный размер — 50-200мм. Поставка ферротитана потребителям может осуществляться в кусках, вес которых не превышает 15 килограммов.
Применяется ферротитан в металлургической промышленности в качестве присадки для дегазации и раскисления стали, в качестве легирующего элемента. Титан способен связывать углерод в карбид титана, что увеличивает коррозионную устойчивость и свариваемость сталей. Используют ферротитан и для изготовления сварочных электродов, а также в производстве жаропрочных и нержавеющих сталей. Обработанные титаном стали приобретают улучшенные механические характеристики.
Ферротитан – сплав титана с железом, используемый в качестве добавки при производстве стали. Екатеринбург не испытывает сегодня дефицита в поставщиках ферротитана. Чьей продукции стоит отдать предпочтение? Что необходимо учесть при выборе поставщика?
Благодаря стремительному развитию металлургического производства, современная сталелитейная промышленность выпускает всё более совершенные виды продукции. Для лучшего «усвоения полезных добавок» стальным расплавом в современной металлургии практикуется применение ферросплавов.
Сплав ферротитан имеет следующий состав: Титан – до 40 или более 65%; Алюминий – 1–7%; Кремний – 1–4,5%; Медь – до 3%; Железо и примеси – остальная часть.
Алюминий, кремний и медь в составе – нежелательные, но неизбежные компоненты. Сплав, содержащий 20-40% титана, получают из ильменитового концентрата алюминотермическим способом. Алюминий здесь служит восстановителем железа и титана из оксидов обогащённой титаномагнетитовой руды. Ферротитан с содержанием Ti 65-78% вырабатывают путём сплавления в индукционных печах титановой губки или титановых отходов со стальным ломом.
Цели использования ферротитана
Ферротитан применяется в металлургии для раскисления и легирования сталей, а также в производстве сварочных электродов и деталей с особыми требованиями к качеству.
Задействование титана в процессе производства нержавеющих и жароупорных сталей позволяет получить титановый карбид, в котором улучшающие свойства углерода проявляются наиболее полно. В результате значительно возрастает показатель свариваемости и сопротивляемости коррозии сплавов.
Титан – весьма тугоплавкий металл, поэтому добавление его в стальную ванну в чистом виде требует высоких затрат энергии и большого расхода шихтовых материалов.
Применение промежуточного сплава – ферротитана – в получении легированных сталей даёт значительные преимущества:
Сокращение времени выплавки. Снижение энергоёмкости процесса. Экономия материалов, задействованных в производстве. Повышение качества конечной продукции.
Ферротитан – сплав, состоящий из титана (20-78%), железа и незначительного количества примесей. Сплав, содержащий 20-40% Ti выплавляют в основном алюминотермическим процессом, восстанавливая алюминием основные составляющие сплава – титан и железо – из оксидов концентрата титаномагнетитовых руд (ильменитового концентрата). Такие сплавы содержат в соответствии с отечественными стандартами 20-40% Ti,
Полученные в промышленных условиях слитки титана называют техническим титаном. Он
Составы титановых сплавов — Большая Химическая Энциклопедия
R-фаза, которая служит промежуточной фазой для облегчения превращения мартенсита в аустенит. Сообщается, что образование R-фазы происходит из-за наличия дислокаций и выделений [11]. Ожидается, что в никель-титановых эндодонтических инструментах и ортодонтических проволоках vwought значительная плотность дислокаций, которые подвергаются значительной механической деформации в процессе производства [12], микроструктурные выделения являются следствием неизбежного отклонения состава никель-титанового сплава от эквиатомный состав NiTi [13,14] ,… [Стр.632]Восстанавливающие кислоты. Коррозионная стойкость титановых сплавов в восстанавливающей добавляемой среде очень чувствительна к концентрации добавляемой жидкости, температуре, химическому составу заднего прохода и плотности добавляемого раствора, помимо состава титанового сплава. Когда температура или концентрация чистых (незагрязненных) восстанавливающих добавочных растворов превышает определенные значения, защитная оксидная пленка титана может разрушиться, что приведет к серьезной общей коррозии. В эту категорию входят соляная, серная, водородная, водородная, фтористоводородная, фосфорная, сульфаминовая, щавелевая и трихлоруксусная кислоты.Поскольку эффективность титановых сплавов в восстановлении … [Pg.687]
H. Hucek, M. Wahl, Справочник по международным составам и обозначениям сплавов, 1990 г., Vol. 1, Titanium, MCIC HB-09, Информационный центр по металлам и керамике, BatteUe Columbus Laboratories, Колумбус, штат Огайо, 1990. [Стр. 27]
Системы из титановых сплавов были тщательно изучены. Одна компания оценила более 3000 композиций за восемь лет (работа Rem-Cm спонсировалась в BatteUe Memorial Institute). Разработка AHoy была нацелена на аэрокосмические приложения при повышенных температурах, прочность для конструктивных приложений, биосовместимость и коррозионную стойкость.Первоначально в аэрокосмической отрасли предпринимались попытки заменить сплавы на основе никеля и кобальта в диапазоне 250–600 ° C. Температурный предел полезной прочности и коррозионной стойкости составляет около 550 ° C. [Стр.100]
Титан, легированный ниобием, демонстрирует сверхпроводимость и отсутствие электрического сопротивления ниже 10 К. Состав составляет от 25 до 50 мас.% Ti. Эти сплавы представляют собой сплавы с P-фазой, имеющие температуры перехода в сверхпроводящее состояние около 10 К. Их использование представляет интерес для производства электроэнергии, силовых установок, исследований термоядерного синтеза и электронных устройств (52).[Стр.108]
Алюминиевая бурильная труба обычно изготавливается из медно-алюминиевого сплава типа 2014 года. Состав этого сплава составляет от 0,50 до 1,20% кремния, максимум 1,00% железа, от 3,90 до 5,0% меди, от 0,40 до 1,20% марганца, максимум 0,25% цинка и 0,05% титана. Сплав подвергается термообработке до условий T6, которые представляют собой предел прочности на разрыв 64 тыс. Фунтов на квадратный дюйм, предел текучести 58 тыс. Фунтов на квадратный дюйм, удлинение на 7% и Hbn 135. Алюминиевая бурильная труба обычно поставляется со стальными замками, которые навинчиваются для обеспечения максимальной прочности, которая не может быть достигнута с помощью алюминиевые соединения.[Pg.1258]
Фиг. 32 представляет собой график, показывающий состав сплавов, нанесенных на медные подложки, в зависимости от концентрации Ti2 + и плотности тока в AICI3-NaCl с концентрацией 66,7 м / o [177]. Сплавы были осаждены в диапазоне силы тока плотности для нескольких концентраций Ti2 +. При низких концентрациях Ti2 + состав сплава зависит от приложенной плотности тока. Сплав с концентрацией титана 25 а / о осаждается только при низких плотностях тока. По мере увеличения плотности тока парциальная плотность тока Ti ограничивается диффузией Ti2 +, и содержание Ti в сплаве падает.При концентрации Ti2 + 150 ммоль л 1. плотность тока … [Pg.331]
Состав товарных сплавов, номенклатура. Простой и общий способ идентификации коммерческого сплава (или группы аналогичных сплавов) заключается в этикетке, на которой указано (в виде округленных значений) массовое содержание основных компонентов в процентах, указанное их химическими символами. Сплав, например Ti-6A1-4V, представляет собой сплав на основе титана, обычно содержащий 6 мас.% Алюминия и 4 мас.% Ванадия. [Pg.321]
Исследователи пытались изготовить пластины, используя множество различных металлов — в основном нержавеющую сталь, алюминиевые сплавы, титановые сплавы, никелевые сплавы, медные сплавы, интерметаллические сплавы и композиты на металлической основе, такие как алюминий, армированный углеродным волокном. сплавы, медные сплавы, армированные углеродным волокном и т. д.[26]. Хотя металлы Ta, Hf, Nb, Zr и Ti демонстрируют хорошую коррозионную стойкость и химическую стабильность [6], стоимость этих металлов слишком высока для их использования в качестве материалов для металлических пластин. Вот почему относительно более дешевые сплавы на основе железа, особенно нержавеющая сталь, широко изучаются в качестве материала пластин. В следующих разделах мы представим безболезненные пластины из нержавеющей стали (SS) и SS, которые были тщательно исследованы и покажут многообещающие результаты для окончательного применения [6,11]. [Pg.326]
Ян Дж.М., Дженг, С. и Ян, С.Дж. (1991). Механизмы разрушения композитов Matrbi из титанового сплава, армированного волокном. Часть I. Межфазное поведение. Mater. Sci. Англ. AI38, 155–167. [Стр.92]
Металлы, такие как алюминий, сталь и титан, являются основными адгезивами, используемыми для адгезионных структур. Однако они никогда не приклеиваются непосредственно к полимерному клею. Защитный оксид, встречающийся в природе или созданный на поверхности металла путем химического травления или анодирования, предназначен для защиты от коррозии.Полученный оксид имеет морфологию, отличную от основной массы, и химию поверхности, зависящую от условий, используемых для образования оксида 39). Исследования различных составов алюминиевых сплавов показывают, что хотя состав оксида не зависит от объемного состава, поверхность оксида содержит химические частицы, которые характерны для основного сплава и ванны для анодирования 50 (42). [Стр.10]
Сплавс памятью. В поисках способа уменьшить хрупкость титана исследователи ВМС США по счастливой случайности обнаружили никель-титановый сплав, обладающий удивительной памятью.Предварительно охлажденные зажимы из сплава (нитинола) являются гибкими и легко устанавливаются на место. При нагревании до заданной температуры металлическая деталь из сплава оказывает огромное давление. Использование обычных зажимов для удержания пучков проводов или кабелей в конструкции корабля или самолета требует специальных инструментов. Для этого и других применений в промышленности и медицине востребован нитинол. Однако сплав непросто произвести, потому что только незначительные изменения в составе могут повлиять на температуру возврата на несколько градусов.[Pg.1072]
Металлы и керамика (глиноподобные материалы) также используются в качестве матриц в современных композитах. В большинстве случаев композиты с металлической матрицей состоят из алюминия, магния, меди или титановых сплавов этих металлов или интерметаллических соединений, таких как TiAl и NiAl. Армирование обычно представляет собой керамический материал, такой как карбид бора (B4C), карбид кремния (SiC), оксид алюминия (A1203), нитрид алюминия (AlN) или нитрид бора (BN). Металлы также использовались в качестве усиления металлических матриц.Например, физические характеристики некоторых типов стали были улучшены за счет добавления алюминиевых волокон. Армирование обычно добавляют в виде частиц, нитевидных кристаллов, пластин или волокон. [Стр.31]
Состав сплава, межузельный кислород, азот и углерод в титане SCC сплавов a и ot-fi Растворы галогенидов в метаноле Горячая соль SCC … [Pg.258]
HDPE, композитные материалы, такие как эпоксидные смолы. стекловолокно и эпоксидно-углеродное волокно, а также ламинатные конструкции, такие как полимерные пленки на объемных металлических подложках.Тонкопроводящие пленочные нагреватели изготавливались из электропроводящих красок, электропроводящих полимерных пленок, металлической фольги (нержавеющая сталь, медь, титан и титановые сплавы) и тонких металлических пленок, напыленных на керамику или стекло. Размеры образцов варьировались от нескольких сантиметров до 5 м. [Стр.54]
Рабочая температура обычных титановых сплавов ограничена 300-500 ° C. Известные композиты на основе Ti обладают высокой прочностью при … [Pg.235]
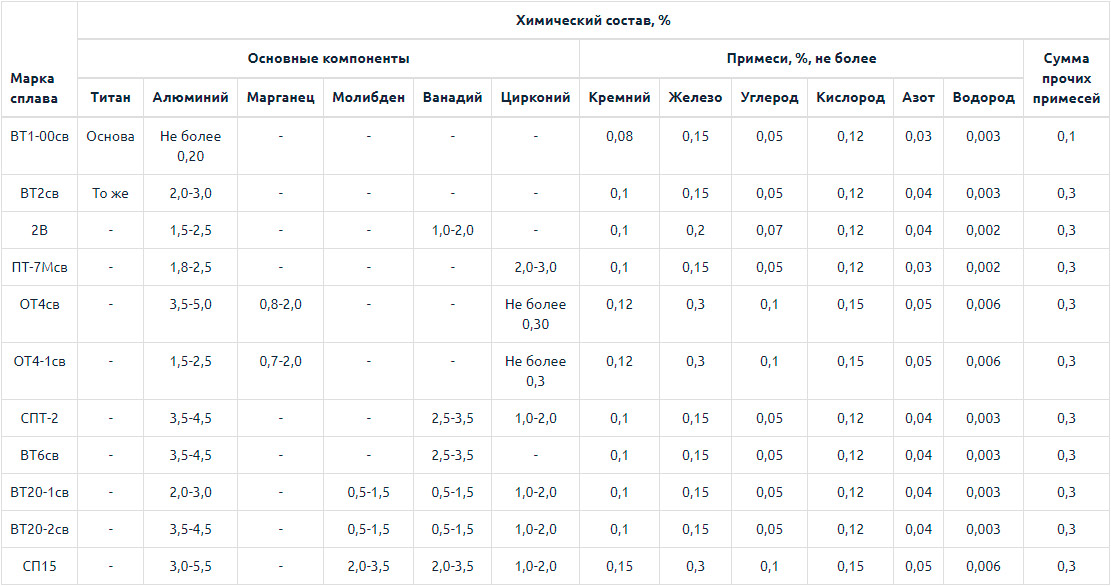
Марки титана, химический состав титана
| Качество титана Титан 1-4 степени является чистым титаном, остальные марки — сплавами.Чистый титан используется из-за его высокой коррозионной стойкости, сплавы из-за чрезвычайно высокого отношения прочности к весу.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Лучший состав стального сплава — отличные предложения по составу стального сплава от мировых продавцов состава стального сплава
Отличные новости !!! Вы выбрали правильный состав стального сплава.К настоящему времени вы уже знаете, что что бы вы ни искали, вы обязательно найдете это на AliExpress. У нас буквально тысячи отличных продуктов во всех товарных категориях. Ищете ли вы товары высокого класса или дешевые и недорогие оптовые закупки, мы гарантируем, что он есть на AliExpress.
Вы найдете официальные магазины торговых марок наряду с небольшими независимыми продавцами со скидками, каждый из которых предлагает быструю доставку и надежные, а также удобные и безопасные способы оплаты, независимо от того, сколько вы решите потратить.
AliExpress никогда не уступит по выбору, качеству и цене. Каждый день вы найдете новые онлайн-предложения, скидки в магазинах и возможность сэкономить еще больше, собирая купоны. Но вам, возможно, придется действовать быстро, поскольку этот состав из лучших стальных сплавов в кратчайшие сроки станет одним из самых востребованных бестселлеров. Подумайте, как вам будут завидовать друзья, когда вы скажете им, что получили свой стальной сплав на AliExpress.Благодаря самым низким ценам в Интернете, дешевым тарифам на доставку и возможности получения на месте вы можете еще больше сэкономить.
Если вы все еще не уверены в составе стального сплава и думаете о выборе аналогичного товара, AliExpress — отличное место для сравнения цен и продавцов. Мы поможем вам решить, стоит ли доплачивать за высококачественную версию или вы получаете столь же выгодную сделку, приобретая более дешевую вещь.А если вы просто хотите побаловать себя и потратиться на самую дорогую версию, AliExpress всегда позаботится о том, чтобы вы могли получить лучшую цену за свои деньги, даже сообщая вам, когда вам будет лучше дождаться начала рекламной акции. и ожидаемая экономия.AliExpress гордится тем, что у вас всегда есть осознанный выбор при покупке в одном из сотен магазинов и продавцов на нашей платформе. Реальные покупатели оценивают качество обслуживания, цену и качество каждого магазина и продавца.Кроме того, вы можете узнать рейтинги магазина или отдельных продавцов, а также сравнить цены, доставку и скидки на один и тот же продукт, прочитав комментарии и отзывы, оставленные пользователями. Каждая покупка имеет звездный рейтинг и часто имеет комментарии, оставленные предыдущими клиентами, описывающими их опыт транзакций, поэтому вы можете покупать с уверенностью каждый раз. Короче говоря, вам не нужно верить нам на слово — просто слушайте миллионы наших довольных клиентов.
А если вы новичок на AliExpress, мы откроем вам секрет.Непосредственно перед тем, как вы нажмете «купить сейчас» в процессе транзакции, найдите время, чтобы проверить купоны — и вы сэкономите еще больше. Вы можете найти купоны магазина, купоны AliExpress или собирать купоны каждый день, играя в игры в приложении AliExpress. Вместе с бесплатной доставкой, которую предлагают большинство продавцов на нашем сайте, вы сможете приобрести композицию из стали по самой выгодной цене.
У нас всегда есть новейшие технологии, новейшие тенденции и самые обсуждаемые лейблы.На AliExpress отличное качество, цена и сервис всегда в стандартной комплектации.


 д.
д.
 R. Lide (Ed.). — 90th edition. — CRC Press; Taylor and Francis, 2009. — 2828 p. — ISBN 1420090844.
R. Lide (Ed.). — 90th edition. — CRC Press; Taylor and Francis, 2009. — 2828 p. — ISBN 1420090844. (неопр.) (недоступная ссылка). Дата обращения: 17 ноября 2007. Архивировано 28 декабря 2007 года.
(неопр.) (недоступная ссылка). Дата обращения: 17 ноября 2007. Архивировано 28 декабря 2007 года. Ч. 1. Физические свойства: Справочник/ Под ред. Г. В. Самсонова. М.: Металлургия, 1976. 600 с.
Ч. 1. Физические свойства: Справочник/ Под ред. Г. В. Самсонова. М.: Металлургия, 1976. 600 с.