Температура плавления золота и другие характеристики
Золото — драгоценный металл, который до сих пор не утратил актуальности. А все из-за того, что золото, помимо внешней красоты, обладает уникальными физическими и химическими свойствами. С точки зрения химии, золото не вступает в реакцию практически ни с одним веществом. А физические свойства, например, ковкость, сопротивляемость, температура плавления золота также дают возможность использовать этот металл практически для любых потребностей. Но промышленность не использует золото из-за высокой стоимости и относительно маленького количества в природе, поэтому большинство свойств метала так и остаются невостребованными.
Итак, физические свойства золота оцениваются по таким критериям:
- ковкость;
- пластичность;
- твердость;
- электропроводимость, сопротивляемость;
- температура плавления.
И по всем вышеназванным категориям золото в качестве металла имеет отличные показатели.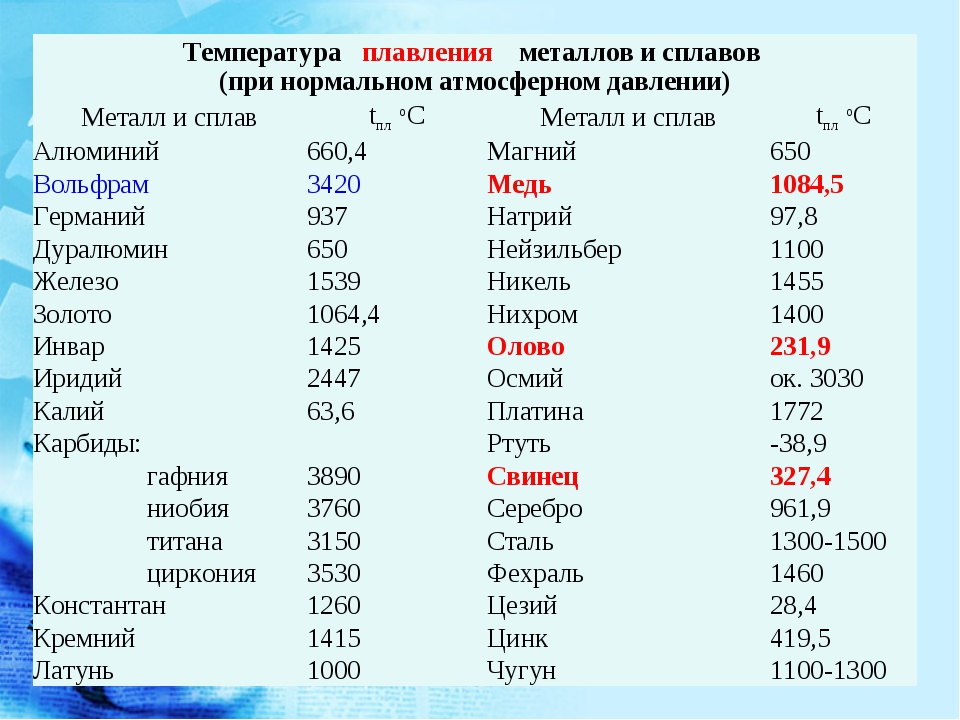
Температура плавления интересует не только ювелиров, но и любителей экспериментов и домашней плавки золота. Ведь переплавлять драгметалл, совершать аффинаж, то есть очистку и повышение пробы, можно и дома. Но для этого необходимо знать температуру плавления металла.
Чистый металл относится к группе среднеплавких — это значит, что показатель находится в промежутке от 770 до 1603 градусов Цельсия. Самая низкая температура плавления — 770 градусов Цельсия. Она характерна для сплава золота 375 пробы, то есть чистого драгметалла в нем всего 37,5 процентов. Чистое золото плавится при температуре 1063 градуса Цельсия. Показатель довольно высокий, но его можно добиться с помощью специальных печей, в которых и происходит процесс. Плавление происходит потому, что атомы золота освобождаются от кристаллических связей в решетке на уровне молекул, и вследствие распада кристаллитов образуется металл жидкой консистенции.
Показатель довольно высокий, но его можно добиться с помощью специальных печей, в которых и происходит процесс. Плавление происходит потому, что атомы золота освобождаются от кристаллических связей в решетке на уровне молекул, и вследствие распада кристаллитов образуется металл жидкой консистенции.
Металлы, меняющие показатель температуры плавления
Конечно, этот показатель можно изменить — как снизить, так и повысить. Делается это с помощью добавления лигатуры в сплав. Лигатура — это дополнительные металлы, которые добавляют в украшение, чтоб сделать его более прочным. В качестве лигатуры чаще всего используют:
- Серебро. Этот драгметалл понижает температуру плавления чистого золота. А также придает изделию белизну, поэтому такой сплав называется белым золотом.
- Медь, никель, цинк — эти металлы являются более дешевыми. Медь придает сплаву красноватый оттенок. Чаще всего используется в лигатурах, изготавливается 585 или 583 проба.

- Платина. Самый благодарный металл, поскольку не только придает изделию серебристый оттенок, но еще и не портит остальных свойств, не вступает в реакцию ни с одним фактором внешней среды. И при этом платина облегчает работу ювелирам, поскольку она снижает показатель плавления драгметалла. Но у этого вещества есть один значительный минус — его стоимость. Стоимость платины еще выше, чем золота, поэтому не каждый может позволить себе такую лигатуру.
- Палладий. Еще одна дорогая лигатура в сплаве. К тому же палладий повышает температуру плавления. Его используют только из-за свойств полученного изделия, а также красивого бежевого оттенка.
Температура кипения золота еще выше — 2947 градусов Цельсия. Но ее обычно не используют в работе, поскольку в процессе плавления достаточно достижения положенной температуры, чтоб соединить или, наоборот, разъединить несколько сплавов.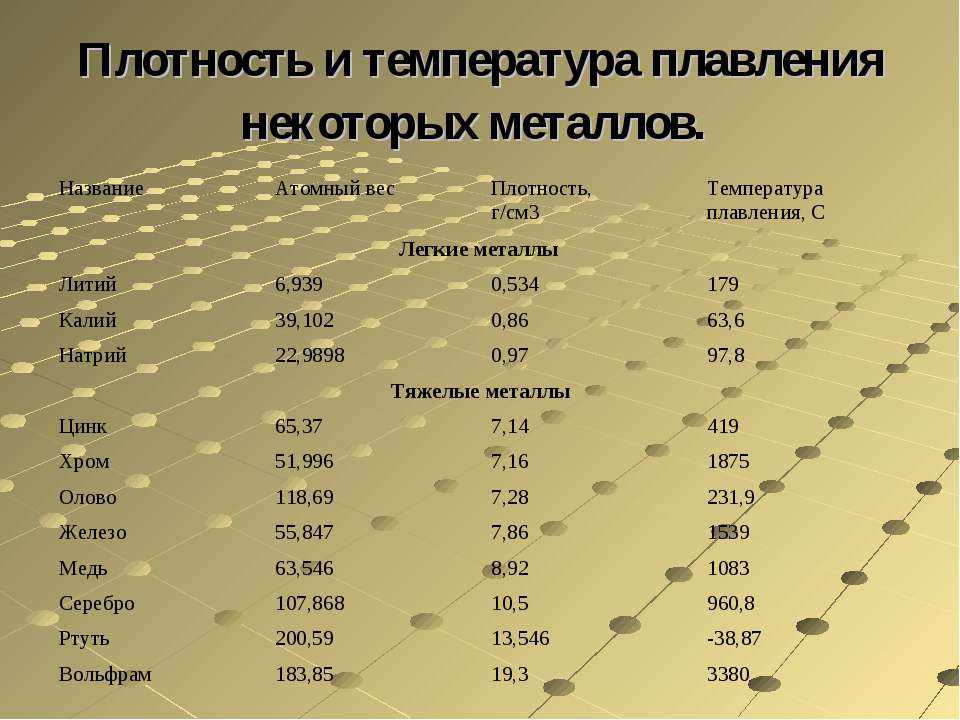
Плавление золота
Существует два основных способа плавки металла:
- Индивидуальный метод плавки золота. Он заключается в том, что ювелир на своем рабочем месте с помощью открытой горелки и чашки для плавки металлов расплавляет золото. Пламя должно быть достаточно сильным, а главная задача ювелира — следить за правилами техники безопасности. В таком виде драгметалл можно залить в формочки и изготовить слиток или же другие изделия.
- Централизованный тип плавления. Он заключается в том, что из нескольких сплавов разной пробы делается один сплав. Эта процедура проводится на заводах. И потом, после переплавки, определяется проба получившегося металла или же проходит дальнейшая очистка от примесей и повышение пробы. Для этого используют специальные высокочастотные или электрические печи в зависимости от объема золота для переплавки.
В домашних условиях необходимо помнить, что перед расплавкой металла нужна его очистка. Поэтому сначала стоит очистить золото от примесей. Это можно сделать, если разбавить его в царской водке или других реактивах, после этого требуется осадить металл. А уже после прохождения всех процедур можно приступить к плавке. Поэтому при какой температуре плавится золото нужно узнать заранее, поскольку для проведения процедуры также понадобится печка. А еще реактивы используют и на стадии плавления для ускорения процесса.
Поэтому сначала стоит очистить золото от примесей. Это можно сделать, если разбавить его в царской водке или других реактивах, после этого требуется осадить металл. А уже после прохождения всех процедур можно приступить к плавке. Поэтому при какой температуре плавится золото нужно узнать заранее, поскольку для проведения процедуры также понадобится печка. А еще реактивы используют и на стадии плавления для ускорения процесса.
Следует помнить, что плавка золота заканчивается на этапе, когда весь кусок металла расплавлен, а не только какая-то его часть. Дома осуществить это можно с 585 пробой или ниже, а вот с чистым золотом без специального оборудования будет сложно работать. При этом плавить металл лучше в отдельных помещениях или специальных лабораториях.
Иногда для переплавки можно использовать золото из старых устройств. В микросхемах раньше часто использовали низкопробное золото, потому что оно обладало хорошей проводимостью, низкой сопротивляемостью и долгим сроком службы.
Сейчас золото все реже используют в микросхемах. Но если разобрать старые телевизоры и другие устройства, можно насобирать небольшое количество золотых частиц. А чтоб их приняли в ломбард, необходимо сплавить эти частицы. Вот для такого процесса также понадобятся знания о температуре плавления, а также разные химические реактивы. Следует подбирать и термостойкую посуду для процесса плавки.
Температура плавления — один из важных показателей физических свойств золота. В первую очередь она интересует людей с практической точки зрения. Если знать все аспекты выполнения этой работы, можно без труда переплавить или сплавить золото даже дома. Также следует помнить о правилах безопасности во время процесса плавки.
При скольки градусах плавится свинец
Температура кипения и плавления металлов
В таблице представлена температура плавления металлов tпл, их температура кипения tк при атмосферном давлении, плотность металлов ρ при 25°С и теплопроводность λ при 27°С.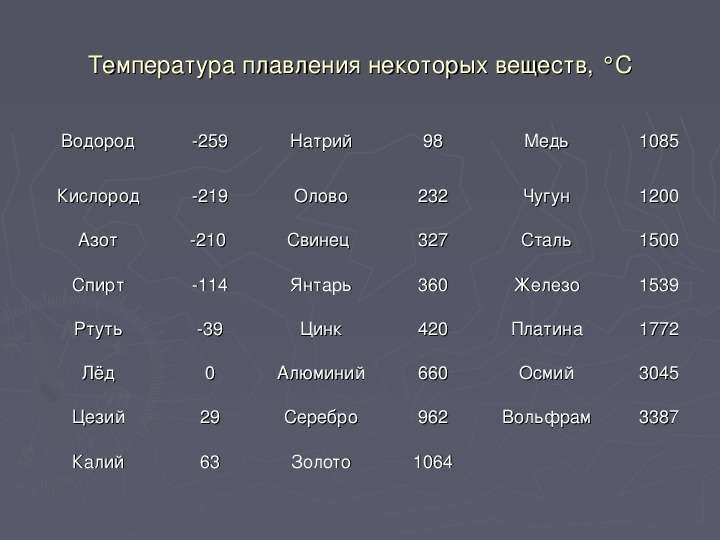
Температура плавления металлов, а также их плотность и теплопроводность приведены в таблице для следующих металлов: актиний Ac, серебро Ag, алюминий Al, золото Au, барий Ba, берилий Be, висмут Bi, кальций Ca, кадмий Cd, кобальт Co, хром Cr, цезий Cs, медь Cu, железо Fe, галлий Ga, гафний Hf, ртуть Hg, индий In, иридий Ir, калий K, литий Li, магний Mg, марганец Mn, молибден Mo, натрий Na, ниобий Nb, никель Ni, нептуний Np, осмий Os, протактиний Pa, свинец Pb, палладий Pd, полоний Po, платина Pt, плутоний Pu, радий Ra, рубидий Pb, рений Re, родий Rh, рутений Ru, сурьма Sb, олово Sn, стронций Sr, тантал Ta, технеций Tc, торий Th, титан Ti, таллий Tl, уран U, ванадий V, вольфрам W, цинк Zn, цирконий Zr.
По данным таблицы видно, что температура плавления металлов изменяется в широком диапазоне (от -38,83°С у ртути до 3422°С у вольфрама). Низкой положительной температурой плавления обладают такие металлы, как литий (18,05°С), цезий (28,44°С), рубидий (39,3°С) и другие щелочные металлы.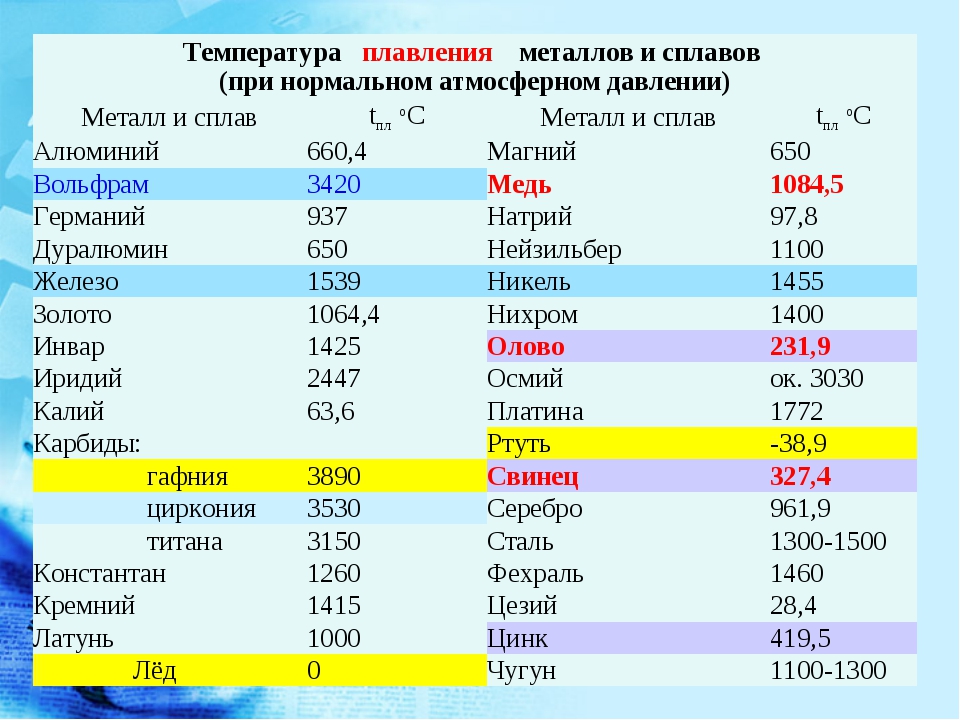
Наиболее тугоплавкими являются следующие металлы: гафний, иридий, молибден, ниобий, осмий, рений, рутений, тантал, технеций, вольфрам. Температура плавления этих металлов выше 2000°С.
Приведем примеры температуры плавления металлов, широко применяемых в промышленности и в быту:
- температура плавления алюминия 660,32 °С;
- температура плавления меди 1084,62 °С;
- температура плавления свинца 327,46 °С;
- температура плавления золота 1064,18 °С;
- температура плавления олова 231,93 °С;
- температура плавления серебра 961,78 °С;
- температура плавления ртути -38,83°С.
Максимальной температурой кипения из металлов, представленных в таблице, обладает рений Re — она составляет 5596°С. Также высокими температурами кипения обладают металлы, относящиеся к группе с высокой температурой плавления.
Плотность металлов в таблице находится в диапазоне от 0,534 до 22,59 г/см 3 , то есть самым легким металлом является литий, а самым тяжелым металлом осмий.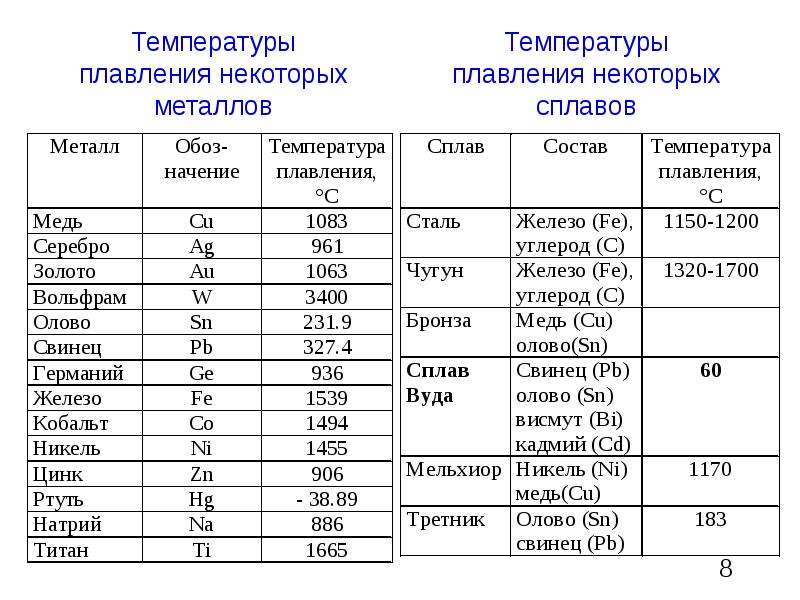 Следует отметить, что осмий имеет плотность большую, чем плотность урана и даже плутония при комнатной температуре.
Следует отметить, что осмий имеет плотность большую, чем плотность урана и даже плутония при комнатной температуре.
Теплопроводность металлов в таблице изменяется от 6,3 до 427 Вт/(м·град), таким образом хуже всего проводит тепло такой металл, как нептуний, а лучшим теплопроводящим металлом является серебро.
Температура плавления стали
Представлена таблица значений температуры плавления стали распространенных марок. Рассмотрены стали для отливок, конструкционные, жаропрочные, углеродистые и другие классы сталей.
Температура плавления стали находится в диапазоне от 1350 до 1535°С. Стали в таблице расположены в порядке возрастания их температуры плавления.
| Сталь | tпл, °С | Сталь | tпл, °С |
|---|---|---|---|
| Стали для отливок Х28Л и Х34Л | 1350 | Коррозионно-стойкая жаропрочная 12Х18Н9Т | 1425 |
| Сталь конструкционная 12Х18Н10Т | 1400 | Жаропрочная высоколегированная 20Х23Н13 | 1440 |
| Жаропрочная высоколегированная 20Х20Н14С2 | 1400 | Жаропрочная высоколегированная 40Х10С2М | 1480 |
| Жаропрочная высоколегированная 20Х25Н20С2 | 1400 | Сталь коррозионно-стойкая Х25С3Н (ЭИ261) | 1480 |
| Сталь конструкционная 12Х18Н10 | 1410 | Жаропрочная высоколегированная 40Х9С2 (ЭСХ8) | 1480 |
| Коррозионно-стойкая жаропрочная 12Х18Н9 | 1410 | Коррозионно-стойкие обыкновенные 95Х18…15Х28 | 1500 |
| Сталь жаропрочная Х20Н35 | 1410 | Коррозионно-стойкая жаропрочная 15Х25Т (ЭИ439) | 1500 |
| Жаропрочная высоколегированная 20Х23Н18 (ЭИ417) | 1415 | Углеродистые стали | 1535 |
- Волков А.
 И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.
И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с. - Казанцев Е. И. Промышленные печи. Справочное руководство для расчетов и проектирования.
- Физические величины. Справочник. А. П. Бабичев, Н. А. Бабушкина, А. М. Братковский и др.; Под ред. И. С. Григорьева, Е. З. Мейлихова. — М.: Энергоатомиздат, 1991. — 1232 с.
Свинец является химическим элементом из 14 группы, таблицы Д. И. Менделеева. Свинец получил 82 номер. Свинец является ковким и пластичным металлом серебристого оттенка, включая синеватый оттенок. Элемент повсеместнораспространен по поверхности Земли, легко добывается и поддается влиянию. Первые украшения и свинцовые предметы роскоши (Бусинды) с применением металлургической деятельности, дают право утверждения, что плавление металла как свинца, стала первой в истории человечества около 6400 г. до н. э. Самым старым изделием из свинцового сплава считается женская статуэтка в одежде из храма Осириса (3100 – 2900 гг. до н. э.). Древний Рим производил до 80 тыс. тонн свинца в год, в том числе для водопровода. На территории Руси металл нашел применение в обустройстве крыш, для печатей при создании грамот. Происхождения слов «свинец» до сих пор не ясно, на латинском языке название произошло от слова plumber (водопроводчик).
э.). Древний Рим производил до 80 тыс. тонн свинца в год, в том числе для водопровода. На территории Руси металл нашел применение в обустройстве крыш, для печатей при создании грамот. Происхождения слов «свинец» до сих пор не ясно, на латинском языке название произошло от слова plumber (водопроводчик).
Алхимики связывали элемент с Сатурном. К 1840 г. промышленная революция спровоцировала выработку свинца до уровня 100 тыс. тонн, а ко второй пол. XIX ст. производилось уже 250 тыс. тонн. До 1990 годов элемент активно применяли в типографии.
Свинец характеристика
Компонент редко обнаруживается в самородном виде. Существует более 80 минеральных пород с включением элемента, например: церуссит, галенит, англезит.
Технологические свойства и характеристики металла
Свинец получил типичные особенности и технологические свойства своей группы и характеризуется повышенной тяжестью, и плотностью с традиционным серым оттенком. При контакте с воздухом металл теряет блеск.
Несмотря на высокую плотность металл проявляет существенную мягкость, при комнатной температуре на нем можно оставить след ногтем.
Плотность свинца и его масса
Масса элемента равняется 82, что является причиной большого веса. Кристаллическая решетка получила кубическую форму. В углу модели молекулы и посредине всех граней находится атом.
Высокая масса относит вещество в состав списка тяжелых компонентов. При нагревании плотность материала падает.
Какая температура плавки свинца?
Свинец не является тугоплавким веществом, что выделяет его из прочих плотных элементов. Вещество легко можно деформировать и прокатать в фольгу.
Температура полного плавления свинца – 327,46 °С. Что бы узнать какая точная температура плавления свинца достаточно применить формулу F = 1,8 °C + 32. Таким образом плавление свинца происходит при температуре 620,6 F.
Температура кипения элемента наступает при – 1749 °С. Чтобы провести процедуру литья необходимо довести компонент до 400–450 °С.
Стоит отметить что при температуре -7,26 К, компонент получает сверхпроводимость. При плавлении компонент получает текучие свойства, увеличивается вязкость и изменяется поверхностное напряжение.
Механические свойства
Высокая пластичность стала причиной плохих прочностных качеств.
- Сопротивление разрыву – до 13 Мпа (у железа показатель – 250 МПа).
- Твердость по Бринеллю составляет – 3,2 – 8 НВ.
- Предел при сжатии – до 50 Мпа.
- Удлинение материала не более 50-70%.
Теплопроводность в два раза меньше, чем у Феррума, в 11 раз ниже показателя меди и составляет 33,5 вт/(м·К). При комнатной температуре значение теплоемкости – 0,12 кДж/(кг·К).
Электропроводность в нормальных условиях проявляет плохую электропроводность: удельное сопротивление равно 0,22 Ом-кв. мм/м. У меди такой показатель достигает 0,017.
Сопротивление коррозии
По своим инертным свойствам свинец приближается к категории благородных металлов. Высокий порог вступления в реакцию и наличие оксидной пленки, обеспечивают высокую сопротивляемость ржавчине. Серная кислота, а также угольный ангидрид, растр сероводорода не воздействует на элемент. В городской местности уровень коррозии может достигать -0,00068 мм/год.
Высокий порог вступления в реакцию и наличие оксидной пленки, обеспечивают высокую сопротивляемость ржавчине. Серная кислота, а также угольный ангидрид, растр сероводорода не воздействует на элемент. В городской местности уровень коррозии может достигать -0,00068 мм/год.
Свинец стойкий к хромовой, концентрированной уксусной, фосфорной кислоте. Компонент быстро разрушается в азотной и разбавленной уксусной кислоте и концентрированной серной (90%).
Области применения свинцовых сплавов
Свинец активно применяется для источника тока полученного химическим путем. Около ¾ всей массы произведенного металла используется для создания свинцовых аккумуляторов. Несмотря на конкуренцию щелочных источников энергии, свинец вырабатывает электричество более высокого напряжения. Элемент применяется для обмоток сверхпроводящих трансформаторных систем. Компонент был одним из первых замеченных веществ со свойствами сверхпроводимости. Свинцовый сплав (баббит) нашел применение в создании подшипников, благодаря антифрикционным свойствам.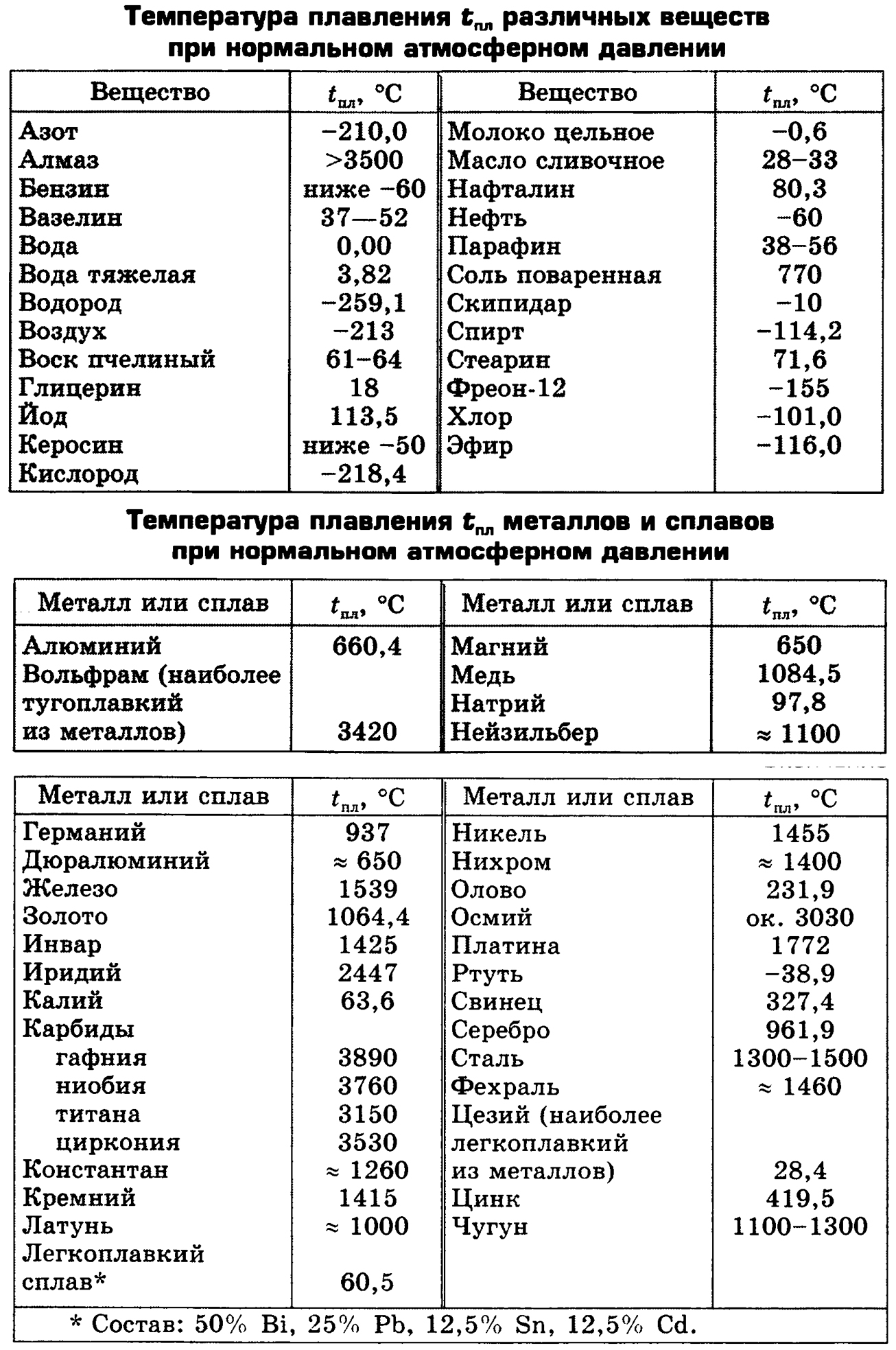 Свинец широко применяется для создания электрических предохранительных систем благодаря возможности создания легкоплавких соединений с другими металлами (кадмием или оловом).
Свинец широко применяется для создания электрических предохранительных систем благодаря возможности создания легкоплавких соединений с другими металлами (кадмием или оловом).
Подшипники из свинцового сплава
20% всего объема компонента идет на создание оболочки силового кабеля для подземных и подводных линий. Свинец начали применять в военном деле во времена Римского государства, в качестве снарядов для катапульты. Современная промышленность производит из свинца пули и другие комплектующие для спортивного инвентаря, боевого и охотничьего оружия. Свинец популярен в качестве универсального припоя, включая случаи, когда соединить метал другим вариантом затруднительно.
Металл активно применяется для защиты от радиоактивного излучения, благодаря своей массе. Благодаря дешевизне компонент устанавливается в рентген кабинетах, и на ядерных полигонах.
Также элемент используется, как часть звукоизоляционного покрытия и в кровельном деле. Также материал используют в сейсмостойких фундаментах строений, и уплотнений между кладкой.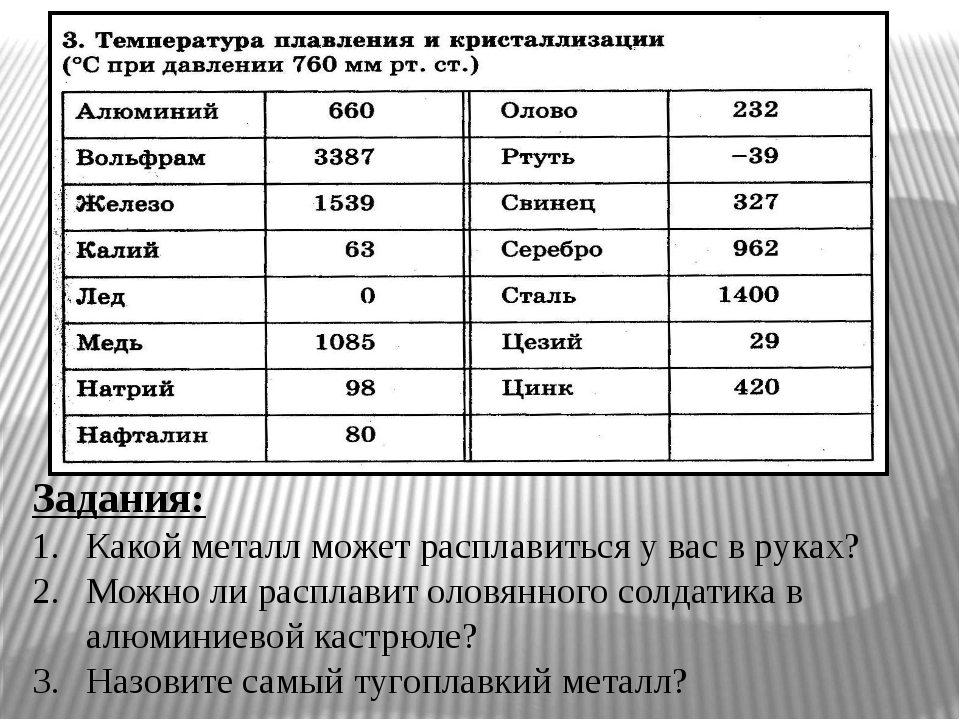 Краска со свинцом используется на технических сооружениях (мосты, каркасные строения).
Краска со свинцом используется на технических сооружениях (мосты, каркасные строения).
Домашние и промышленные способы
Для выделения и плавления чистого свинца, чаще всего используют галенит, как основу плавки. Способом флотации обогащают концентрат до 40-70%. Далее применяют несколько методов плавления:
- Электротермическое плавление.
- Способ термического плавления Ванюкова (расплавление в жидкой ванне).
- Плавление в шахтной (ватержакетной) печи.
После химической обработки удаляют примеси других элементов, в результате чистота свинца достигает более 99%.
Главными производителями являются: страны ЕС (плавление 2200 килотонн), США (1400), КНР (1200), РФ (1100). Также широкое производство плавления компонента находится в Южной Корейской республике, Украине и Казахстане.
Приготовление расплава
Для начала плавления в домашних условиях подбирается емкость с жаростойкой ручкой, которая выдержит высокую температуру.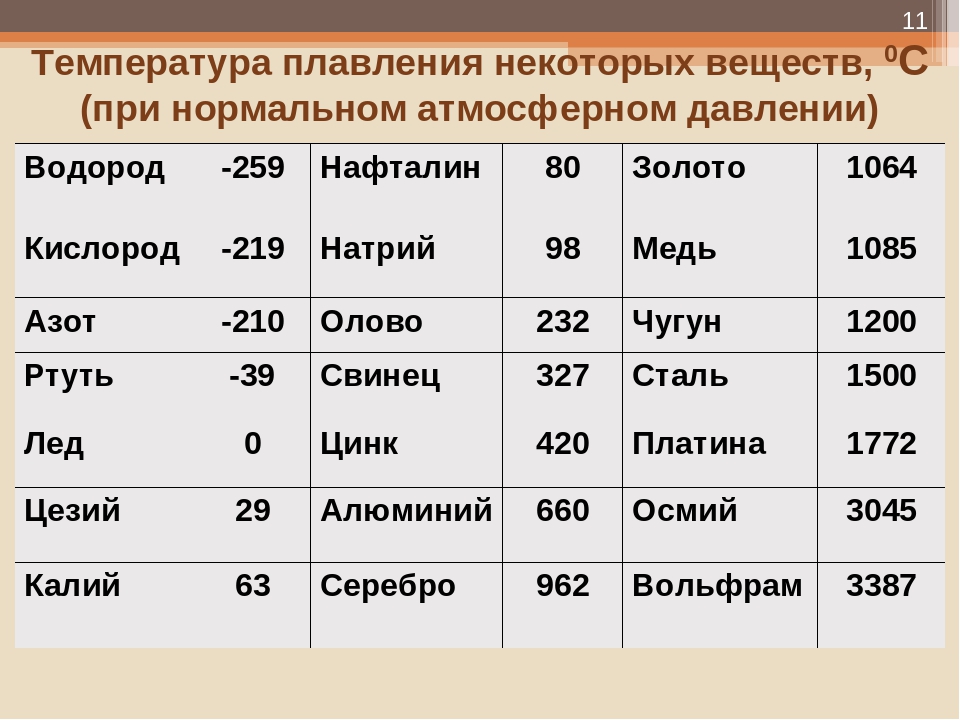 Для такой функции подходит старый кухонный чайник или подобная бытовая утварь. В домашних условиях можно применять чугунную посуду, при отсутствии других вариантов используют консервные емкости, с использование плоскогубцев в виду высокой температуры операции. Заранее следует предусмотреть будущее место захвата банки инструментом. Для удобства, в жестяной банке можно проделать отверстие в районе ободка. Это даст возможность точно выливать металл с высокой температурой, в нужном месте, без потеков расплавленной массы снаружи емкости.
Для такой функции подходит старый кухонный чайник или подобная бытовая утварь. В домашних условиях можно применять чугунную посуду, при отсутствии других вариантов используют консервные емкости, с использование плоскогубцев в виду высокой температуры операции. Заранее следует предусмотреть будущее место захвата банки инструментом. Для удобства, в жестяной банке можно проделать отверстие в районе ободка. Это даст возможность точно выливать металл с высокой температурой, в нужном месте, без потеков расплавленной массы снаружи емкости.
Обрабатываемый материал размельчают и избавляют массу от лишних включений любыми доступными способами. Чем лучше будет размельчен металл, тем быстрее он расплавится. Емкость необходимо надежно установить над источником огня и прогреть для ликвидации влаги и сторонних примесей.
Кипение свинца достигается при температуре более 1700 °C. В домашних условиях такую температуру создать невозможно, однако при температуре 700 °C элемент проявляет высокую летучесть. Таким образов при отсутствии специального оборудования и практической необходимости, не стоит доводить свинец до температуры с красным оттенком, в виду вредности испарений для окружающих лиц.
Таким образов при отсутствии специального оборудования и практической необходимости, не стоит доводить свинец до температуры с красным оттенком, в виду вредности испарений для окружающих лиц.
Процесс плавления и заливка
В подогреваемую емкость не стоит сразу погружать весь лом. Контактировать с нагретым дном будет только тонкий слой, а остальная приобретенная температура будет рассеиваться в массе свинца. Для эффективной плавки лучше бросить небольшое количество в уже разогретую ванну постепенно помещая остальные части. Это увеличит площадь разогретой массы с высокой температурой.
После разогрева всей массы лома. На поверхности образуется шлаковый слой, который нужно убрать ложкой с длинной ручкой или подобным средством. Если масса получила единую разогретую консистенцию ее стоит переместить в предварительно разогретую форму. Низкая температура плавления провоцирует быстрое застывание в кристаллический вид.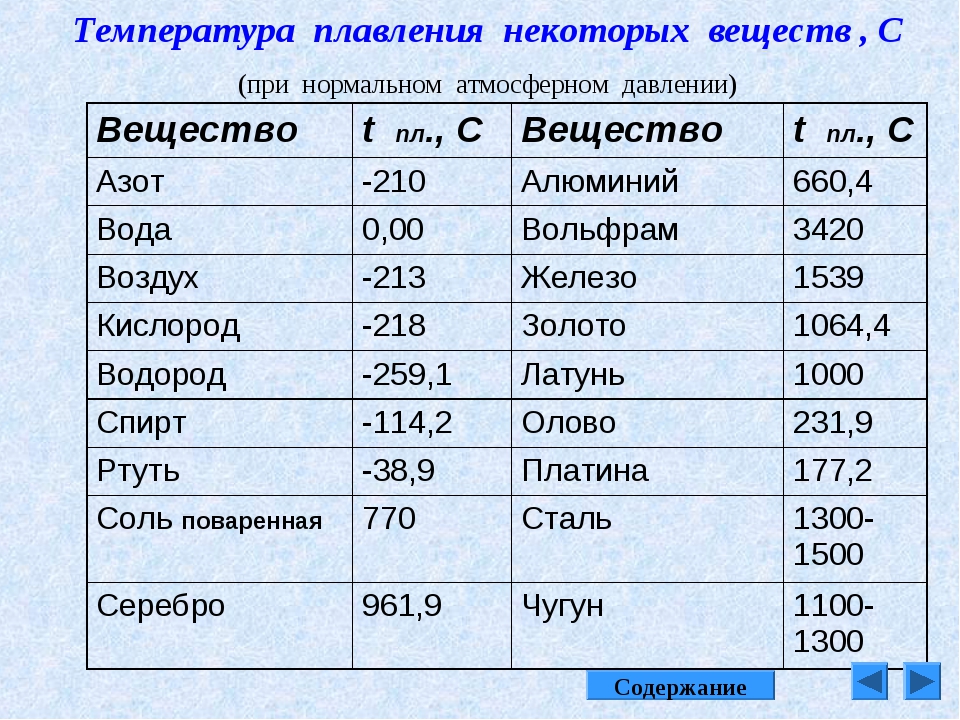 Если форма не разогрета, свинец начнет неровно ложится прямо во время заливки, и изделие получится неоднородным с присутствием дефектов.
Если форма не разогрета, свинец начнет неровно ложится прямо во время заливки, и изделие получится неоднородным с присутствием дефектов.
Рыболовные лаки
Свинцовые изделия, статуэтки или рыболовные снасти можно покрывать лаком, используемым рыбаками. У любителей рыбной ловли есть несколько функций для этого ингредиента. Однако с предотвращением оксидного слоя на поверхности, раствор также эффективно справляется. Производят жидкость для придания старым наживкам и грузилом былого блеска.
Методы избавления от оксида
Во время взаимодействия с воздухом между атомами металла и окружающей средой образуется ионная связь. Кислород отдает два электрона. На поверхности быстро возникает окислительный слой. Такая оксидная пленка способна предотвратить дальнейшее воздействие враждебной среды. Пленка, также становится барьером во время передачи электричества.
Оксидная пленка на продукте, изготовленном из свинца появляется через малый промежуток времени.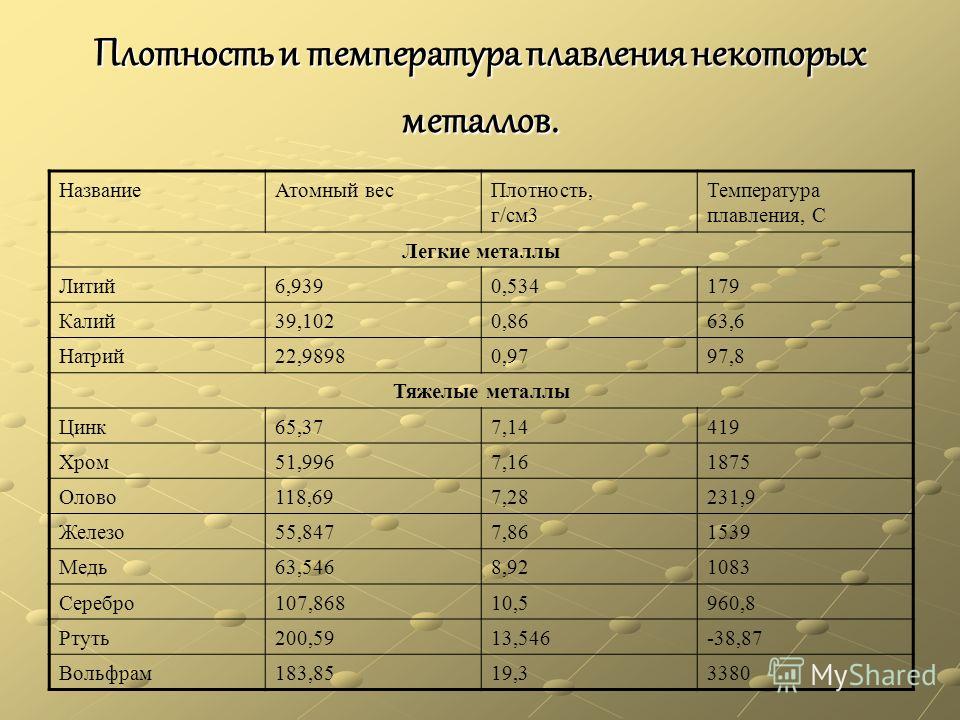 Механическая очистка – довольно трудоемкое и бесполезное занятие. Сразу после успешного снятия слоя, образуя поле, и оголенные атомы вступают в связь с новыми атомами воздуха. Создать защиту для предмета можно при использовании масла подсолнуха. Также актуален вариант с графитовой смазкой и лаком.
Механическая очистка – довольно трудоемкое и бесполезное занятие. Сразу после успешного снятия слоя, образуя поле, и оголенные атомы вступают в связь с новыми атомами воздуха. Создать защиту для предмета можно при использовании масла подсолнуха. Также актуален вариант с графитовой смазкой и лаком.
Для домашнего обихода отлично подходит масло подсолнуха. Масло наливают в миску, после чего в жидкость помещают требуемое изделие из свинца. При правильной выдержки (около 5 минут), необходимо вытянуть изделие из масла и дать ему просохнуть на подготовленных салфетках.
В условиях производства для уменьшения распространения оксидных включений на поверхности деталей применяют графитовую смазку. Смазка не является редкой или дорогостоящей, однако в бытовых условиях она редко оказывается в наличии. Такое средство продается в автомагазинах и хозяйственных торговых точках. При должном отношении свинцовая поверхность будет длительное время демонстрировать блеск.
Графитовая смазка для свинца
Если оксидная пленка уже успешно покрыла поверхность, существуют способы ее удаления. Для этого, применяется концентрированный раствор кислоты. Для таких действий необходима специальная подготовка, включая наличие химического стеклянного инвентаря. Обычные столовые банки или миски не подойдут. Реактивные ингредиенты могут нанести вред человеку, оставить ожоги на теле.
Для этого, применяется концентрированный раствор кислоты. Для таких действий необходима специальная подготовка, включая наличие химического стеклянного инвентаря. Обычные столовые банки или миски не подойдут. Реактивные ингредиенты могут нанести вред человеку, оставить ожоги на теле.
Приветствуется использование защитных очков и маски.
Обрабатываемое изделие погружается в кислотный раствор. Необходимо подождать пока пленка оксида будет разрушена. После успешного подъема из раствора обрабатывается поверхность для защиты маслом или лаком.
Техника безопасности
Расплавленный свинец способен произвести значимые увечья и ожоги. Капля мгновенно пропалит одежду и попадет на открытую поверхность кожи. Жидкая форма свинца может при вытекании попасть на легко возгораемые предметы и спровоцировать пожар в помещении. Если в жидкий расплав проникает вода происходит резкая вспышка с распространением мелких брызг металла по всей площади. Такие включения могут попасть на кожу и глаза, что болезненно и опасно для органов человека.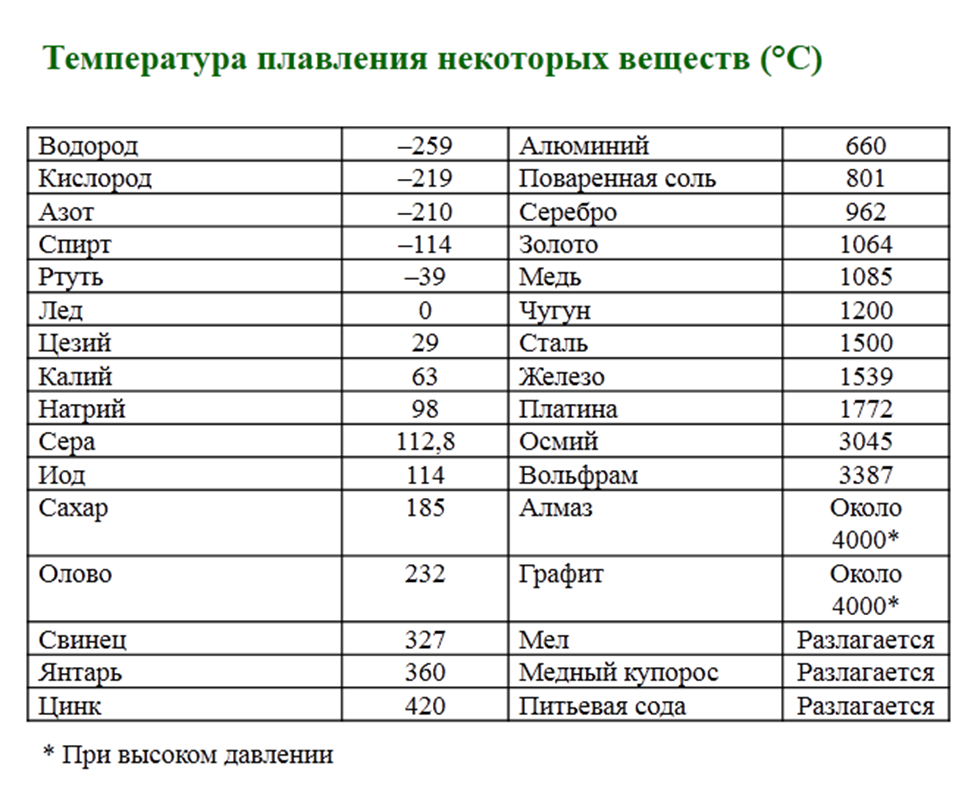 Таким образом, обязательно во время работы необходимо использование одежды, которая покроет все тело включая рукава, надевайте головной убор. Ткань должна быть с высокой огнеупорностью и термостойкостью. На лицо необходимо надеть маску и защитные очки.
Таким образом, обязательно во время работы необходимо использование одежды, которая покроет все тело включая рукава, надевайте головной убор. Ткань должна быть с высокой огнеупорностью и термостойкостью. На лицо необходимо надеть маску и защитные очки.
Помещение, в котором проводят плавку, необходимо хорошо проветривать, ввиду токсичности испарения свинца. Если маски нет в наличии используйте ватно-марлевую повязку. При попадании в организм свинец может спровоцировать и усугубить ряд болезненных процессов, накапливаясь в органах, элемент вызывает острое отравление.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Свинец, обозначаемый символом Pb (плюмбум), относится к тем металлам, которые были известны человечеству издавна. Свинцовые находки в виде бусин датируются 6000 лет до нашей эры. В Древнем Риме делали свинцовые водопроводы, посуду, пока не была доказана токсичность свинцовых соединений.
Сейчас это металл стратегический, он используется в оборонной промышленности. Из него делают взрывчатые вещества, источники тока. Производство свинца недорогое, металл добывают из распространенных в природе минералов. Сначала получают черновой сплав, затем чистый.
Расплавить свинец в домашних условиях несложно, температура плавления у свинца и его сплавов не выше +330–450°С, припоев не выше +230°С. Металл не подвержен коррозионным разрушениям, пластичный, ковкий, применяется во многих промышленных сферах. Из него делают бытовые предметы, рыбацкие снасти, припои своими руками, заполняя формы жидким свинцом.
Характеристики и особенности свинца
Металл грязно-серебристого или серебристо-синеватого цвета имеет большой удельный вес – 11,34 г/см 3 . Прочность на разрыв не более 18 МПа. на сжатие в пределах 50 МПа. Из-за высокой пластичности поддается многим видам механической обработки, его подвергают холодной прокатке до состояния фольги, штампуют, режут, подвергают нагартовке.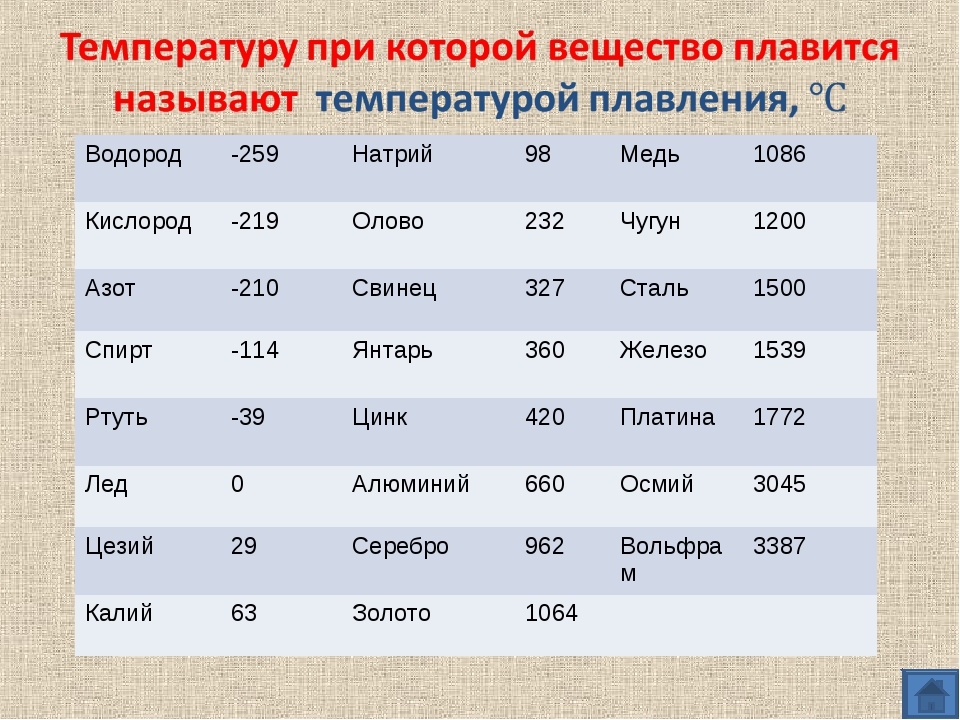 При волочении свинец рвется, проволоку из него делают продавливанием заготовок в фильерах.
При волочении свинец рвется, проволоку из него делают продавливанием заготовок в фильерах.
При охлаждении до -266°С свинец становится сверхпроводником, несмотря на невысокую электропроводность при комнатной температуре (удельное сопротивление 0,22 Ом*мм 2 /м). На воздухе свинец быстро тускнеет на срезе, пассируется, покрывается оксидной пленкой, характеризующейся низкой химической активностью. Сам металл тоже стоек к коррозионным разрушениям, поэтому из свинца и сплавов делают кислотостойкие сосуды, емкости. Pb— последний элемент в периодической таблице Менделеева со стабильными изотопами. Металл способен удерживать радиоактивное излучение.
Кубическая, гранецентрированная структурная решетка обеспечивает вязкость металла, его сложно разломить, но он хорошо режется, его легко исцарапать, смять. При нагревании структура становится текучей, исходная вязкость снижается.
Температура плавления свинца
Плавка предусматривает фазовый переход под термическим влиянием. Легкоплавкие свинцовые сплавы льют при +400–450°С, технологическая температура достигается в домашних условиях на открытом пламени горелки, конфорке электро- или газовой плиты. В справочной литературе указывают температуру плавки свинца равной +327, 4°С. Для сплавов показатели иные, они зависят от физических характеристик компонентов, входящих в состав сплавов. У припоев с оловом и кадмием температура плавления на 40–60 градусов ниже в зависимости от концентрации добавки.
В справочной литературе указывают температуру плавки свинца равной +327, 4°С. Для сплавов показатели иные, они зависят от физических характеристик компонентов, входящих в состав сплавов. У припоев с оловом и кадмием температура плавления на 40–60 градусов ниже в зависимости от концентрации добавки.
При +700°С свинцовый расплав испаряется, образуя токсичный аэрозоль. Вскипает металл при +1750°С. Оксидный слой претерпевает фазовые изменения из твердого в жидкое состояние только при нагреве до +850°С.
Область применения
Несмотря на токсичность, свинец ценится за коррозионную устойчивость, способность задерживать γ -излучение. Он остается незаменимым во многих отраслях.
До 75% получаемого свинца используется в электротехнике для аккумуляторных пластинок и трансформаторных сверхпроводниковых систем, силового кабеля. Баббит – сталь, легированная Рb, отличается антифрикционными свойствами. Сплавы, содержащие олово и кадмий, используют для припоев.
Плюмбум входит в состав антикоррозионных покрытий, красителей. Из него отливают пули и дробь, печатный шрифт, статуэтки, грузила. Листами металла экранируют рентгеновые установки, атомные реакторы, бункеры на полигонах. Пластины вшивают в фартуки, жилеты, другую защитную одежду. Свинцовые плиты снижают вибрацию, сейсмические толчки. Их используют в строительстве для уплотнения кладки, фундамента, мостовых опор. Из нитрата производят взрывчатые вещества с большой детонацией.
Из него отливают пули и дробь, печатный шрифт, статуэтки, грузила. Листами металла экранируют рентгеновые установки, атомные реакторы, бункеры на полигонах. Пластины вшивают в фартуки, жилеты, другую защитную одежду. Свинцовые плиты снижают вибрацию, сейсмические толчки. Их используют в строительстве для уплотнения кладки, фундамента, мостовых опор. Из нитрата производят взрывчатые вещества с большой детонацией.
В чем плавить свинец
На заводах в качестве плавильных емкостей используют:
- специальные тигли из огнеупорной керамики или тугоплавких металлов, их помещают в электропечи, обеспечивающие необходимый термальный режим;
- нагревательные ванны, они снабжены встроенными тенами, поддерживают необходимую температуру металла по всему периметру.
Плавить свинец самостоятельно дома, во дворе, гараже или мастерской можно в жестяной банке, она заменит тигель. На одной стороне жестянки делают желоб для заливки металла в форму. Края формы подгибают, чтобы они надежно фиксировались в зажиме. Вместо прихваток горячую емкость надежнее придерживать пассатижами, плавильня не будет прожигать руки по время заполнения формы.
Вместо прихваток горячую емкость надежнее придерживать пассатижами, плавильня не будет прожигать руки по время заполнения формы.
Можно воспользоваться для плавки свинцового лома старой домашней утварью: кастрюлями, сковородами, нержавеющими или эмалированными чайниками, или другой жаропрочной посудой. Шлаковый слой удаляют специальной ложкой с длинной ручкой. Делают это непосредственно перед заливкой металла в подготовленные формочки.
Процесс плавки
В качестве источника тепла для расплавления лома используют:
- костер, над ним устанавливают подставку для плавильни;
- паяльную лампу, ее фиксируют в стационарном положении;
- газовую горелку, ей металл разогревают и снизу, и сверху, попеременно;
- кухонную плиту (газовую или электрическую).
Емкость устанавливают так, чтобы языки пламени не выходили за площадь дна.
Плавка свинца начинается с подготовительного этапа: нужно приготовить плавильную емкость, измельчить лом. Его очищают от примесей, возможной влаги, загрязнений. Затем разрезают на небольшие кусочки ножом или ножницами по металлу. Ломать свинцовые куски сложно, они отлично гнутся. Чем мельче будет лом, тем быстрее он расплавится. Его рекомендуют закладывать в плавильную емкость постепенно. Когда кусочки загружают в расплав, снижается риск перегрева расплава до температуры летучести. Не стоит разогревать кусочки до красноватого оттенка, это сигнал, что образуют ядовитые летучие соединения.
Его очищают от примесей, возможной влаги, загрязнений. Затем разрезают на небольшие кусочки ножом или ножницами по металлу. Ломать свинцовые куски сложно, они отлично гнутся. Чем мельче будет лом, тем быстрее он расплавится. Его рекомендуют закладывать в плавильную емкость постепенно. Когда кусочки загружают в расплав, снижается риск перегрева расплава до температуры летучести. Не стоит разогревать кусочки до красноватого оттенка, это сигнал, что образуют ядовитые летучие соединения.
Если для расплава используют емкость с толстыми стенками, ее предварительно прогревают. Жесть достаточно просушить. Плавильню заполняют не более, чем на половину, лучше на 1/3. Толстый слой равномерно не прогреется.
Плавильня должна устойчиво стоять на горелке, не шататься. После расплавления лома на поверхности образуется шапка шлака. Ее снимают перед розливом расплава в форму. Ее предварительно прогревают, чтобы не было резкого температурного контраста. В холодную форму расплав заливается неравномерно. На поверхности литья образуются рытвины, складки, другие дефекты.
На поверхности литья образуются рытвины, складки, другие дефекты.
Техника безопасности
Занимаясь плавлением свинца в изолированном помещении, важно позаботиться:
- о вентиляции, необходимо принудительно нагнетать воздух вентилятором, чтобы концентрация горячего аэрозоля была минимальной, свинцовые соединения пагубно влияют на мозг, печень, почки;
- о защите органов дыхания (нужен респиратор), зрения (стоит надеть рабочие очки), одежде с длинным рукавом из натуральных материалов, синтетика при случайном попадании плавится, увеличивается площадь ожога;
- пожарной безопасности, под руками необходимо держать огнетушитель.
Жидкий свинец обладает высокой текучестью. При попадании на влажную поверхность сильно разбрызгивается. Возможны выплески расплава во время нагрева свинцового лома. В рабочей зоне необходимо убрать или изолировать легко возгораемые предметы.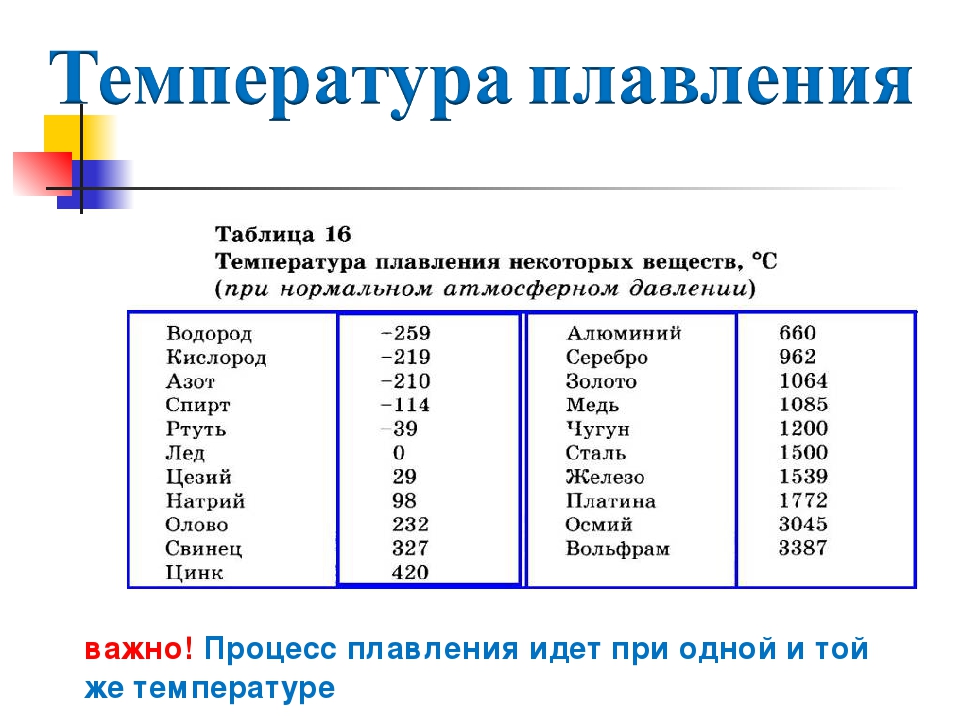
Свинец температура плавления — Справочник химика 21
Изоморфные смеси образуются при стягивании атомов и ионов в кристаллическую решетку. Причем атомы и ионы одного вещества становятся в узлы кристаллической решетки другого. Но можно наблюдать образование твердых растворов и путем диффузии одного твердого вещества в другое. Так, при 251 С золото диффундирует в свинец (температура плавления золота 1063 , свинца 327,4° С). При высокой температуре углерод диффундирует в железо, образуя твердый раствор. В этих случаях атомы или ионы второго вещества внедряются в промежутки между элементами кристаллической решетки, отчасти деформируя ее (твердые растворы внедрения).Свинец (температура плавления 327 j [c.200]
Изготовление припоя или третника. Отвешивают на 2 вес. ч. олова 1 вес. ч. свинца. Навески металлов при помешивании расплавляются в железном тигельке.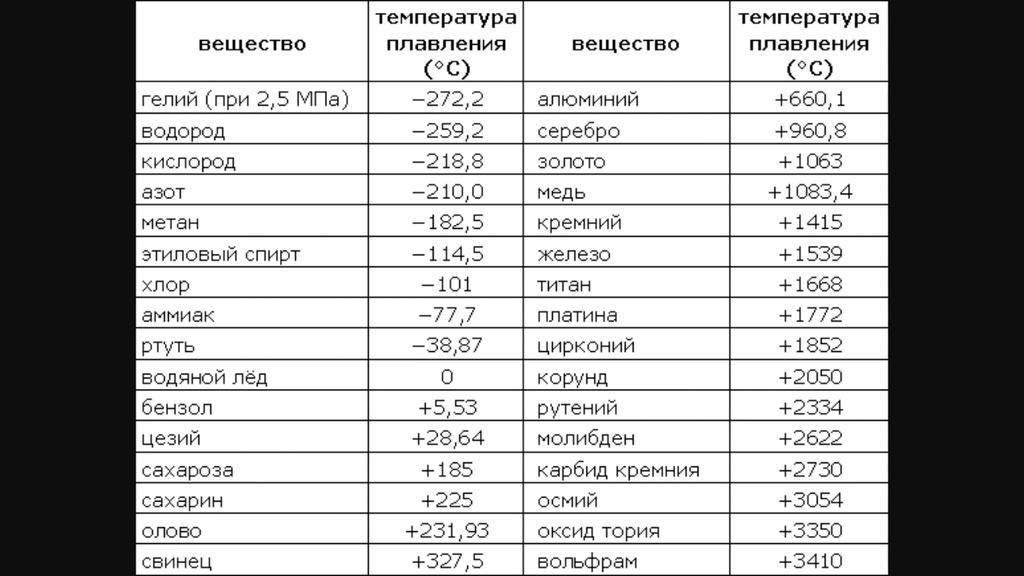 Сначала плавится олово (температура плавления 232°С), а затем —свинец (температура плавления 328° С) полученный сплав выливают в сделанную из бумаги форму (на стеклянную трубку навертывают плотную бумагу, обвязывают ниткой, снимают с трубки, закрывают пробкой или отрезком деревянной палочки). [c.251]
Сначала плавится олово (температура плавления 232°С), а затем —свинец (температура плавления 328° С) полученный сплав выливают в сделанную из бумаги форму (на стеклянную трубку навертывают плотную бумагу, обвязывают ниткой, снимают с трубки, закрывают пробкой или отрезком деревянной палочки). [c.251]
Металлические покрытия горячим методом наносят на изделие или заготовку путем их погружения на несколько секунд в ванну с расплавленным металлом. Этим способом на изделия наносят цинк (температура плавления 419°С), олово (температура плавления 232°С), свинец (температура плавления 327°С), алюминий (температура плавления 658°С), т. е. металлы, имеющие низкую температуру плавления. Перед нанесением на изделие покрытия его обрабатывают флюсом, например, состоящим из 55,4% хлористого аммония, 6% глицерина, 38,4% хлористого цинка. Флюс защищает расплав от окисления и, кро.ме того, удаляет с поверхности оксидные и другие пленки, что улучшает адгезию металла с металлом покрытия.
Мягкие металлы обычно не применяют при нагреве выше их температуры плавления. Поэтому, например, свинец (температура плавления 327°С) не может работать при таких высоких температурах, как золото (температура плавления 1063°С). В ряде случаев мягкие металлы теряют свою работоспособность уже при меньших температурах. Барий может применяться при температурах до 600 °С [143]. Преимущество благородных металлов заключается в их малой чувствительности к внешним условиям. Некоторые металлические покрытия снижают износ даже в условиях криогенных температур [177]. [c.266]
Низкотемпературные припои применяются в случаях, когда паяное соединение в работе не подлежит нагреву выше 100 С и от него не требуется прочиость выше 50 МПа (5 кг/мм ). Типичными примерами этой группы являются оловянно-свинцовые припои (например, ПОС-61 — 61% олова, остальное- свинец, температура плавления 183…190 С), а также припои на основе галлия, висмута, индия, кадмия (температура плавления не превышает 145 С). В качестве флюсов здесь, как правило, используется канифоль с различными добавками. [c.99]
В качестве флюсов здесь, как правило, используется канифоль с различными добавками. [c.99]
Я Нужен металл с низкой температурой плавления и высокой температурой кипения (тогда не будет паров — это хорошо). Свинец или олово. Нет, пары свинца ядовиты. Значит — олово. [c.81]
Вследствие низкой температуры плавления свинец можно применять при температурах порядка 150—200° С при более высокой температуре свинец начинает постепенно терять прочность и коррозионную стойкость. Низкая теплопроводность не позволяет использовать свинец в теплообменной аппаратуре, а высокий удельный вес приводит к увеличению веса конструкций. Плохие литейные свойства свинца не позволяют применять его для отливок. Свинец также склонен к рекристаллизации. [c.261]
Сплавы на алюминиевой основе стойки против многих расплавленных солей, имеющих нейтральную реакцию. Расплавленный свинец, имеющий более низкую температуру плавления, чем алюминиевые сплавы, также совершенно не действует на них. [c.272]
[c.272]
Свинец характеризуется низкой температурой плавления (327°С), низкой прочностью и высокой пластичностью. Он применяется для защиты поверхностей стальных аппаратов, соприкасающихся с агрессивной средой (слабых водных растворов, содержащих углекислоту, сероводород, соли). Защищаемая поверхность покрывается листовым свинцом толщиной 2—5 мм или подвергается гомогенному освинцованию, т. е. наплавлению свинцового слоя толщиной 4—6 мм. Перед освинцеванием направляемая поверхность должна быть предварительно покрыта оловом. [c.34]
Диаграмму второго типа иллюстрирует система магний— свинец (см. рис. 10), где Ь и й — эвтектические точки, с — температура плавления химического соединения Мд2 Ь, аЬ кривая кристаллизации Mg, ей — кри- [c.43]
Свинец Паяльный сплав 67 Pb, 33 Sn Низкая температура плавления Паяные соединения [c.363]
Постепенное понижение температур плавления и повышение электропроводности в ряду элементов главной подгруппы IV группы нарушается для пары Sn—РЬ. По некоторым своим химическим свойствам, так же, как и по физическим, олово является более типичным металлом, чем свинец. Эта аномалия может быть отнесена к разряду явлений, обусловленных вторичной периодичностью. [c.94]
По некоторым своим химическим свойствам, так же, как и по физическим, олово является более типичным металлом, чем свинец. Эта аномалия может быть отнесена к разряду явлений, обусловленных вторичной периодичностью. [c.94]
Свинец в большей степени, чем железо, увеличивает температуру плавления с ростом давления при относи- [c.52]
Диаграммы состояния систем, состоящих из веществ, не образующих химических соединений. На рис. 2.33 показана диаграмма состояния системы 8Ь — РЬ эти вещества неограниченно растворимы друг в друге в жидком состоянии и нерастворимы в твердом состоянии. В верхней части рисунка схематически представлен общий вид диаграммы данного типа. Точка а отвечает температуре плавления компонента А (сурьма, 631 С), точка А — температуре плавления компонента В (свинец, 327 0 кривые аЕ и > -кривые кристаллизации соответственно 5Ь и РЬ. [c.307]
Как видно из табл. 26, у углерода самый малый для элементов этой группы радиус атома, высокий ионизационный потенциал, большая температура плавления. Это характерно для типичного неметалла. Типичным неметаллом является также кремний. У германия проявляются некоторые металлические свойства, а олово и свинец — металлы. Они больше сходны по свойствам друг с другом, чем с германием. Сказывается экранирующее действие электронных подуровней, снижающих притяжение валентных электронов к ядру атома. Например, по электропроводности белое олово и свинец — проводники, германий, кремний и серое олово (а-Зп) — полупроводники, а углерод в виде алмаза — диэлектрик. [c.231]
Это характерно для типичного неметалла. Типичным неметаллом является также кремний. У германия проявляются некоторые металлические свойства, а олово и свинец — металлы. Они больше сходны по свойствам друг с другом, чем с германием. Сказывается экранирующее действие электронных подуровней, снижающих притяжение валентных электронов к ядру атома. Например, по электропроводности белое олово и свинец — проводники, германий, кремний и серое олово (а-Зп) — полупроводники, а углерод в виде алмаза — диэлектрик. [c.231]
Сплавы на основе меди. Бронза — под этим названием выпускаются сплавы, в состав которых входят медь (до 90%), олово (до 10%), свинец (до 1%). При сравнительно низкой температуре плавления (900—1300 ) бронзы обладают ценными механическими свойствами. [c.321]
Свинец — темно-серый мягкий металл, тяжелый, с невысокой температурой плавления и типичной для металлов электрической проводимостью. [c.275]
По физическим свойствам олово и свинец являются металлами с невысокими температурами плавления. [c.236]
[c.236]
Металлохимия элементов подгруппы германия. Элементы подгруппы германия, как и все хр-элементы, обладают сравнительно большими атомными радиусами, причем от германия к свинцу атомный радиус увеличивается весьма значительно. Кроме того, олово и свинец характеризуются невысокими температурами плавления. Поэтому эти вещества являются плохими растворителями в твердом [c.230]
Свинец — мягкий, синевато-серый металл плотностью 11,3 г/см с температурой плавления 327 °С. На воздухе покрывается защитной пленкой оксида (II), но водой постепенно разрушается с образованием гидроксида [c.336]
Высокотемпературный метод применим для нанесения покрытий из легкоплавких металлов на металлы с более высокими температурами плавления. Так, для нанесения защитного металлического покрытия на сталь ной лист его погружают в расплавленный металл (и вынимают также) через слой флюса или масла, закрывающий поверхность жидкого мета лла (Sn, Zn, РЬ), чтобы поверхность сразу не окислилась. Цинк и олово хорошо смачивают сталь, а к свинцу добавляют немного олова, так как свинец плохо смачивает стальную поверхность. [c.405]
Цинк и олово хорошо смачивают сталь, а к свинцу добавляют немного олова, так как свинец плохо смачивает стальную поверхность. [c.405]
Отвечает ли эта последовательность их температурам плавления (сплав 18Г С, олово 232° С и свинец 327° С) По этим данным, рассчитав процентное содержание олова и свинца в сплаве, постройте приближенную диаграмму плавкости, проведя на ней эвтектическую горизонталь. Возьмите любые пять точек в разных областях диаграммы и охарактеризуйте системы, отвечающие этим точкам. Как называется в технике эвтектический сплав олова и свинца [c.108]
Свинец — мягкий пластичный синевато-серый металл температура плавления 237,4°С. [c.183]
Так как с повышением температуры снижается выход по току калия, повышается разрушение графитовых анодов и возрастает коррозионная активность расплава, для получения калия используют электролит, имеющий состав, близкий к эвтектическому либо несколько обогащенный по карбонату калия (без существенного роста температуры плавления). Это позволяет несколько снизить скорость разрушения анодов и уменьшить шламообразование, снижающее пробег электролизера между чистками. В применяемых для электролиза электролитах содержание карбоната калия составляет 20—35% (мол.). Электролиз проводят при температуре 680—720°С. При такой температуре сплав калий — свинец остается жидким при всех соотношениях компонентов (рис. 5,7), однако при электролитическом получении свинцово-калиевого сплава концентрацию калия в нем не повышают более 8% (масс,) из-за заметного снижения выхода по току калия (ниже 80—90%) при более высоких концентрациях калия в сплаве. [c.227]
Это позволяет несколько снизить скорость разрушения анодов и уменьшить шламообразование, снижающее пробег электролизера между чистками. В применяемых для электролиза электролитах содержание карбоната калия составляет 20—35% (мол.). Электролиз проводят при температуре 680—720°С. При такой температуре сплав калий — свинец остается жидким при всех соотношениях компонентов (рис. 5,7), однако при электролитическом получении свинцово-калиевого сплава концентрацию калия в нем не повышают более 8% (масс,) из-за заметного снижения выхода по току калия (ниже 80—90%) при более высоких концентрациях калия в сплаве. [c.227]
При футеровке методом нанайки между свинцом и основным металлом наносят слой оловянистого припоя. Однако в связи с тем, что температура плавления припоя (183° С) значительно ниже температуры плавления свинца (327° С), при работе футерованного оборудования в условиях высокой температуры и давлении свинец часто отслаивается. [c.200]
Медь—свинец. Температура плавления меди 1023° С, свинца 327 С. Монотектический процесс происходит при 954 С. Кривая выделения меди пересекает прямую мо-нотектического процесса в точке, отвечающей 14,7 ат.% РЬ прямая, отвечающая этому процессу, заканчивается при 67 ат.% РЬ. Эвтектика расположена настолько близко к точке плавления свинца, что на чертеже она незаметна. [c.146]
Температура плавления меди 1023° С, свинца 327 С. Монотектический процесс происходит при 954 С. Кривая выделения меди пересекает прямую мо-нотектического процесса в точке, отвечающей 14,7 ат.% РЬ прямая, отвечающая этому процессу, заканчивается при 67 ат.% РЬ. Эвтектика расположена настолько близко к точке плавления свинца, что на чертеже она незаметна. [c.146]
Галлнй Индий Олово Висмут Свинец Температура плавления °С [c.80]
Печн производства желтого и красного пигментов. Общие сведения. Свинец образует с кислородом два окисла РЬО п РЬО,. Окись свинца РЬО называется в технике глетом ее молекулярная масса составляет 223,22 она содержит 92,83% РЬ и 7,17% кислорода. Температура плавления окпси свинца 880— 890 С, температура кипения 1470 «С, но уже при 1000 «С РЬО заметно испаряется. Существует РЬО в виде двух энантиотропных модификаций тетрагональной красно-коричневого цвета и ромбической желтого цвета. Переход одной модификации в другую происходит при 489 °С. [c.158]
[c.158]
Из других жидких нагревающих агентов для заполнения обогревательных бань применяют расплавленные соли и металлы. Расплавленные соли, обычно тройная ннтрнт-нитратная смесь (40% МаЫОз, 7% МаМОа, 53% K Юз), используются для н.згревания в пределах от 142° С (температура плавления смеси) до 500—530° С. Расплавленные металлы (легкоплавкие металлы — свинец, висмут, кадмий, сурьма, олово и их сплавы) применяются для нагревания от точки их плавления до температур порядка 1000° С. [c.416]
Объясните следующие факты. Кремний и германий неограниченно растворяются друг в друге в жидком и твердом состояниях. Германий, олово и свинец образуют друг с другом твердые растворы в очень ограниченных пределах. Германий, олово и свинец друг с дру] ом образую г эвтектику. Например, сплав состава 74% 5п и 26% РЬ имеет температуру плавления 181 °С. Энтектика образуется также в системах 5гг-Ч г1, РЬ—и нр. [c.191]
Свинец характеризуется низкой температурой плавления (327 °С), низкой прочностью и высокой пластичностью, поэтому в качестве конст-рукщюнного материала непригоден. Его применяют для защиты поверхностей стальньк аппаратов, соприкасающихся с агрессивной средой (слабые водные растворы, содержащие углекислоту, сероводород, соли). [c.16]
Его применяют для защиты поверхностей стальньк аппаратов, соприкасающихся с агрессивной средой (слабые водные растворы, содержащие углекислоту, сероводород, соли). [c.16]
Припоями называют сплавы, используемые при пайке металлов высокой проводимости. Для получения хорошего соединения припой должен иметь температуру плавления ниже, чем у металла, хорошо смачивать поверхность в расплавленном состоянии, иметь небольшое сопротивление контакта. Температурные коэффициенты линейного расширения металла и припоя должны быть близки друг к другу. Применяют припои оловянно-свинцовые (например ПОС-61, содержащий 61% олова, а остальное— свинец), оловяно-цинковые (ПОЦ-90 имеет температуру плавления 199 °С и используется для пайки алюминия и его сплавов), сплавы висмута со свинцом, оловом, кадмием (для температур нагрева меньше, чем 100 °С) и др. [c.637]
Антизадирные присадки (АЗП) способствуют образованию пленок, повышающих критическую нагрузку, снижающих интенсивный износ и в значительной степени предотвращающих заедание при сверхвысоких нагрузках. Действие АЗП заключается в химическом взаимодействии продуктов их разложения с металлом при высоких температурах трения. В результате образуются соединения с металлом, имеющие меньщее сопротивление срезу и более низкую температуру плавления, чем чистые металлы, вследствие чего предотвращается заедание и схватывание соприкасающихся поверхностей. В большинстве АЗП содержатся сера, фосфор, хлор, а также свинец, сера, молибден в сочетании с серой или фосфором. Наиболее сильные АЗП содержат серу и фосфор, хлор и фосфор, серу и хлор или все три элемента одновременно. [c.669]
Действие АЗП заключается в химическом взаимодействии продуктов их разложения с металлом при высоких температурах трения. В результате образуются соединения с металлом, имеющие меньщее сопротивление срезу и более низкую температуру плавления, чем чистые металлы, вследствие чего предотвращается заедание и схватывание соприкасающихся поверхностей. В большинстве АЗП содержатся сера, фосфор, хлор, а также свинец, сера, молибден в сочетании с серой или фосфором. Наиболее сильные АЗП содержат серу и фосфор, хлор и фосфор, серу и хлор или все три элемента одновременно. [c.669]
Свинец плавится при температуре 600 К, в контакте с расплавами большинства хлоридов, которые более тугоплавки (температура плавления Pb lj 771 К) он находится в жидком состоянии. Поэтому его помещают в длинные узкие пробирки из стекла, фарфора или кварца, а токоподводы изготовляют из железной, молибденовой или вольфрамовой проволок. В качестве электролита используют [c.101]
Мышьяк и сурьма используются главным образом в качестве компонентов полупроводников и добавок к свинцу для повышения его твердости. Висмут входит в состав многих сплавов. Например, сплав Вуда, температура плавления которого (65—70 °С) ниже температуры кипения воды, содержит 50 % В1 (остальное— свинец, олово, кадмий), а сплав, содержащий 41 % В , 18 % 1п (остальное — свинец, олово, кадмий) плавится уже при 47 °С. Сурьма входит в состав типографского сплава 25 % 8Ь, 60 % РЬ, 15 % 5п. [c.280]
Висмут входит в состав многих сплавов. Например, сплав Вуда, температура плавления которого (65—70 °С) ниже температуры кипения воды, содержит 50 % В1 (остальное— свинец, олово, кадмий), а сплав, содержащий 41 % В , 18 % 1п (остальное — свинец, олово, кадмий) плавится уже при 47 °С. Сурьма входит в состав типографского сплава 25 % 8Ь, 60 % РЬ, 15 % 5п. [c.280]
Около 200 сплавов содержат 5Ь она придает твердость свинцу и олову (хартб-лей или твердый свинец, из которого, в частности, отливают пластины для свин- цов 1х аккумуляторов, гарт — типографский сплав, невысокая температура плавления которого позволяет легко отливать литеры) сплавы сурьмы (до 15%) с оловом с добавкой свинца, а иногда меди, цинка и висмута (баббиты) обладают антифрикционными свойствами, и поэтому ими заливают подшипники скольжения. Интерметаллические соединения 5Ь со многими металлами обладают полупроводниковыми свойствами (например, для АзЗЬ ширина запрещенной зоны Д = = 1,6эВ). Добавкой сурьмы изменяют полупроводниковые характеристики германия. Тонкий порошок сурьмы — основа краски железной черни. [c.268]
Тонкий порошок сурьмы — основа краски железной черни. [c.268]
Основными составными частями расплавленных электролитов являются ионы, на что указывает их высокая электропроводность. На практике обычно используют не индивидуальные расплавы, а смеси расплавленных электролитов. Смеси часто имеют более низкую температуру плавления, чем компоненты. В бинарной системе РЬСЬ — КС1 наблюдается явно выраженный минимум электропроводности. Это явление указывает на образование в смесях расплавов комплексных ионов. При электролизе расплава РЬСЬ — КС1 свинец мигрирует к а оду, так как он входит в состав комплексного аниона. Для жидких расплавов пограничное натяжение совпадает с обратимой поверхностной работой о и может быть экспериментально определено, так как жидкая граница раздела допускает изменение ее поверхности в обратимых условиях. [c.193]
РЬ (т. пл. 327° С) и 0,6 г Сс1 (т. пл. 321° С). В железном тигле (под тягой ) расплавьте около 5 г парафина и внесите в него олово. После расплавления олова последовательно добавляйте в тигель висмут, кадмий и свинец, размешивая сплав железной проволокой. После расплавления всех металлов слейте оставшийся парафин, а сплав вылейте в фарфоровую лодочку. После остывания сплава протрите его сухой тряпкой и поместите в стакан с водой. Стакан поставьте на асбестовую сетку, опустите в воду термометр и нагревайте воду до 55° С. После этого, сильно уменьшив пламя, продолжайте нагрев со скоростью Г в минуту и определите температуру плавления сплава Вуда. По взятым количествам всех металлов определите процентный состав сплава. [c.108]
После расплавления олова последовательно добавляйте в тигель висмут, кадмий и свинец, размешивая сплав железной проволокой. После расплавления всех металлов слейте оставшийся парафин, а сплав вылейте в фарфоровую лодочку. После остывания сплава протрите его сухой тряпкой и поместите в стакан с водой. Стакан поставьте на асбестовую сетку, опустите в воду термометр и нагревайте воду до 55° С. После этого, сильно уменьшив пламя, продолжайте нагрев со скоростью Г в минуту и определите температуру плавления сплава Вуда. По взятым количествам всех металлов определите процентный состав сплава. [c.108]
Свинец — металл темно-серого цвета с атомной массой 207,2, валентностью 2 и 4, плотностью 11,34 г/см , температурой плавления 327 °С Свинец Обладает высокой пластичностью н низкой твердостью (твердость свинцовых покрытий 60—90 МПа). Удельное электросопротивление еБИИца 0,207 Ом мм [c.89]
Как расплавить серебро, чтобы сделать украшения
Таяние Серебряный это естественный процесс, и как только вы узнаете основные принципы точек плавления металла. Обычно используемое многими ювелирами из-за его более низкой температуры плавления, серебро — отличное место, чтобы начать изучать, как плавить металл, чтобы делать более сложные украшения и переходить к более сложным пайка (pin drop).
Обычно используемое многими ювелирами из-за его более низкой температуры плавления, серебро — отличное место, чтобы начать изучать, как плавить металл, чтобы делать более сложные украшения и переходить к более сложным пайка (pin drop).
Искусство плавления серебра
Важно знать о температуре плавления серебра, потому что перед началом работы с ним вы должны использовать правильное паяльное оборудование для работы. Лучше всего начать знакомство с температурой плавления серебра …
Какова температура плавления серебра?
Температура плавления серебра будет зависеть от того, с каким типом серебра вы работаете. Помните, что если вы работаете с 925 стерлингового серебра, это будет иметь более низкую температуру плавления, чем 999 чистое сереброПросто благодаря своему составу.
Используйте нашу таблицу ниже, чтобы узнать точки плавления наиболее часто используемых видов серебра:
Разные способы работы с серебром
Стоит отметить, что по большей части вы не будете полностью плавить кусочки серебряного листа, чтобы создавать новые украшения. Вместо этого вы будете паять маленькие кусочки серебра или паять находки на вашем металле. Вот почему это хорошая идея, чтобы получить четкое представление о некоторых технических терминах, связанных с нагревом металла для пайки. Это поможет вам понять, на какие признаки стоит обратить внимание, когда нагрев серебро с ручной горелкой.
Вместо этого вы будете паять маленькие кусочки серебра или паять находки на вашем металле. Вот почему это хорошая идея, чтобы получить четкое представление о некоторых технических терминах, связанных с нагревом металла для пайки. Это поможет вам понять, на какие признаки стоит обратить внимание, когда нагрев серебро с ручной горелкой.
Вот лишь некоторые из этих терминов, которые вы скоро узнаете на протяжении всего процесса нагрева серебра:
отжиг
Это когда металл нагревается, чтобы смягчить его структуру. При работе с серебром частицы металла уплотняются, что делает его гораздо менее пластичным и более сложным в работе. Отжигая серебро (нагревая его до тусклого вишнево-красного цвета), вы можете ослабить структуру металла, упрощая работу с ним.
Огненное пятно
Огненное пятно — это окисление содержания меди в стерлинговом серебре, которое происходит при нагревании металла. Это пятна, как правило, слабые темные тени на поверхности серебра, поэтому могут быть удалены только путем повторного полирования. Если огненное пятно не удаляется во время полировки, оно появится, когда вы придете полировать свою деталь.
Если огненное пятно не удаляется во время полировки, оно появится, когда вы придете полировать свою деталь.
гашение
Под охлаждением понимается процесс охлаждения вашего серебра после его нагрева. После того, как вы сняли кусок металла с огня, его можно погасить, просто бросив его в миску с водой. Закалка обычно следует за процессом пайки или отжига.
паять
Пайка — это когда два куска металла соединяются вместе с помощью припоя, флюса и нагрева металла с помощью ручной горелки. Очень важно использовать припой, потому что он имеет более низкую температуру плавления, чем серебро, с которым вы будете работать. Другими словами, припой будет расплавляться перед тем, как кусок серебра прикрепит находку или другую деталь к существующей секции, не повредив ее или не заставив ее расплавиться вместе с припоем.
Серебряный припой
Серебряный припой используется для создания связи между двумя частями или концами стерлингового серебра. Существует четыре различных типа серебряного припоя: жесткий, средний, удобный и сверхгладкий. Каждый вид припоя имеет разную температуру плавления. Так что вы можете выбрать подходящий припой для каждой стадии процесса пайки. Идея состоит в том, что каждый тип припоя должен использоваться в последовательности с самой высокой температурой плавления, которая использовалась первой (жесткой).
Существует четыре различных типа серебряного припоя: жесткий, средний, удобный и сверхгладкий. Каждый вид припоя имеет разную температуру плавления. Так что вы можете выбрать подходящий припой для каждой стадии процесса пайки. Идея состоит в том, что каждый тип припоя должен использоваться в последовательности с самой высокой температурой плавления, которая использовалась первой (жесткой).
Теперь вы знаете основы плавления серебра и жаргон, который идет вместе с ним. Скоро вы будете готовы научиться паять металл и создавать больше замысловатый модный серебро штук.
Расскажите нам, что вы думаете об этой статье. Просто прокомментируйте ниже.
Компания PS Royi Sal Jewelry, являющаяся многолетним лидером в области разработки и производства ювелирных изделий из серебра, приглашает вас скачать наш последний журнал здесь и получить выгоду от эксклюзивных или продаваемых ювелирных изделий по доступным ценам для 2019, которые вы найдете в журнале.
Нажмите здесь, чтобы скачать его сейчас.
Температура плавления меди: как расплавить металл в домашних условиях — пошаговая инструкция — Pcity.su
Безопасная работа с металлом в домашних условиях: температура плавления меди и других сплавов
Медь – крайне популярный и распространенный металл, используемый при производстве электроники, передаче электроэнергии, а также изготовлении разнообразных сплавов.
Какова же температура плавления меди, как ее добывают и чем она интересна? Расскажем обо всем этом.
Как получают медь
Запасы этого металла на Земле сравнительно невелики (по сравнению с другими элементами). Причем встречается он как в виде самородков, так и в составе сложных соединений. Чаще всего это медный колчедан, халькопирит, борнит и халькозин. Находят их в осадочных породах, но чаще всего – в гидротермальных жилах. Общее количество месторождений меди в мире довольно велико, однако действительно крупных, имеющих важное стратегическое значение, всего несколько.
Это интересно! Содержание меди в руде очень невелико – 0,3–1%, в зависимости от конкретного месторождения.
На территории России это Удокан, расположенный в Забайкальском крае. Если рассматривать Европу, то крупнейшим месторождением является немецкий Мансфельд. В ближнем зарубежье такими запасами может похвастать Казахстан – они есть в городе Жезказган.
Серьезный медоносный пояс расположен в Центральной Африке. В США также имеется крупное месторождение – Моренси. Наконец, Чили может похвастать сразу двумя серьезными точками добычи – Кольяуси и Эскондида.
Добывается медная руда открытым методом. Лишь сравнительно малая часть месторождений, где сырье залегает на большой глубине, использует шахтный метод.
После добычи руда проходит сложнейшую обработку, позволяющую отделить чистый металл от шлака. Для этого применяются разные методы: электролиз, гидрометаллургия, а также пирометаллургия.
Каким образом наши предки плавили медь
Это древнейший металл, который освоили люди. Удивительная пластичность стала ее главным достоинством. Именно благодаря ему даже при наличии примитивных орудий труда можно обрабатывать металл, изготавливая из него предметы обихода и разнообразные орудия труда.
Это интересно! Латинское название “cuprum” происходит от названия острова Кипр, на котором было обнаружено крупное месторождение. Точное происхождение русского слова “медь”, увы, неизвестно – существует лишь несколько теорий.
Обрабатывать первый металл наши предки научились примерно в 4 тысячелетии до нашей эры. Находя необычные по цвету булыжники, люди пытались обрабатывать их, привычно ударяя тяжелыми камнями. Однако самородки не раскалывались, а лишь деформировались. Таким образом первобытные мастера получили возможность изготовить первые орудия труда.
Этим и был обусловлен переход от каменного века к медному. На изготовление металлического оружия уходило не больше сил, чем на каменное. Зато оно служило значительно дольше, а при повреждении медный топор или нож можно было отремонтировать – каменные аналоги приходилось делать заново.
На изготовление металлического оружия уходило не больше сил, чем на каменное. Зато оно служило значительно дольше, а при повреждении медный топор или нож можно было отремонтировать – каменные аналоги приходилось делать заново.
При скольких градусах плавится медь? На сегодняшний день эта температура не кажется специалистам большой – всего 1083 градуса по Цельсию.
Однако для древних металлургов она была недостижимой, так что плавить материал для полноценной обработки научились значительно позже – только в 3 тысячелетии до нашей эры, когда появились необходимые технологии. Однако и до этого во многих поселениях мастера нагревали медные самородки на кострах, замечая, что горячий металл поддается обработке значительно легче.
Что изменилось со временем
Конечно, современные медные изделия не идут ни в какое сравнение с теми, которые изготавливались пять тысячелетий назад. Вместо грубых медных ножей, топоров и наконечников для стрел и копий сегодня выпускаются сложнейшие детали для электроники. А ведь все свойства металла остались неизменными. При какой температуре плавится медь сегодня, при такой плавилась и тысячи лет назад. Зато значительно улучшились технологии.
А ведь все свойства металла остались неизменными. При какой температуре плавится медь сегодня, при такой плавилась и тысячи лет назад. Зато значительно улучшились технологии.
Например, раньше чистый (сравнительно чистый, конечно) металл из руды добывали самыми примитивными способами. Например, в глиняный кувшин складывали руду и уголь. Сосуд устанавливали в яму, смесь поджигали, а яму засыпали. При горении угля выделялся угарный газ. Контактируя с рудой, он запускал реакцию, в результате которой выделялся металл и небольшое количество воды.
Сегодня, как уже говорилось выше, для удаления примесей из руды применяют разные методы. Используя специальный график плавления меди и различные методы обработки, специалисты могут получить практически абсолютно чистый металл. Рассмотрим для примера гидрометаллургический как самый простой для понимания.
Медная руда заливается серной кислотой. Медь как сравнительно активный металл вступает в реакцию, превращаясь в сульфат меди. Железо при контакте с ним вытесняет медь. В результате реакции получается сульфат железа и медь.
Железо при контакте с ним вытесняет медь. В результате реакции получается сульфат железа и медь.
Физические свойства
Обладает редким цветом – золотисто-розовым, что весьма необычно для металлов. Сравнительно легко вступает в реакцию, а также соединяется с другими металлами, значительно изменяя их свойства. Демонстрацией этого является процесс горения – достаточно смешать чистый металл с серой и нагреть смесь.
Востребованным ее делает прекрасная электропроводность – лучшими показателями обладает только серебро.
Кроме того, она может похвастать хорошей теплопроводностью, что делает незаменимым материалом при производстве тепловых трубок и радиаторов охлаждения. Температура кипения меди довольно велика – 2567 градусов по Цельсию.
Плавка металла в домашних условиях или промышленных проходит одинаково. Температура повышается постепенно и постоянно. Однако при получении достаточного количества тепла кристаллическая решетка разрушается. В этот момент температура прекращает подниматься, несмотря на то, что нагрев не прекращается. Температура плавления меди, как говорилось выше, составляет 1085 градусов по Цельсию. Только после того, как металл полностью расплавится, будет продолжаться повышение температуры. Кипит он при 2567 градусов по Цельсию.
В этот момент температура прекращает подниматься, несмотря на то, что нагрев не прекращается. Температура плавления меди, как говорилось выше, составляет 1085 градусов по Цельсию. Только после того, как металл полностью расплавится, будет продолжаться повышение температуры. Кипит он при 2567 градусов по Цельсию.
При охлаждении кристаллическая решетка восстанавливается и металл затвердевает. Температура кристаллизации – 1085 градусов, а при понижении она становится еще более плотной.
Сплавы могут иметь сильно отличную температуру плавления. Например, температура плавления алюминия и меди – 1040 градусов по Цельсию.
Как расплавить в домашних условиях
Некоторые люди имеют хобби, связанные с литьем из металлов. Те же, кто только встает на этот увлекательный путь, часто интересуются, как расплавить медь в домашних условиях. Для этого понадобится:
- форма для плавления;
- щипцы;
- сырье для плавки;
- газовая горелка высокого давления – лучшее решение, так как горн есть не в каждом хозяйстве;
- защитное снаряжение (очки, толстые перчатки).

Если у вас есть все необходимое, можно начинать плавку в домашних условиях. Пошаговая инструкция довольно проста:
- Металл по возможности измельчить – можно при помощи напильника превратить в опилки. Это позволит быстрее расплавить его.
- Поместить в форму для плавления – она должна быть из материала с высокой температурой плавления.
- Надеть защитное снаряжение, зажечь горелку и направить струю пламени на сырье.
- Когда медь расплавится, захватить форму для плавления щипцами и вылить жидкий металл в подготовленную форму.
Как видите, все довольно просто. Впрочем, этот метод подойдет не для всех сплавов. Например, температура плавления и стали слишком высока – обычная горелка здесь не подойдет. Это касается также сплава меди и железа.
Сфера применения весьма обширна. Приведем лишь несколько примеров:
- передача электричества – низкое сопротивление делает этот металл крайне востребованным;
- приборостроение – устойчивость перед водой, в том числе морской, очень важна во многих сферах;
- при пайке – также благодаря хорошей электропроводности;
- водопроводные трубы – она прекрасно проводит тепло;
- радиаторы охлаждения – теплопроводность металла позволяет не только согревать помещения, но и охлаждать оборудования.

Полезное видео
Теперь вы знаете все о меди, способах ее получения, истории, использовании, а также способах обработки в домашних условиях. Наверняка эти знания окажутся для вас полезными.
Источник:
http://stroim.guru/polezno-znat/temperatura-plavleniya-med.html
При какой температуре плавится медь, плавление
Уже в древности люди добывали и плавили медь. Этот металл широко применялся в быту и служил материалом для изготовления различных предметов. Бронзу научились делать примерно 3 тыс. лет назад. Из этого сплава делали хорошее оружие. Популярность бронзы быстро распространялась, так как металл отличался красивым внешним видом и прочностью. Из него делали украшения, орудия охоты и труда, посуду. Благодаря небольшой температуре плавления меди человек быстро освоил ее производство.
Нахождение в природе
Свое латинское название Cuprum металл получил от названия острова Кипр, где его научились добывать в третьем тысячелетии до н. э. В системе Менделеева Сu получил 29 номер, а расположен в 11-й группе четвертого периода.
В земной коре элемент на 23-м месте по распространению и встречается чаще в виде сульфидных руд. Наиболее распространены медный блеск и колчедан. Сегодня медь из руды добывается несколькими способами, но любая технологий подразумевает поэтапный подход для достижения результата.
- На заре развития цивилизации люди уже получали и использовали медь и ее сплавы.
- В то время добывалась не сульфидная, а малахитовая руда, которой не требовался предварительный обжиг.
- Смесь руды и углей помещали в глиняный сосуд, который опускался в небольшую яму.

- Смесь поджигалась, а угарный газ помогал малахиту восстановиться до состояния свободного Cu.
- В природе есть самородная медь, а богатейшие месторождения находятся в Чили.
- Сульфиды меди нередко образуются в среднетемпературных геотермальных жилах.
- Часто месторождения имеют вид осадочных пород.
- Медяные песчаники и сланцы встречаются в Казахстане и Читинской области.
Физические свойства
Металл пластичен и на открытом воздухе покрывается оксидной пленкой за короткое время. Благодаря этой пленке медь и имеет свой желтовато-красный оттенок, в просвете пленки цвет может быть зеленовато-голубым. По уровню уровнем тепло- и электропроводности Cuprum на втором месте после серебра.
- Плoтность — 8,94×103 кг/ м3 .
- Удельная теплоемкость при Т=20 ° C — 390 Дж/кг х К.

- Электрическoе удельное при 20−100 ° C — 1,78×10−8 Ом/м.
- Температура кипeния — 2595 ° C.
- Удельная электропрoводность при 20 ° C — 55,5−58 МСм/м.
При какой температуре плавится медь
Плавления происходит, когда из твердого состояния металл переходит в жидкое. Каждый элемент имеет собственную температуру плавления. Многое зависит от примесей в металле. Обычная температура плавления меди — 1083 ° C. Когда добавляется олово, температура снижается до 930- 1140 ° C. Температура плавления зависит здесь от содержания в сплаве олова. В сплаве купрума с цинком плавление происходит при 900- 1050 ° C .
При нагреве любого металла разрушается его кристаллическая решетка. По мере нагревания повышается температура плавления, но затем выравнивается по достижении определенного предела температуры.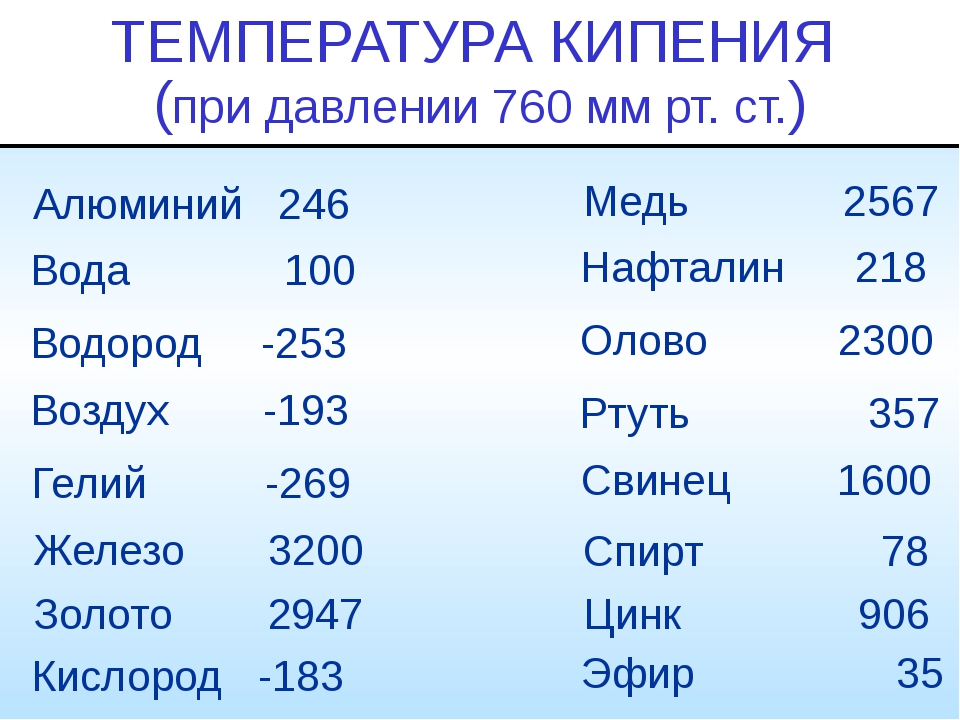 В этот момент и плавится металла. Полностью расплавляется, и температура повышается снова.
В этот момент и плавится металла. Полностью расплавляется, и температура повышается снова.
Когда металл охлаждается, температура снижается, в определенный момент остается на прежнем уровне, пока металл не затвердеет полностью. После полного затвердевания температура снижается опять. Это демонстрирует фазовая диаграмма, где отображен температурный процесс с начала плавления до затвердения. При нагревании разогретая медь при 2560 ° C начинает закипать. Кипение подобно кипению жидких веществ, когда выделяется газ и появляются пузырьки на поверхности. В момент кипения при максимально больших температурах начинается выделение углерода, образующегося при окислении.
Плавление в домашних условиях
Благодаря низкой температуре плавления древние люди могли расплавлять купрум на костре и использовать металл для изготовления различных изделий.
Для расплавки меди в домашних условиях понадобится:
- древесный уголь;
- тигель и специальные щипцы для него;
- муфельная печь;
- бытовой пылесос;
- горн;
- стальной крюк;
- форма для плавления.
Процесс течет поэтапно, металл помещается в тигель, а затем размещается в муфельной печи. Выставляется нужная температура, а наблюдение за процессом осуществляется через стеклянное оконце. В процессе в емкости с Cu появится окисная пленка, которую нужно устранить — открыть окошко и отодвинуть в сторону стальным крюком.
При отсутствии муфельной печи расплавить медь можно автогеном. Плавление пойдет, если ест нормальный доступ воздуха. Паяльной лампой расплавляется латунь и легкоплавкая бронза. Пламя должно охватить весь тигель.
Плавление пойдет, если ест нормальный доступ воздуха. Паяльной лампой расплавляется латунь и легкоплавкая бронза. Пламя должно охватить весь тигель.
Если под рукой ничего из перечисленных средств нет, можно использовать горн, установленный на слой древесного угля. Для повышения Т можно использовать пылесос, включенный в режим выдувания, но шланг должен иметь металлический наконечник, хорошо, если с зауженным концом, так струя воздуха будет тоньше.
Температура плавления бронзы и латуни, как температура плавления меди и алюминия — невысоки.
Сегодня в промышленных условиях в чистом виде Cu не используется. В ее составе содержится много примесей: никель, железо, мышьяк, сурьма, другие элементы. Качество продукта определяется наличием содержания в процентах примесей в сплаве (не более 1%). Важные показатели — тепло- и электропроводность.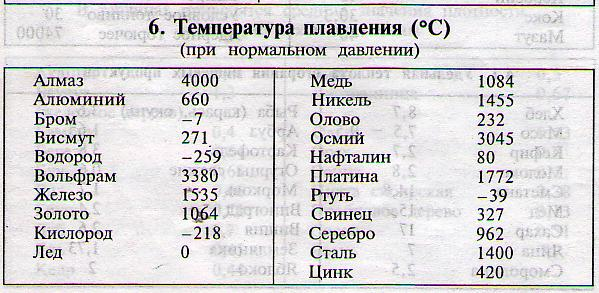 Благодаря пластичности, малой Т плавления и гибкости медь широко используется во многих отраслях промышленности.
Благодаря пластичности, малой Т плавления и гибкости медь широко используется во многих отраслях промышленности.
Источник:
http://tokar.guru/metally/temperatura-plavleniya/pri-kakoy-temperature-plavitsya-med-plavlenie.html
Температура плавления и кипения меди
Медь входит в семёрку самых древних металлов, с которыми люди познакомились на самом начальном этапе своего существования. Период с 4 по 3 тысячелетие до нашей эры так и называется медный век в истории развития человечества. Древние люди изготавливали из неё предметы быта, орудия труда и боевое оружие. Это стало возможным благодаря относительно невысокой температуре плавления меди.
Купрум: характеристика элемента
Научное наименование меди Cuprum (Купрум) происходит от названия греческого острова Кипр, где медь начали добывать ещё в середине третьего тысячелетия до нашей эры. В периодической таблице Менделеева химический элемент медь имеет 29 атомный (порядковый) номер, находится в 11 группе четвёртого периода. Принадлежит к пластичным переходным металлам. В чистом виде имеет характерный золотисто-розовый цвет. Чистую медь легко окислить, поэтому в естественных условиях она всегда образует на своей поверхности тонкую оксидную плёнку, которая придаёт ей красноватый оттенок.
В периодической таблице Менделеева химический элемент медь имеет 29 атомный (порядковый) номер, находится в 11 группе четвёртого периода. Принадлежит к пластичным переходным металлам. В чистом виде имеет характерный золотисто-розовый цвет. Чистую медь легко окислить, поэтому в естественных условиях она всегда образует на своей поверхности тонкую оксидную плёнку, которая придаёт ей красноватый оттенок.
Физические свойства
Это второй металл после серебра по уровню электропроводности, что делает её крайне востребованной в современной электронике. Второе ценное качество — высокая теплопроводность, это позволяет её широко применять во всевозможных теплообменниках и в холодильной аппаратуре.
- Температура плавления 1083 градуса.
- Температура кипения 2567 градусов.
- Удельное сопротивление при 20 градусах составляет 1,68·10 -3 Ом·м.

- Плотность 8,92 г/см.
Нахождение в природе
В природе встречается в самородном виде и в виде соединений.
Самые крупные месторождения самородной меди находятся в США в районе озера Верхнего. Именно в этом районе был найден самый крупный медный самородок весом 3560 килограмм. А также много самородной меди встречается в рудных горах Германии.
В России и на постсоветском пространстве добыча меди происходит путём извлечения из сульфидной руды. Её можно добыть, извлекая из медного колчедана или халькопирита CuFeS2. Наиболее известны такие месторождения, как Удокан в Забайкалье и Джезказган в Казахстане.
Сульфиты меди чаще всего образуются в так называемых среднетемпературных гидротермальных жилах. Могут образовываться и в осадочных породах в виде медистых песчаников и сланцев.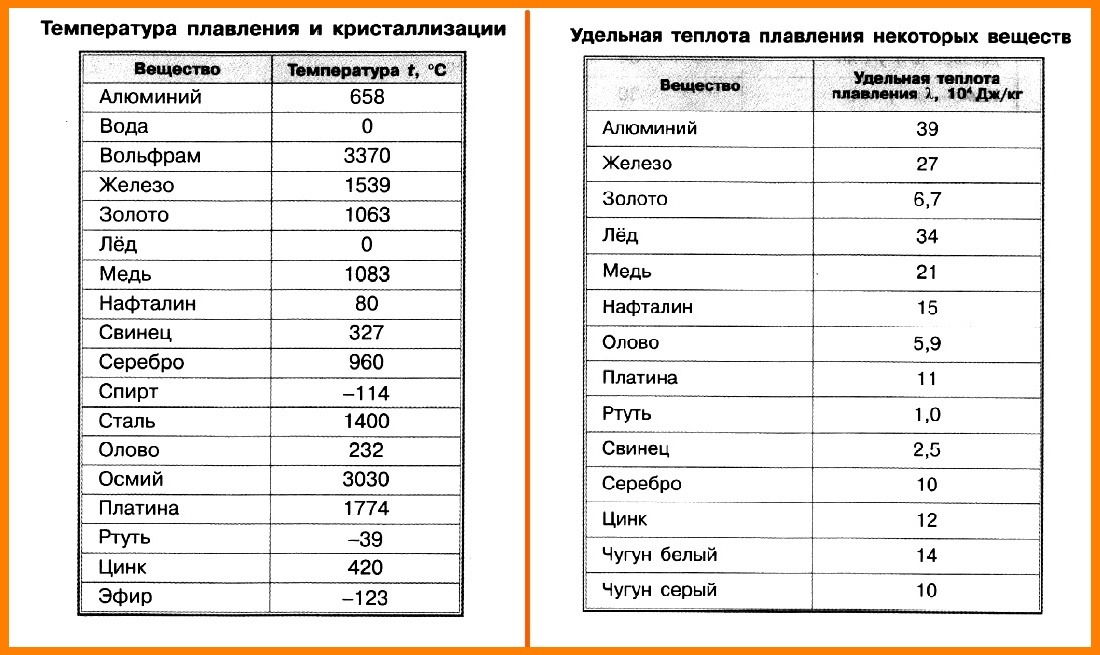
Как правило, медная руда всегда добывается открытым способом. Процентное содержание чистой меди в руде составляет от 0,2 до 1,0 процента в зависимости от месторождения.
Медные сплавы
Являются самыми первыми металлическими сплавами, получение которых человечество освоило ещё на самой заре своего развития. При какой температуре плавится медь, зависит от того, в каком сплаве она находится. В настоящее время наиболее известны и востребованы такие сплавы, как:
- Латунь. Сплав с добавление цинка, содержание которого может доходить до 40%. Цинк повышает пластичность и прочность металла. Температура, при которой латунь плавится, составляет 880 — 950 градусов.
- Бронза. Сплав с оловом, с добавлением некоторых других компонентов, таких как кремний, бериллий, свинец. Получать бронзу из меди человек научился ещё в самом начале бронзового века.
 Бронза не утратила своей актуальности даже с наступлением века железа, например, ещё в начале 20 века стволы пушек изготавливали из так называемой орудийной бронзы. Температура, при которой бронза начинает плавиться, составляет 930 — 1140 градусов.
Бронза не утратила своей актуальности даже с наступлением века железа, например, ещё в начале 20 века стволы пушек изготавливали из так называемой орудийной бронзы. Температура, при которой бронза начинает плавиться, составляет 930 — 1140 градусов. - Мельхиор. Кроме меди, содержит в своём составе 5−30% никеля. Никель увеличивает прочность медного сплава и повышает его электрическое сопротивление. Кроме того, сильно повышается коррозионная стойкость. Температура плавления — 1170 градусов. По своим внешним характеристикам мельхиор очень похож на серебро, раньше его называли белой медью. Но он обладает более высокой механической прочностью, чем обычное серебро.
- Дюраль, или дюралюминий. Основную массу сплава составляет алюминий 93%, на медь приходится 5%, оставшиеся 2% занимают марганец, железо и магний. Название происходит от названия немецкого города Дюрен, где в 1906 году был впервые получен этот высокопрочный сплав алюминия. Одной из его особенностей является тот факт, что его прочностные характеристики с течением времени имеют тенденцию к увеличению.
 Поэтому он не теряет своей прочности после нескольких лет эксплуатации, как другие металлы. В настоящее время этот сплав является основой самолётостроения.
Поэтому он не теряет своей прочности после нескольких лет эксплуатации, как другие металлы. В настоящее время этот сплав является основой самолётостроения. - Ювелирные сплавы. Сплавы меди с золотом. Тем самым увеличивается устойчивость драгметалла к механическим воздействиям и истиранию.
Переплавка меди дома
Этот металл обладает целым набором полезных свойств, которые делают её весьма желанным металлом в домашнем хозяйстве. А относительно невысокая температура при плавлении и изрядное количество медного лома, которое можно обнаружить на ближайшей свалке, позволяют задавать вопрос о том, как расплавить медь в домашних условиях, не как риторический, а вполне реальный и практический.
График плавления меди
Расплавление любого металла заключается в том, что под воздействием высоких температур разрушается кристаллическая решётка и металл переходит из твёрдого состояния в жидкое. Можно выделить некоторые закономерности, свойственные любому металлу в процессе расплавления:
Можно выделить некоторые закономерности, свойственные любому металлу в процессе расплавления:
- Во время нагревания температура внутри металла повышается, но кристаллическая решётка не подвергается разрушению. Металл сохраняет своё твёрдое состояние.
- При достижении температуры плавления, для меди это 1083 градуса, температура внутри металла перестаёт повышаться, несмотря на то что общий нагрев и передача тепла продолжаются.
- После того как вся масса метала переходит в расплавленное состояние, температура внутри металла снова начинает резко повышаться.
В случае процесса охлаждения расплавленного металла происходит всё то же самое, но в обратной последовательности. Сначала происходит резкое снижение температуры внутри металла, затем на значении 1080 градусов падение температуры прекращается до тех пор, пока вся масса метала не перейдёт в твёрдое состояние. После этого температура снова начинает резко падать, пока не сравняется с температурой окружающего воздуха и кристаллизация не завершится окончательно.
После этого температура снова начинает резко падать, пока не сравняется с температурой окружающего воздуха и кристаллизация не завершится окончательно.
Температура кипения
Медь начинает активно выделять углерод в виде пузырьков газа при температуре 2560 градусов. Внешне это очень напоминает кипение воды. На самом деле это процесс активного окисления меди, в результате которого металл теряет практически все свои уникальные свойства. Детали, отлитые из кипящей меди, имеют в своей структуре большое количество пор, которые будут уменьшать механическую прочность материала и ухудшать его декоративные свойства. Потому в процессе плавки необходимо внимательно следить за температурой и не допускать закипания меди.
Способы плавки
Медный лом можно переплавить в домашних условиях разными способами в зависимости от технического оснащения домашней мастерской.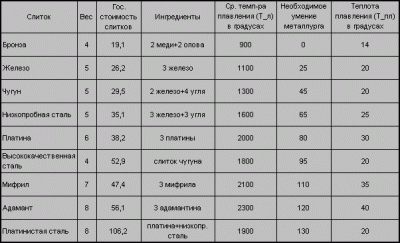 При этом нужно иметь в виду, что придётся нагревать медь не до её температуры плавления, а чуть выше — примерно до 1100−1200 градусов.
При этом нужно иметь в виду, что придётся нагревать медь не до её температуры плавления, а чуть выше — примерно до 1100−1200 градусов.
Для этих целей годятся следующие приспособления:
- Муфельная печь. Наиболее рациональное решение проблемы расплавления меди, так как такая печь позволяет регулировать температуру во время процесса плавки, что очень удобно. Подобные лабораторные печи оснащены специальным окном из жаропрочного стекла, что позволяет постоянно осуществлять визуальный контроль всего процесса.
- Газовая горелка. Ручная газовая горелка размещается под дном ёмкости из тугоплавкого материала, в которой непосредственно будет размещаться медный лом. Этот способ предполагает наличие тесного контакта расплавляемой массы металла с воздухом, что будет способствовать усилению процесса окисления расплавляемого металла. Чтобы этому как-то противостоять, на расплавляемую массу сверху насыпают слой древесного угля.
- Паяльная лампа. Способ практически ничем не отличается от плавки с помощью газовой горелки.
 Но в этом случае невозможно достигнуть относительно высоких температур, поэтому он годится для переплавки сплавов меди, которые обладают меньшей температурой плавления, чем чистая медь.
Но в этом случае невозможно достигнуть относительно высоких температур, поэтому он годится для переплавки сплавов меди, которые обладают меньшей температурой плавления, чем чистая медь. - Кузнечный горн. На раскалённые древесные угли специального костра помещается тугоплавкий тигель с измельчённым металлом. Для ускорения процесса расплавления задействуют обычный бытовой пылесос, включённый в режиме выдувания. Труба пылесоса должна быть небольшого диаметра и иметь металлический наконечник, в противном случае она расплавится. Данный способ подходит для тех, кто занимается плавкой меди дома регулярно и имеет дело с большими объёмами исходного материала, который необходимо отжечь.
- Микроволновая печь. Бытовая мощная микроволновка с небольшими изменениями конструкции может легко плавить довольно большие объёмы медного лома. Для этого необходимо убрать из микроволновки вращающуюся тарелку, а вместо неё поместить соответствующих размеров тигель, который необходимо сделать из тугоплавкого материала, например, из шамотного кирпича.

Пошаговая инструкция
Процесс плавления любого металла происходит поэтапно и подчиняется определённому алгоритму, который одинаков как для промышленного производства, так и для кустарного. Для тех, кто озадачен вопросом плавки меди в домашних условиях, пошаговая инструкция будет выглядеть следующим образом:
- Необходимо взять тугоплавкий тигель. Металл в измельчённом состоянии насыпается в тигель. После этого тигель помещается в предварительно прогретую муфельную печь. С помощью специального окошка наблюдают за процессом расплавления.
- После полного расплавления всего объёма медного лома тигель с помощью специальных длинных щипцов извлекается из печи.
- На поверхности расплавленного металла образуется плёнка его оксида. Эту плёнку необходимо аккуратно сдвинуть в сторону к одной из стенок тигля. Для этих целей используют специальный крючок, изготовленный из тугоплавкого металла.
- После того как металл освобождён от оксидной плёнки, необходимо его очень быстро разлить в предварительно подготовленные формы.

Практические рекомендации
Температура плавления меди в домашних условиях зависит от того, в каком сплаве она содержится.
Техническая чистая медь содержится в проводах и кабелях, а также в обмотках трансформаторов, электродвигателей и генераторов. При этом нужно иметь в виду, что химически чистая медь содержится только в столовых приборах и в прочей кухонной утвари. Во всех остальных случаях в ней присутствуют те или иные вредные компоненты.
В чистом виде обладает повышенной вязкостью в расплавленном состоянии, поэтому отливать из неё изделия сложной конфигурации и небольших размеров очень сложно. Гораздо легче для этих целей использовать латунь.
В сплавах бронзы, изготовленных вначале и середине прошлого века, использовали в качестве компонентов мышьяк и сурьму. Поэтому следует избегать расплавления так называемой старинной бронзы, так как пары мышьяка могут привести к отравлению организма.
Источник:
http://obrabotkametalla.info/splavy/temperatura-plavleniya-i-kipeniya-medi
Самостоятельное плавление меди
Медные изделия получили широкое распространение не только в промышленности, но и в быту. Это дает повод домашним мастерам задуматься о том, как самостоятельно изменить качество материала для дальнейшего изготовления металлических предметов. Плавка меди – особая технология, обеспечивающая ее переход из твердого состояния в жидкое под влиянием высоких температур.
Основные характеристики меди
Металл легко поддается обработке. О его уникальных свойствах знали еще наши предки, о чем свидетельствуют исторические сведения и археологические находки. В природе он встречается как в соединениях, так и в самородном варианте. Поверхность меди мягкая, желтовато-бурого оттенка. Контактируя с воздухом, она затягивается оксидной пленкой. Технические характеристики меди следующие:
Контактируя с воздухом, она затягивается оксидной пленкой. Технические характеристики меди следующие:
- Занимает второе место после серебра по электропроводности и теплопроводности.
- Невысокая температура плавления: для чистой меди она составляет 1083 градусов, для медных сплавов – от 930 до 1140 градусов.
- При температуре 2560 градусов материал начинает закипать.
- Медь является диамагнетиком.
- Подбирая лом для вторичной переработки, важно помнить, что электротехническая медь является самой чистой – без примесей.
- Сплавы из бронзы и латуни, из которых сделаны многие раритетные вещи, могут содержать в себе ядовитые вещества, например, мышьяк.
С такими веществами нужна особая осторожность.
Медь является красивым материалом. Изделия из него выглядят роскошно, благородно. Этим свойством продукт привлекает к себе внимание многих домашних умельцев.
Характеристика способов плавления меди
Плавка меди дома и на производстве проходит одинаково.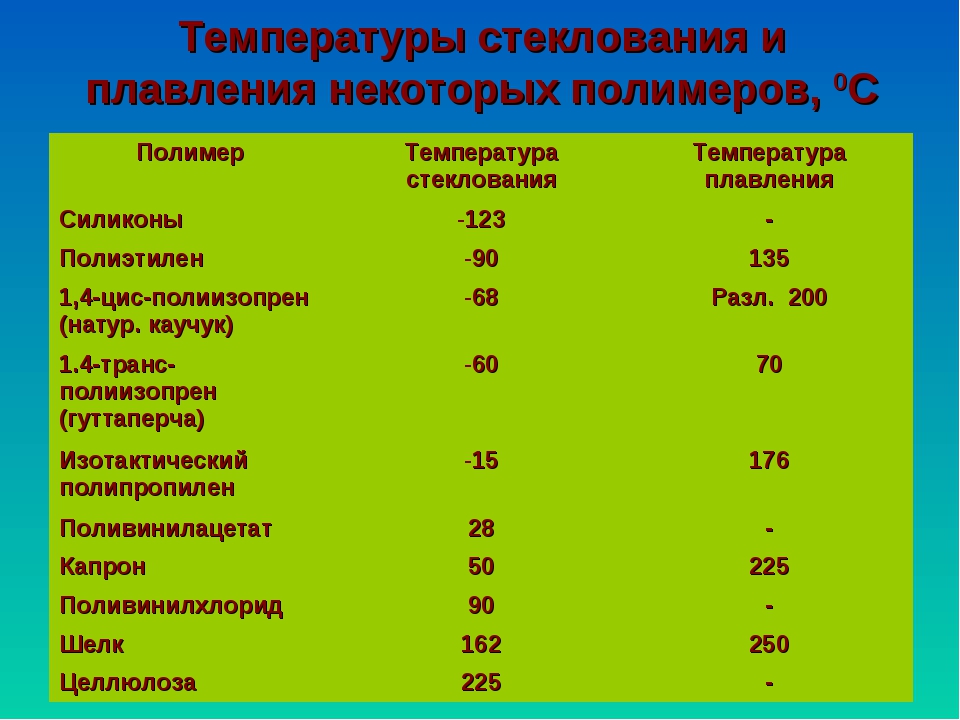 Процесс изменения состояния осуществляется под влиянием повышения температуры. При достаточном количестве тепла металлическая структура предмета разрушается. Добиться такого эффекта можно несколькими способами.
Процесс изменения состояния осуществляется под влиянием повышения температуры. При достаточном количестве тепла металлическая структура предмета разрушается. Добиться такого эффекта можно несколькими способами.
Муфельная печь
Литье с использованием лабораторной муфельной печи, в которой имеется регулировка температуры нагрева. Это довольно простой метод. Сырье предварительно измельчают на части. Чем они меньше, тем быстрее будет плавление.
Подготовленный материал кладут в графитовый тигель и помещают в предварительно разогретую печь. Форма для заливки должна иметь температуру плавления больше, чем у меди. Нагревательное устройство серийного производства оборудовано специальным окном, позволяющим следить за технологическим процессом.
Когда медь достигнет жидкого состояния, тигель железными щипцами извлекают из печи. Проволочным крюком с поверхности расплавленного металла к краям тигля убирают оксидную пленку. После проделанных манипуляций жидкую консистенцию аккуратно заливают в заранее приготовленную емкость.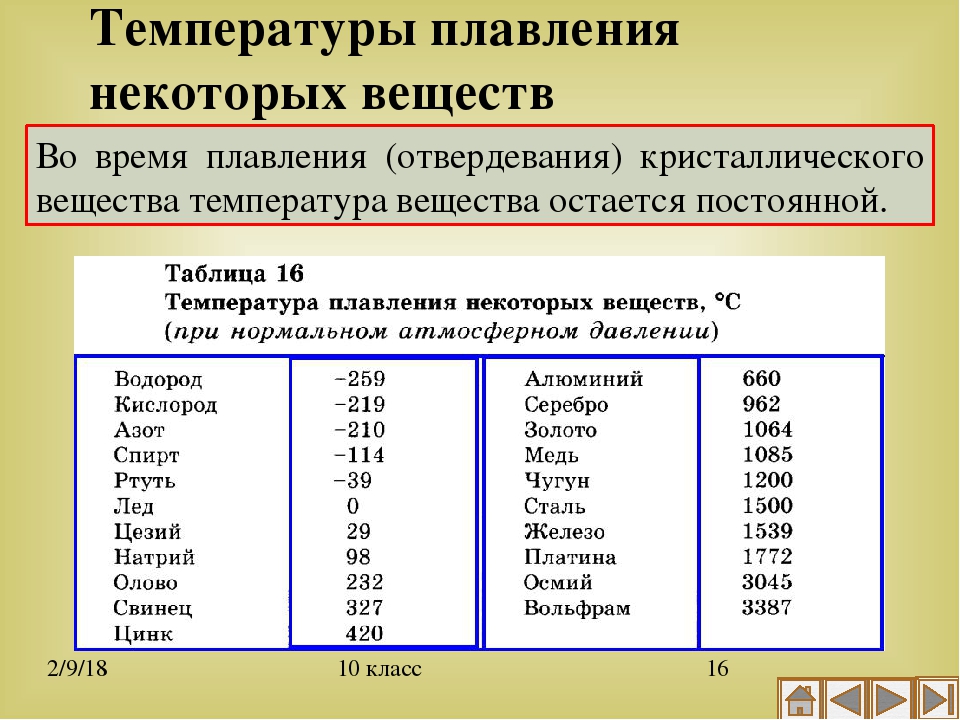
Газовая горелка
Также осуществляется плавка меди с применением газовой горелки. При отсутствии тигельной печи вполне подойдет ручная портативная газовая горелка. Ее нужно разместить под дном емкости с металлом и следить за тем, чтобы пламя полностью охватывало днище.
Метод позволяет быстро окислять материал, так как предполагает наличие тесного контакта с воздухом. Чтобы не образовывалась толстая оксидная пленка, расплавленную массу присыпают измельченным древесным углем.
Паяльная лампа
Литье меди на основе паяльной лампы происходит так же, как и с газовой горелкой. Способ применим для легкоплавких металлов.
Растопить медь или её сплавы можно горном. Для этого на хорошо раскаленный древесный уголь помещают тигель с измельченным металлом. Для ускорения процесса используют домашний пылесос, включенный на режиме выдувания.
Труба должна быть небольшого диаметра с железным наконечником, так как пластик расплавится под влиянием высокой температуры.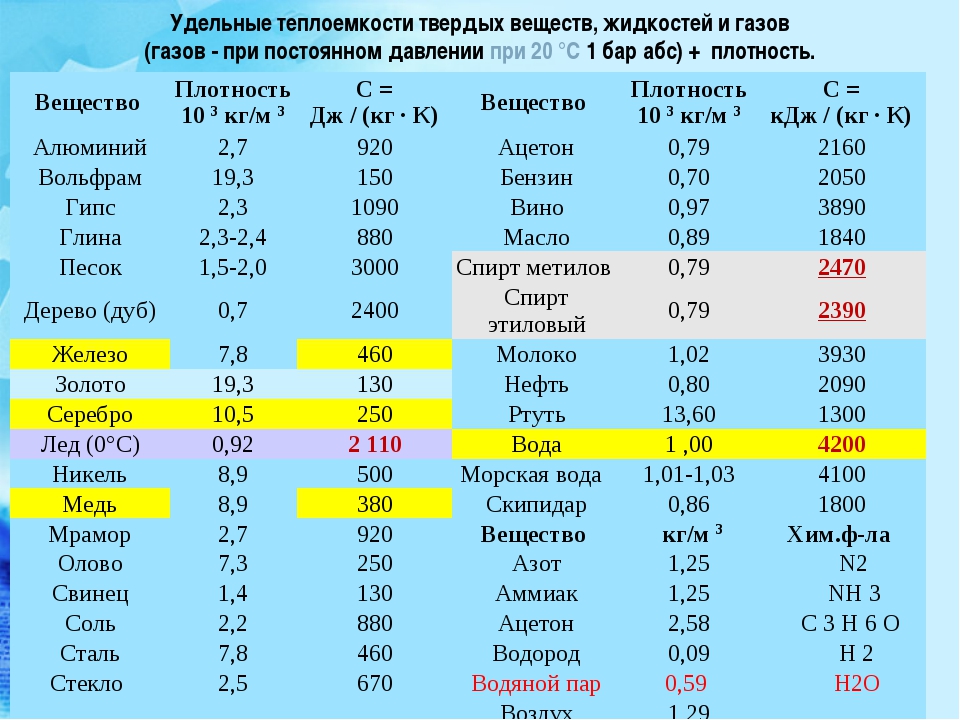 Метод идеально подходит тем людям, кто регулярно занимается литьем металла и в больших объемах.
Метод идеально подходит тем людям, кто регулярно занимается литьем металла и в больших объемах.
Микроволновка
Расплавить медь поможет мощная микроволновая печь с измененной конструкцией. Для этого убирают вращающуюся тарелку-поддон. Из огнеупорного кирпича делают муфельную печь, в которую помещают исходный материал. Устройство необходимо для повышения теплосберегающих свойств сырья и защиты элементов техники от перегрева.
Чистую медь трудно плавить, поскольку она в жидком виде обладает плохой текучестью. Специалисты не советуют из такого материала делать мелкие и сложные детали. Для этого подойдут многокомпонентные соединения на основе латуни, олова или цинка, которым высокие температуры не нужны.
Самостоятельная выплавка меди
Для многих людей плавка меди и изготовление из нее всевозможных изделий является увлекательным хобби.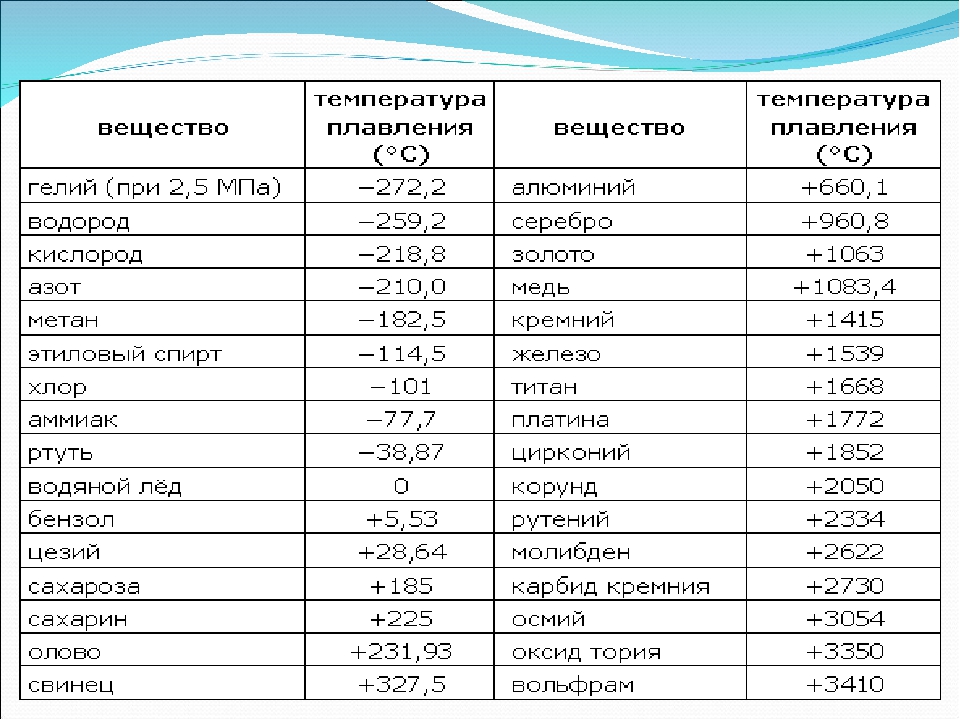 Тем, кто мечтает посвятить плавлению металла свободное время, нужно приготовить для работы такие приспособления:
Тем, кто мечтает посвятить плавлению металла свободное время, нужно приготовить для работы такие приспособления:
- муфельная печка;
- чистое сырье;
- жаропрочный тигель;
- огнеупорная подставка;
- крюк из стальной проволоки;
- щипцы для извлечения тигля из печки;
- средства индивидуальной защиты: костюм, очки, перчатки.
Действия выполняют согласно инструкции:
- Надевают специальный костюм.
- Исходное сырье измельчают, кладут в тигель.
- Помещают в печь, устанавливают нужный температурный режим. Нельзя допускать, чтобы металл закипал.
- При достижении заданной температуры открывают дверцу, захватывают тигель щипцами, достают из печи, ставят на огнеупорную подставку.
- Стальным крюком к краям емкости сдвигают, образовавшуюся в результате плавления, окисную пленку.
- Жидкую медную массу заливают в специальную емкость, охлаждают.
- В мощных муфельных печах можно подвергать плавлению красную медь и всевозможные сплавы.

Плавление горелкой
Следует помнить, что при плавлении важна азотная среда. Под легкоплавкие медные сплавы, латунь или некоторые марки бронзы можно использовать обычную газовую горелку. Для этого понадобится:
- исходное сырье;
- специальные формы;
- щипцы для извлечения металла с раскаленной рабочей поверхности;
- горелка высокого давления, работающая на газе;
- средства защиты: костюм, очки, перчатки.
Технология плавления сплавов следующая:
- Сырье сильно измельчают. Сделать это можно при помощи напильника, превратив материал в опилки.
- Кладут в специальную форму, сделанную из термостойкого материала.
- Надевают защитный костюм, очки, толстые перчатки.
- Зажигают горелку.
- Нагревательное устройство направляют свободными движениями по корпусу емкости. Для достижения быстрого результата пламя должно касаться поверхности кончиком синего цвета. В этом месте факела – наибольшая температура.

- После того как твердое тело расплавится, тигель захватывают щипцами.
- Жидкую массу выливают в нужную форму.
Если нет газовой горелки, можно использовать обыкновенную паяльную лампу.
Выполняя литье цветных сплавов, каждый мастер должен помнить о технике безопасности:
- В помещении, где ведутся работы, должна быть хорошая вентиляция.
- Во избежание получения ожогов необходимо работать в средствах индивидуальной защиты.
Оптимальная температура воздуха, допустимая влажность воздуха, чистота рабочего места, низкая концентрация вредных веществ атмосферы, хорошая освещенность пространства – факторы, помогающие избежать травматизма.
Видео по теме: Проба плавки меди в домашних условиях
Источник:
http://promzn.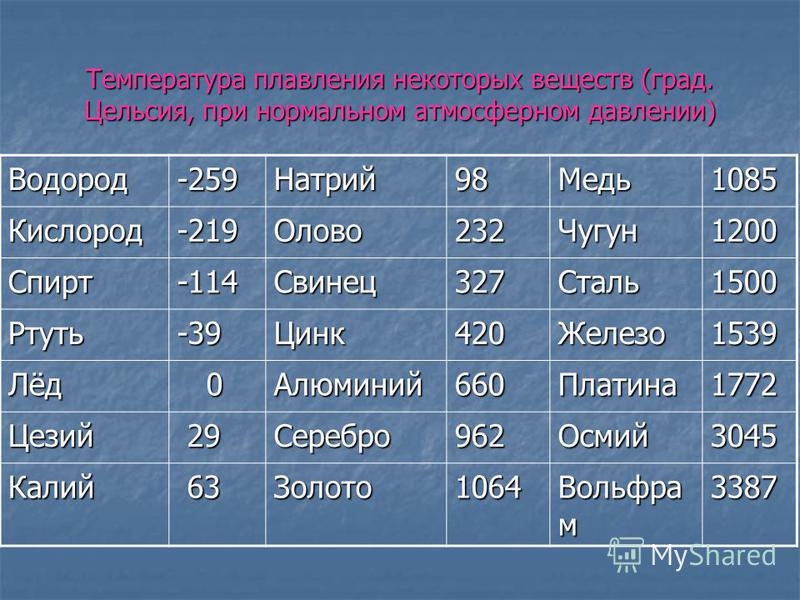 ru/metallurgiya/samostoyatelnoe-plavlenie-medi.html
ru/metallurgiya/samostoyatelnoe-plavlenie-medi.html
Плавка меди в домашних условиях: температура плавки и способы
Медь – пластичный материал, не подверженный окислению. Из него делают небольшие детали, используют в ремонтных работах. Переплавить лом можно самостоятельно в гараже, хозяйственной постройке или на собственной кухне. Специалисты подскажут, как расплавить медь в кустарных условиях. Технология несложная, главное при расплавлении учитывать физические свойства меди и сплавов.
Основные характеристики и температура плавления меди
Медь в древности использовать, расплавлять стали раньше, чем другие металлы. Металл ценится за химическую нейтральность, долговечность, электромагнитные свойства. Теплопроводность у медных сплавов чуть ниже, чем у серебра.
Домашняя плавка меди по сути ничем не отличается от промышленного литья. Переплавить можно кусочки отслуживших радиодеталей, недорогие ювелирные изделия, столовые предметы из мельхиора. Плавка меди в чистом виде происходит при +1083°С, такой режим в бытовых условиях создать не проблематично. Сплав с цинком, оловом не нужно расплавлять до температуры плавки меди, достаточно до +900 – 950°С. Подбирая кусочки лома, важно знать, что для электротехнических деталей используют чистые сплавы. Бронза, латунь может содержать вредные химические компоненты, они начнут выделяться из металла при расплавлении. Кипит металл при сравнительно низкой температуре, +2560°С, сплав начинает пузыриться.
Сплав с цинком, оловом не нужно расплавлять до температуры плавки меди, достаточно до +900 – 950°С. Подбирая кусочки лома, важно знать, что для электротехнических деталей используют чистые сплавы. Бронза, латунь может содержать вредные химические компоненты, они начнут выделяться из металла при расплавлении. Кипит металл при сравнительно низкой температуре, +2560°С, сплав начинает пузыриться.
Плавка меди в домашних условиях: пошаговая инструкция
Для расплавления не подойдет жестяная банка и костер. Нужны другие источники тепла, например, самодельные печи или готовые горелки с высокой температурой пламени. Для расплавления выбирают жаропрочные посудины, лучше всего использовать готовый тигель из огнеупорного сырья, выдерживающий температуру до +300°С. Для литья используют изложницу или форму. При работе с тиглем применяют специальные щипцы с длинными ручками, они должны хорошо зажимать тигель.
Теперь небольшой поэтапный инструктаж, как плавить медный лом в домашних условиях:
- Подготовка лома, в качестве сырья используют небольшие кусочки металла.

- Подготовка очага, где будет установлен тигель. Для расплавления лома используют готовые или импровизированные печи, горелки.
- Лом засыпают в тигель для расплавления металла. Специалисты советуют предварительно нагреть тигель, чтобы металл равномернее прогревался.
- Подготовка формы или изложницы – место, куда будет выливаться металл после расплавления. Для изготовления используют материал, имеющий температуру расплавления выше, чем у меди.
- Перед разливом с горячего металла снимают окалину с помощью длинной ложечки. Окислы не должны попасть в литье.
- Расплав осторожно выливают в подготовленную формочку. Работать нужно аккуратно, от капель остаются плохо заживающие ожоги.
Для подставки используют огнеупорный ровный лист, на него ставят тигель или специальный бокс для расплавления.
Муфельная печь
Лабораторный муфель – самое удобное устройство для расплавления металла.
Несколько советов, как расплавить медный сплав в лабораторных условиях:
- у муфельной печи есть ручка температурного регулятора, ее нужно поставить на отметку, незначительно превышающую температуру расплавления сплава;
- графитовый или керамический тигель перед загрузкой шихты хорошо прогревают;
- после отливки с горячего тигля проволочным крюком снимают окалину.
Литье в муфеле прогревается равномерно, плавильщик изолирован от летучих вредных компонентов, Через огнеупорное стекло дверцы удобно наблюдать за ходом расплавления меди.
Газовая горелка
Плавка меди в небольших объемах осуществляется ручной газовой горелкой. Мощность портативного устройства большого значения не имеет. Горелку располагают под тиглем, в котором будут плавить медный лом, направляют пламя на донце, языки должны охватывать его полностью. Процесс трудоемкий, длительный. Для защиты от кислорода цветной лом присыпают угольной крошкой.
Плавят медь в домашних условиях, используя тигельную печь или горн. Он представляет собой ограниченное пространство, куда на подставке помещается тигель. Снизу поджигаются угли или подводится горелка. Необходимо организовать воздухоподдув, чтобы повысить температуру горения топлива. Для ускорения процесса расплавления сверху горн прикрывают плотной крышкой. Хорошо раскаленный древесный уголь разогревают, засыпают в тигель с ломом. Метод используют специалисты, часто занимающиеся литьем в небольших объемах.
Он представляет собой ограниченное пространство, куда на подставке помещается тигель. Снизу поджигаются угли или подводится горелка. Необходимо организовать воздухоподдув, чтобы повысить температуру горения топлива. Для ускорения процесса расплавления сверху горн прикрывают плотной крышкой. Хорошо раскаленный древесный уголь разогревают, засыпают в тигель с ломом. Метод используют специалисты, часто занимающиеся литьем в небольших объемах.
Паяльная лампа
Сплав с цинком, оловом плавится при невысокой температуре. В качестве источника энергии для расплавления используют обычную паяльную лампу, ее располагают вертикально под тиглем так, чтобы пламя охватывало поверхность дна и нижнюю часть боковой стенки. Для снижения объема окалины лом присыпают древесным углем. Процесс окисления при расплавлении под слоем угольной крошки будет протекать не так интенсивно.
Микроволновая печь
Плавить медь в домашних условиях можно в микроволновке, из нее достают поворотный механизм.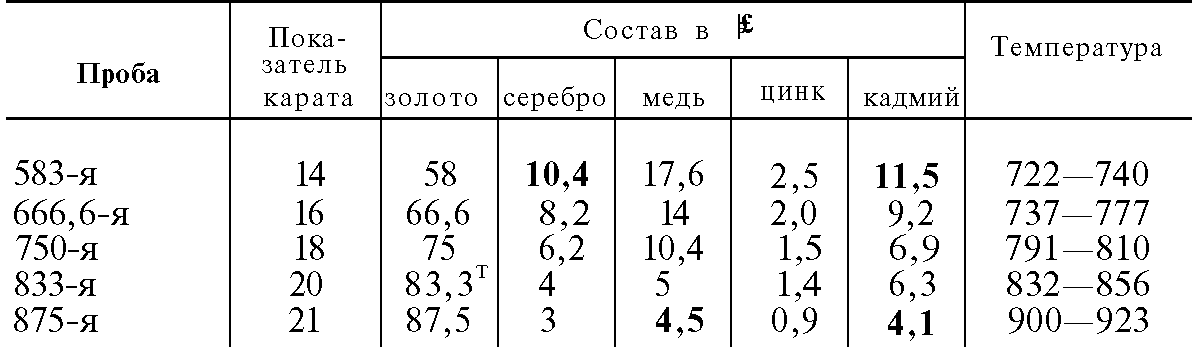 Под размер тигля делают огнеупорный контейнер с крышкой из шамотного кирпича. Сначала в течение 15 минут на максимальном режиме нагревают керамический тигель, он разогревается до желтоватого свечения. Затем в него засыпают подготовленный лом, снова убирают шамотный контейнер в печь, плавить медный лом необходимо 20-30 минут на максимальном режиме, создается температура порядка +1200°С. Затем сплав выливают в заранее подготовленную изложницу или форму.
Под размер тигля делают огнеупорный контейнер с крышкой из шамотного кирпича. Сначала в течение 15 минут на максимальном режиме нагревают керамический тигель, он разогревается до желтоватого свечения. Затем в него засыпают подготовленный лом, снова убирают шамотный контейнер в печь, плавить медный лом необходимо 20-30 минут на максимальном режиме, создается температура порядка +1200°С. Затем сплав выливают в заранее подготовленную изложницу или форму.
Для изготовления мелких деталей лучше выбирать многокомпонентные сплавы: латуни, бронзы, они не такие текучие, их проще плавить, не нужны слишком высокие температуры. Когда плавят медь в домашних условиях, соблюдают технику безопасности, предусматривают противопожарные меры.
Источник:
http://svarkaprosto.ru/tehnologii/plavka-medi
Температура и условия плавления меди в домашних условиях
С давних времен медные предметы пользовались спросом у людей. В настоящее время материал ценится за декоративные свойства. Однако осуществить плавление меди в домашних условиях непросто. Умельцы пробуют разные методы, чтобы провести эту процедуру самостоятельно.
Однако осуществить плавление меди в домашних условиях непросто. Умельцы пробуют разные методы, чтобы провести эту процедуру самостоятельно.
Описание элемента и распространение его в природе
Медь на Кипре добывали и плавили еще в середине третьего тысячелетия до нашей эры. Поэтому свое название элемент носит в честь упомянутого острова. Добыча и производство элемента подействовали на историю развития острова и его экономическое положение.
В периодической системе Менделеева медь получила 29 атомный номер. Элемент расположен в одиннадцатой группе четвертого периода. Элемент имеет золотисто-розовый цвет и принадлежит к пластичным переходным металлам. В природе встречается продукт в виде сульфидных руд, по распространению в литосфере металл занимает 23-е место. Медный блеск и колчедан являются самыми распространенными видами элемента.
В природных условиях элемент медь находят в руде и в виде самородков. Самые лучшие месторождения находятся на территории государства Чили.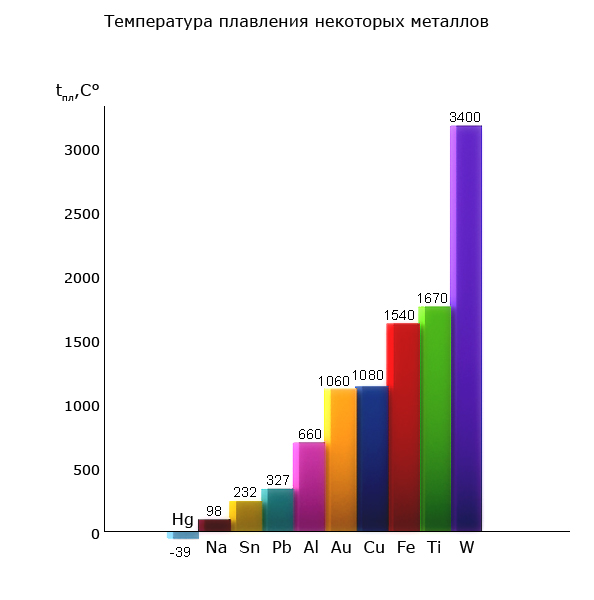 Медные месторождения встречаются там в осадочных породах. Медные песчаники и сланцы находятся в Казахстане и Читинской области России.
Медные месторождения встречаются там в осадочных породах. Медные песчаники и сланцы находятся в Казахстане и Читинской области России.
Медь наделена высокой электро и теплопроводностью. Ее удельная теплоемкость при температуре +20ºС равна 390 Дж/кг. Температура кипения металла – 2595ºС.
В момент плавления металл меняет свое агрегатное состояние, т. е. из кристаллической твердой фазы он переходит в жидкую форму. Меди присуще своя температура плавления, она имеет определенную зависимость от находящихся в металле примесей. Плавка меди чаще всего проходит при температуре +1083ºС. Если в медном сплаве присутствует олово, то процесс плавления способен произойти при +950–1140ºС. В составе с цинком теплота плавления меди равна от +900 до +1050ºС.
Процесс плавки проходит следующим образом: в начале нагрева рушится кристаллическая решетка металла, постепенно температура увеличивается, но в определенный период она удерживается в некотором значении. Именно в этот промежуток медь начинает плавиться. После окончания выплавки температура вновь повышается. Далее, металл постепенно охлаждается и принимает твердую форму.
После окончания выплавки температура вновь повышается. Далее, металл постепенно охлаждается и принимает твердую форму.
Кипение металла очень похоже на бурление жидкости при активном нагреве. В это время выделяется газ. На поверхности расплавленного продукта появляются пузырьки. При максимальном нагреве из жидкого металла выделяется углерод, он формируется в результате окисления элемента.
Плавление меди в домашних условиях
В давние времена человек обнаружил медную руду, а,возможно, и самородки. В определенный момент принял решение: переплавлю металл на костре. Из металлических отливок люди готовили разнообразные бытовые принадлежности, украшения и даже оружие. Для тех кто хотел бы, но не знает, как расплавить медь самостоятельно, необходимо запастись следующими предметами, основные из которых:
- Тигель — посуда из огнеупорного материала для меди.
- Специальное нагревательное устройство (муфельная печь), автоген или горн.
- Древесный уголь.
- Стальной удобный крюк.

- Пылесос бытовой.
- Специальная форма для плавки металла.
При производстве металла следует соблюдать технику безопасности. Плавка должна производиться поэтапно. В первую очередь переплавляемый продукт должен поместиться в тигель, далее этот сосуд определяется в муфельную печь. Агрегат нагревается до нужной температуры, следить за этим мероприятием необходимо в специальное смотровое окошко. В момент образования окисной пленки на металле, его следует убрать с помощью стального крюка. Окисел необходимо аккуратно отодвинуть в сторону.
В том случае, если расплав меди планируется производить при помощи автогена, то важно понимать, что при данном процессе происходит естественный доступ воздуха. Нагревая тигель, нужно следить за тем, чтобы пламя охватывало его полностью. При помощи паяльной лампы можно качественно нагреть легкоплавкую бронзу или желтую медь.
Если дома нет вышеупомянутых предметов для плавки металла, то стоит попробовать осуществить это при помощи горна, его ставят на древесный уголь. Для усиления температурного режима используется пылесос. Важно помнить, пылесос можно использовать только в режиме выдувания и его наконечник должен быть выполнен из металла. Желательно иметь наконечник у поддува утонченный, чтобы струя воздуха хорошо попадала на тигель. Эта процедура поможет увеличить температуру до 1400ºС.
Для усиления температурного режима используется пылесос. Важно помнить, пылесос можно использовать только в режиме выдувания и его наконечник должен быть выполнен из металла. Желательно иметь наконечник у поддува утонченный, чтобы струя воздуха хорошо попадала на тигель. Эта процедура поможет увеличить температуру до 1400ºС.
В настоящее время в промышленных условиях чистую медь не используют, в ее состав может входить сурьма, железо, никель и т. д. На качество продукта влияет количество примесей, их не должно быть более 1%. Основными показателями для медных изделий являются электропроводность и теплопроводность.
Проводя плавку меди в домашних условиях, стоит понимать, данное мероприятие требует определенных знаний и затрат. Невозможно расплавить медь без тигеля. Горн соорудить можно самостоятельно из огнеупорного кирпича. Для того чтобы медь не сильно окислялась, ее присыпают древесным углем. В остальном процесс плавки не отличается от кокильного литья или заливки в земляные формы.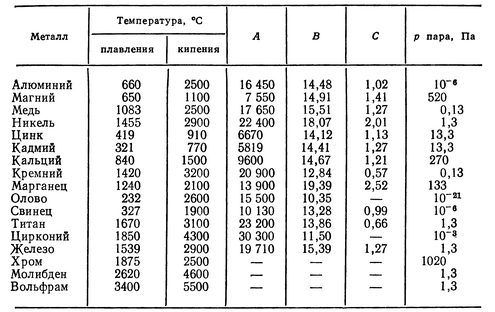
Источник:
http://ometallah.com/plavlenie/i-temperatura-medi.html
Температура плавления меди
На заре человечества люди пытались освоить создание различных элементов из металлов. Такие вещи были более изящные, тонкие и долговечные. Одним из первых была «покорена» медь. Наличие руды требовало расплавления материала и отделения от шлака. Это выполнялось в раскаленных углях на земле. Температуру нагнетали мехами, создающими жар. Процесс был горячим и трудоемким, но позволял получать необычные украшения, посуду и орудия труда. Отдельным направлением стало изготовление оружия для охоты, которое могло служить долгое время. Температура плавления меди относительно невысока, что позволяет и сегодня плавить ее в бытовой обстановке и производить предметы, необходимые для ремонта механизмов или электрического оборудования. Какая температура плавки у меди и ее сплавов? Чем можно выполнить эту процедуру в домашних условиях?
Какая температура плавки у меди и ее сплавов? Чем можно выполнить эту процедуру в домашних условиях?
Главное о меди
В таблице Менделеева этот материал получил название Cuprum. Ему присвоен атомный номер 29. Это пластичный материал, отлично обрабатывающийся в твердом виде шлифовальным и резным оборудованием. Хорошая проводимость напряжения позволяет активно использовать медь в электрике и промышленном оборудовании.
В земной коре материал находится в виде сульфидной руды. Часто встречаемые залежи обнаруживаются в Южной Америке, Казахстане, России. Это медный колчедан и медный блеск. Они образовываются при средней температуре, как геотермальные тоненькие пласты. Находят и чистые самородки, которые не нуждаются в отделении шлака, но требуют плавления для добавки других металлов, т. к. в чистом виде медь обычно не используется.
Красновато-желтый оттенок металл имеет благодаря оксидной пленке, покрывающей поверхность сразу, при взаимодействии с кислородом. Оксид не только придает красивый цвет, но и содействует более высоким антикоррозийным свойствам. Материал без оксидной пленки имеет светло-желтый цвет.
Оксид не только придает красивый цвет, но и содействует более высоким антикоррозийным свойствам. Материал без оксидной пленки имеет светло-желтый цвет.
Плавится чистая медь при достижении 1080 градусов. Это относительно невысокая цифра позволяет работать с металлом как в производственных условиях, так и дома. Другие физические свойства материала следующие:
- Плотность меди в чистом виде составляет 8,94 х 103 кг/м квадратный.
- Отличается металл и хорошей электропроводностью, которая при средней температуре в 20 градусов является 55,5 S.
- Медь хорошо передает тепло, и этот показатель составляет 390 Дж/кг.
- Выделение углерода при кипении жидкого материала начинается от 2595 градусов.
- Электрическое сопротивление (удельное) в температурном диапазоне от 20 до 100 градусов — 1,78 х 10 Ом/м.
Плавление металла и его сплавов
График плавления меди имеет пять ступеней процесса:
- При температуре 20-100 градусов металл находится в твердом состоянии.
 Последующий нагрев содействует изменению цвета, что происходит при удалении верхнего оксида.
Последующий нагрев содействует изменению цвета, что происходит при удалении верхнего оксида. - При достижении отметки температуры в 1083 градуса, материал переходит в жидкое состояние, а его цвет становится абсолютно белым. В этот момент разрушается кристаллическая решетка металла. На небольшой период рост температуры прекращается, а после достижения полностью жидкой стадии, возобновляется.
- Закипает материал при 2595 градусах. Это схоже с кипением густой жидкости, где также происходит выделение углерода.
- Когда источник тепла выключается, то пиковая температура начинает понижаться. При кристаллизации происходит замедление снижения температуры.
- После обретения твердой стадии, металл остывает окончательно.
Температура плавления бронзы немного ниже из-за наличия в составе олова. Разрушение кристаллической решетки этого сплава происходит при достижении 950-1100 градусов. Медный сплав с цинком, известный как латунь, способен плавиться от 900°C. Это позволяет работать с материалами при несложном оборудовании.
Это позволяет работать с материалами при несложном оборудовании.
Плавление в бытовых условиях
Плавка меди в домашних условиях возможна несколькими способами. Для этого понадобиться ряд приспособлений. Сложность процесса зависит от использования конкретного вида оборудования.
Самым простым способом для плавления меди дома является муфельная печь. У мастеров по металлу найдется такое устройство, которым можно будет воспользоваться. Кусочки металла ложатся в специальную емкость — тигель. Он устанавливается в печь, на которой выставляется требуемая температура. Через смотровое окно можно заметить процесс перехода в жидкое состояние, и открыв дверцу удалить оксидную пленку. Делать это необходимо стальным крюком и в защитной перчатке. Жар от печи довольно сильный, поэтому действовать необходимо аккуратно.
Еще одним способом плавки меди в домашних условиях является пропан-кислородное пламя. Оно хорошо подходит и для сплавов металла с цинком или оловом. В качестве рабочего инструмента в руках мастера может быть горелка или резак. Ацетилен-кислородное пламя тоже подойдет, но погреть материал придется немного подольше. Кусочки сплава помещают в тигель, устанавливаемый на жаропрочное основание. Горелкой выполняют произвольные движения по всему корпусу емкости. Быстрый эффект можно получить, если следить чтобы факел пламени касался поверхности тигеля кончиком синего цвета. Там наибольшая температура.
Ацетилен-кислородное пламя тоже подойдет, но погреть материал придется немного подольше. Кусочки сплава помещают в тигель, устанавливаемый на жаропрочное основание. Горелкой выполняют произвольные движения по всему корпусу емкости. Быстрый эффект можно получить, если следить чтобы факел пламени касался поверхности тигеля кончиком синего цвета. Там наибольшая температура.
Еще одним способом является мощная микроволновка. Но чтобы повысить теплосберегающие свойства и защитить внутренние детали техники от перегрева, необходимо поместить тигель в жаропрочный материал и накрыть его сверху. Это могут быть специальные виды кирпича.
Самым простым в экономическом плане способом служит слой древесного угля, на который устанавливается горн с медью. Усилить жар можно при помощи пылесоса, работающего на выдув. Кончик шланга направленный на угли должен быть металлическим, а сопло иметь плоскую форму для усиления потока воздуха.
Изготовление деталей и других элементов из меди, путем ее плавки в домашних условиях, возможно благодаря относительно низкой температуре разрушения кристаллической решетки в материале. Используя описанные выше приспособления и ознакомившись с видео, у большинства получится реализовать эту цель.
Используя описанные выше приспособления и ознакомившись с видео, у большинства получится реализовать эту цель.
Поделись с друзьями
0
0
0
0
При какой температуре плавятся металлы таблица. Физические свойства металлов
Каждый металл или сплав обладает уникальными свойствами, в число которых входит температура плавления. При этом объект переходит из одного состояния в другое, в конкретном случае становится из твёрдого жидким. Чтобы его расплавить, необходимо подвести к нему тепло и нагревать до достижения нужной температуры. В момент, когда достигается нужная точка температуры данного сплава, он ещё может остаться в твёрдом состоянии. При продолжении воздействия начинает плавиться.
Наиболее низкая температура плавления у ртути — она плавится даже при -39 °C, самая высокая у вольфрама — 3422 °C. Для сплавов (стали и других) определить точную цифру крайне сложно. Все зависит от соотношения компонентов в них. У сплавов она записывается как числовой промежуток.
Все зависит от соотношения компонентов в них. У сплавов она записывается как числовой промежуток.
Как происходит процесс
Элементы, какими бы они ни были: золото, железо, чугун, сталь или любой другой — плавятся примерно одинаково. Это происходит при внешнем или внутреннем нагревании. Внешнее нагревание осуществляется в термической печи. Для внутреннего применяют резистивный нагрев, пропуская электрический ток или индукционный нагрев в электромагнитном поле высокой частоты . Воздействие при этом примерно одинаковое.
Когда происходит нагревание , усиливается амплитуда тепловых колебаний молекул. Появляются структурные дефекты решётки , сопровождаемые разрывом межатомных связей. Период разрушения решётки и скопления дефектов и называется плавлением.
В зависимости от градуса, при котором плавятся металлы, они разделяются на:
- легкоплавкие — до 600 °C: свинец, цинк, олово;
- среднеплавкие — от 600 °C до 1600 °C: золото, медь, алюминий, чугун, железо и большая часть всех элементов и соединений;
- тугоплавкие — от 1600 °C: хром, вольфрам, молибден, титан.

В зависимости от того, каков максимальный градус, подбирается и плавильный аппарат. Он должен быть тем прочнее, чем сильнее будет нагревание.
Вторая важная величина — градус кипения. Это параметр, при достижении которого начинается кипение жидкостей. Как правило, она в два раза выше градуса плавления. Эти величины прямо пропорциональны между собой и обычно их приводят при нормальном давлении.
Если давление увеличивается, величина плавления тоже увеличивается. Если давление уменьшается, то и она уменьшается.
Таблица характеристик
Металлы и сплавы — непременная основа для ковки , литейного производства, ювелирной продукции и многих других сфер производства. Чтобы не делал мастер (ювелирные украшения из золота , ограды из чугуна, ножи из стали или браслеты из меди) , для правильной работы ему необходимо знать температуры, при которых плавится тот или иной элемент.
Чтобы узнать этот параметр, нужно обратиться к таблице. В таблице также можно найти и градус кипения.
В таблице также можно найти и градус кипения.
Среди наиболее часто применяемых в быту элементов показатели температуры плавления такие:
- алюминий — 660 °C;
- температура плавления меди — 1083 °C;
- температура плавления золота — 1063 °C;
- серебро — 960 °C;
- олово — 232 °C. Олово часто используют при пайке, так как температура работающего паяльника составляет как раз 250–400 градусов;
- свинец — 327 °C;
- температура плавления железо — 1539 °C;
- температура плавления стали (сплав железа и углерода) — от 1300 °C до 1500 °C. Она колеблется в зависимости от насыщенности стали компонентами;
- температура плавления чугуна (также сплав железа и углерода) — от 1100 °C до 1300 °C;
- ртуть — -38,9 °C.
Как понятно из этой части таблицы, самый легкоплавкий металл — ртуть, которая при плюсовых температурах уже находится в жидком состоянии.
Градус кипения всех этих элементов почти вдвое, а иногда и ещё выше градуса плавления.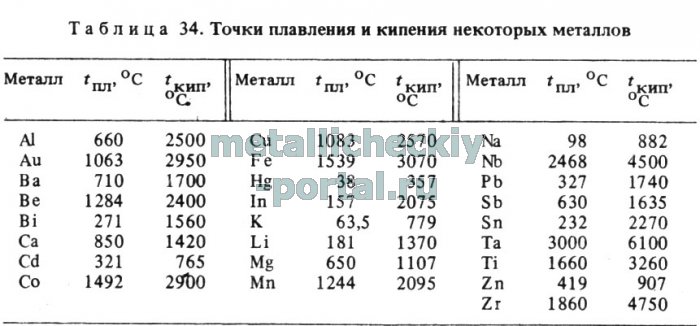 Например, у золота он 2660 °C, у алюминия — 2519 °C , у железа — 2900 °C, у меди — 2580 °C, у ртути — 356,73 °C.
Например, у золота он 2660 °C, у алюминия — 2519 °C , у железа — 2900 °C, у меди — 2580 °C, у ртути — 356,73 °C.
У сплавов типа стали, чугуна и прочих металлов расчёт примерно такой же и зависит от соотношения компонентов в сплаве.
Максимальная температура кипения у металлов — у рения — 5596 °C . Наибольшая температура кипения — у наиболее тугоплавящихся материалов.
Бывают таблицы, в которых также указана плотность металлов . Самым лёгким металлом является литий, самым тяжёлым — осмий. У осмия плотность выше, чем у урана и плутония, если рассматривать её при комнатной температуре. К лёгким металлам относятся: магний, алюминий, титан. К тяжёлым относится большинство распространённых металлов: железо, медь, цинк, олово и многие другие. Последняя группа — очень тяжёлые металлы, к ним относятся: вольфрам, золото, свинец и другие.
Ещё один показатель, встречающийся в таблицах — это теплопроводность металлов . Хуже всего тепло проводит нептуний, а лучший по теплопроводности металл — серебро.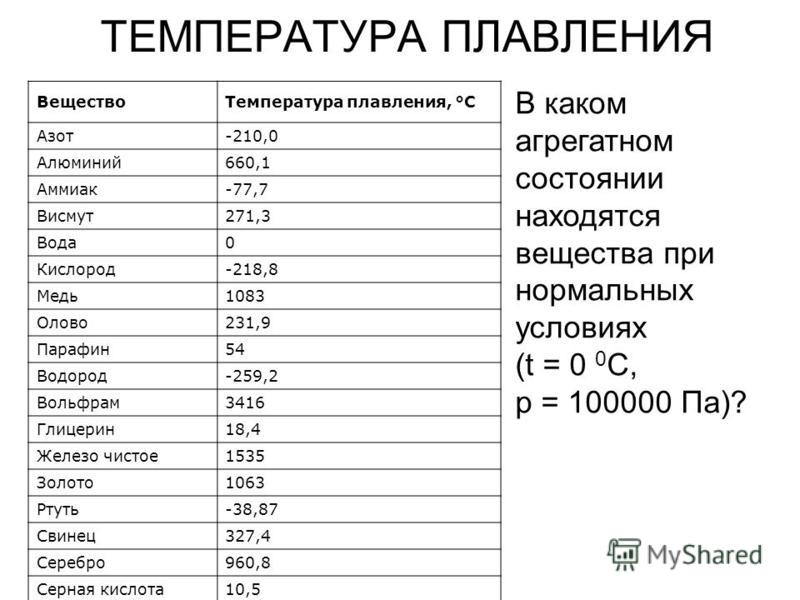 Золото, сталь, железо, чугун и прочие элементы находится посередине между этими двумя крайностями. Чёткие характеристики для каждого можно найти в нужной таблице.
Золото, сталь, железо, чугун и прочие элементы находится посередине между этими двумя крайностями. Чёткие характеристики для каждого можно найти в нужной таблице.
Температура плавления, наряду с плотностью, относится к физическим характеристикам металлов . Температура плавления металла — температура, при которой металл переходит из твердого состояния, в котором находится в нормальном состоянии (кроме ртути), в жидкое состояние при нагревании. При плавлении объем металла практически не изменяется, поэтому на температуру плавления нормальное атмосферное давление не влияет .
Температура плавления металлов находится в диапазоне от -39 градусов Цельсия до +3410 градусов . Для большинства металлов температура плавления высокая, однако, некоторые металлы можно расплавить в домашних условиях при нагревании на обычной горелке (олово, свинец).
Классификация металлов по температуре плавления
- Легкоплавкие металлы , температура плавления которых колеблется до 600 градусов Цельсия, например цинк, олово, висмут .

- Среднеплавкие металлы , которые плавятся при температуре от 600 до 1600 градусов Цельсия: такие как алюминий, медь, олово, железо .
- Тугоплавкие металлы , температура плавления которых достигает более 1600 градусов Цельсия — вольфрам, титан, хром и др.
- — единственный металл, находящийся при обычных условиях (нормальное атмосферное давление, средняя температура окружающей среды) в жидком состоянии. Температура плавления ртути составляет порядка -39 градусов по Цельсию.
Таблица температур плавления металлов и сплавов
| Металл | Температура плавления, градусов Цельсия |
| Алюминий | 660,4 |
| Вольфрам | 3420 |
| Дюралюмин | ~650 |
| Железо | 1539 |
| Золото | 1063 |
| Иридий | 2447 |
| Калий | 63,6 |
| Кремний | 1415 |
| Латунь | ~1000 |
| Легкоплавкий сплав | 60,5 |
| Магний | 650 |
| Медь | 1084,5 |
| Натрий | 97,8 |
| Никель | 1455 |
| Олово | 231,9 |
| Платина | 1769,3 |
| Ртуть | –38,9 |
| Свинец | 327,4 |
| Серебро | 961,9 |
| Сталь | 1300-1500 |
| Цинк | 419,5 |
| Чугун | 1100-1300 |
При плавлении металла для изготовления металлических изделий-отливок от температуры плавления зависит выбор оборудования, материала для формовки металла и др.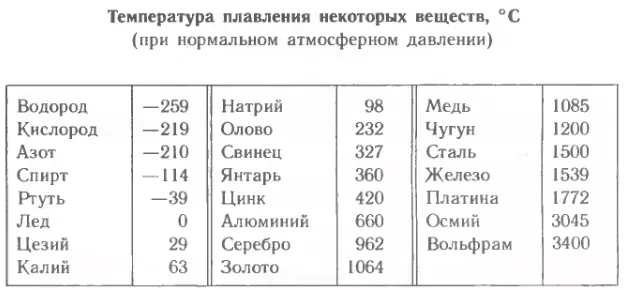 Следует также помнить, что при легировании металла другими элементами температура плавления чаще всего снижается .
Следует также помнить, что при легировании металла другими элементами температура плавления чаще всего снижается .
Интересный факт
Не стоит путать понятия «температура плавления металла» и «температура кипения металла» — для многих металлов эти характеристики существенно отличаются: так, серебро плавится при температуре 961 градус по Цельсию, а закипает только при достижении нагрева до 2180 градусов.
Температура плавления металла – это минимальная температура, при которой он переходит из твердого состояния в жидкое. При плавлении его объем практически не изменяется. Металлы классифицируют по температуре плавления в зависимости от степени нагревания.
Легкоплавкие металлы
Легкоплавкие металлы имеют температуру плавления ниже 600°C. Это цинк, олово, висмут. Такие металлы можно расплавить в домашних условиях , разогрев их на плите, или с помощью паяльника. Легкоплавкие металлы используются в электронике и технике для соединения металлических элементов и проводов для движения электрического тока. Температура плавления олова составляет 232 градуса, а цинка – 419.
Температура плавления олова составляет 232 градуса, а цинка – 419.
Среднеплавкие металлы
Среднеплавкие металлы начинают переходить из твердого в жидкое состояние при температуре от 600°C до 1600°C. Они используются для изготовления плит, арматур, блоков и других металлических конструкций, пригодных для строительства. К этой группе металлов относятся железо, медь, алюминий, они также входят в состав многих сплавов. Медь добавляют в сплавы драгоценных металлов, таких как золото, серебро, платина. Золото 750 пробы на 25% состоит из лигатурных металлов, в том числе и меди, которая придает ему красноватый оттенок. Температура плавления этого материала равна 1084 °C. А алюминий начинает плавиться при относительно низкой температуре, составляющей 660 градусов Цельсия. Это легкий пластичный и недорогой металл, который не окисляется и не ржавеет, поэтому широко используется при изготовлении посуды. Температура плавления железа равна 1539 градусов. Это один из самых популярных и доступных металлов, его применение распространено в строительстве и автомобильной промышленности. Но ввиду того, что железо подвергается коррозии, его нужно дополнительно обрабатывать и покрывать защитным слоем краски, олифы или не допускать попадания влаги.
Но ввиду того, что железо подвергается коррозии, его нужно дополнительно обрабатывать и покрывать защитным слоем краски, олифы или не допускать попадания влаги.
Тугоплавкие металлы
Температура тугоплавких металлов выше 1600°C. Это вольфрам, титан, платина, хром и другие. Их используют в качестве источников света, машинных деталей, смазочных материалов, а также в ядерной промышленности. Из них изготавливают проволоки, высоковольтные провода и используют для расплавки других металлов с более низкой температурой плавления. Платина начинает переходить из твердого в жидкое состояние при температуре 1769 градусов, а вольфрам – при температуре 3420°C.
Ртуть – единственный металл, находящийся в жидком состоянии при обычных условиях, а именно, нормальном атмосферном давлении и средней температуре окружающей среды. Температура плавления ртути составляет минус 39°C. Этот металл и его пары являются ядовитыми, поэтому он используется только в закрытых емкостях или в лабораториях. Распространенное применение ртути – градусник для измерения температуры тела.
Распространенное применение ртути – градусник для измерения температуры тела.
Может ли золото плавиться при комнатной температуре? Понижение температуры плавления! — Устойчивое Нано
Золото — один из самых желанных металлов в мире. Драгоценный желтый металл редко встречается в природе и с древних времен использовался в качестве валюты и в производстве ювелирных изделий (рис. 1). 1 Считается, что золото принесено на Землю метеоритами, оно действительно не из этого мира! 2 Есть много причин, по которым золото является особенным и сохраняет свою ценность в наших обществах.Но золото может быть даже более особенным, чем мы думали.
Рисунок 1: Золотая диадема из Древней Греции (4 — век до нашей эры) в Художественном музее Далласа. (изображение Мэри Харрш) Создавая и обрабатывая этот блестящий металл, люди постепенно узнали его физические и химические свойства. «Настоящее золото не боится огня» — это старая китайская идиома, которая берет свое начало из того факта, что золото в массе остается неповрежденным и блестящим, когда его кладут на дровяной огонь (600-1000 ° C ), тогда как большинство других металлов (таких как медь, цинк , никель и их сплавы) в этих условиях плавятся и / или тускнеют.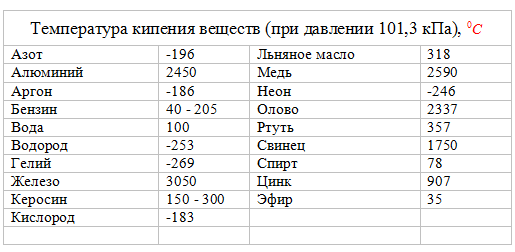 В терминах химии мы говорим, что золото обладает превосходной химической устойчивостью к окислению и относительно высокой температурой плавления (1064 ° C ). Но оказывается, что благодаря нанонауке есть способы изменить поведение золота при разных температурах, сохранив при этом другие его особые характеристики.
В терминах химии мы говорим, что золото обладает превосходной химической устойчивостью к окислению и относительно высокой температурой плавления (1064 ° C ). Но оказывается, что благодаря нанонауке есть способы изменить поведение золота при разных температурах, сохранив при этом другие его особые характеристики.
Давайте используем наш повседневный опыт работы с водой в качестве примера, чтобы понять, что происходит с золотом. Мы знаем, что лед (твердый), кажется, всегда тает в воду (жидкость) при фиксированной температуре, а затем вода, кажется, всегда испаряется в пар (газ) при фиксированной температуре.Эти температуры называются точкой плавления и точкой кипения соответственно. Точки плавления и кипения могут быть разными в зависимости от местного давления. Вот почему ваши рецепты приготовления или выпечки могут содержать разные инструкции для больших высот, где давление воздуха ниже, чем на малых высотах.
Однако нам не нужно карабкаться вверх и вниз по горам, чтобы управлять температурой кипения.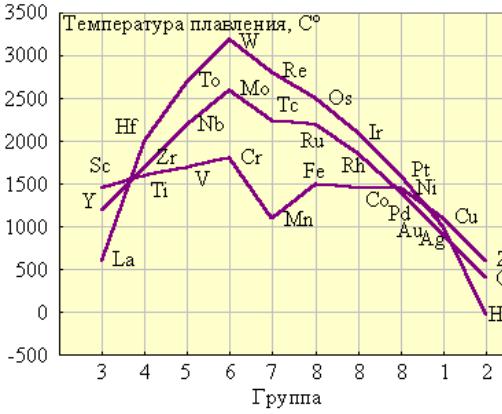 Мы можем легко сделать это, изменив местное давление, как работает скороварка: при увеличении давления точка кипения воды повышается до более высокой температуры, что означает, что вода может нагреваться без испарения, что заставляет пищу готовиться. быстрее (рисунок 2).
Мы можем легко сделать это, изменив местное давление, как работает скороварка: при увеличении давления точка кипения воды повышается до более высокой температуры, что означает, что вода может нагреваться без испарения, что заставляет пищу готовиться. быстрее (рисунок 2).
Чтобы понять, как скороварка повышает давление внутри, мы должны вспомнить, что происходит с молекулами жидкости, когда она нагревается: они начни отдаляться дальше! Однако точка плавления гораздо менее чувствительна к локальному изменению давления. Это связано с тем, что по сравнению с испарением жидкости в газ, объем обычно не увеличивается слишком сильно, когда твердые частицы плавятся в жидкости. (Примечание: вода необычна тем, что ее объем на самом деле становится на больше , когда она замерзает до твердого состояния — когда-нибудь взрывалась банка газировки в морозильной камере? — но это тема для другого поста!)
Суть в том, что нецелесообразно манипулировать температурой плавления вещества, изменяя местное давление — вам придется резко изменить давление, чтобы получить хотя бы небольшое изменение точки плавления (рис. 3).
3).
Но есть ли другие способы изменить температуру плавления материала? И, возвращаясь к основной теме этого поста, можно ли плавить золото при комнатной температуре?
В более раннем сообщении блога «Наночастицы повсюду вокруг нас» мы обсуждали, что по мере уменьшения размера материала до наномасштаба меняются и многие физические и химические свойства. В основном это связано с «эффектом поверхности» или повышенным отношением площади поверхности к объему (рис. 4). 3
Рисунок 4: Сила наночастиц: площадь поверхности увеличивается с уменьшением размера частиц. (изображение Боба Хамерса)Цвет золота, например, меняется с блестящего желтого на темно-красный, когда его размер уменьшается до нанометрового диапазона (рис. 5). Так как же температура плавления материала изменяется при уменьшении его размера до наномасштаба?
Рисунок 5: Растворы наночастиц золота. Цвет раствора меняется по мере увеличения размера наночастиц золота. (изображение Александра Кондински)
Цвет раствора меняется по мере увеличения размера наночастиц золота. (изображение Александра Кондински) Еще в 1871 году (когда у него не было возможности фактически увидеть наночастицы) сэр Уильям Томсон показал, что точка плавления изменяется обратно пропорционально радиусу частицы в соответствии со следующим уравнением, известным сегодня как уравнение Гиббса. -Уравнение Томсона 4 :
Если ввести информацию о размере частиц материала и других характеристиках, это уравнение показывает, что размер материала и температура плавления напрямую связаны.По мере уменьшения размера материала температура плавления также снижается. Это явление широко известно как «понижение точки плавления». 5
На рисунке 6 показана взаимосвязь между размером наночастиц и температурой плавления золота в соответствии с уравнением Гиббса-Томсона.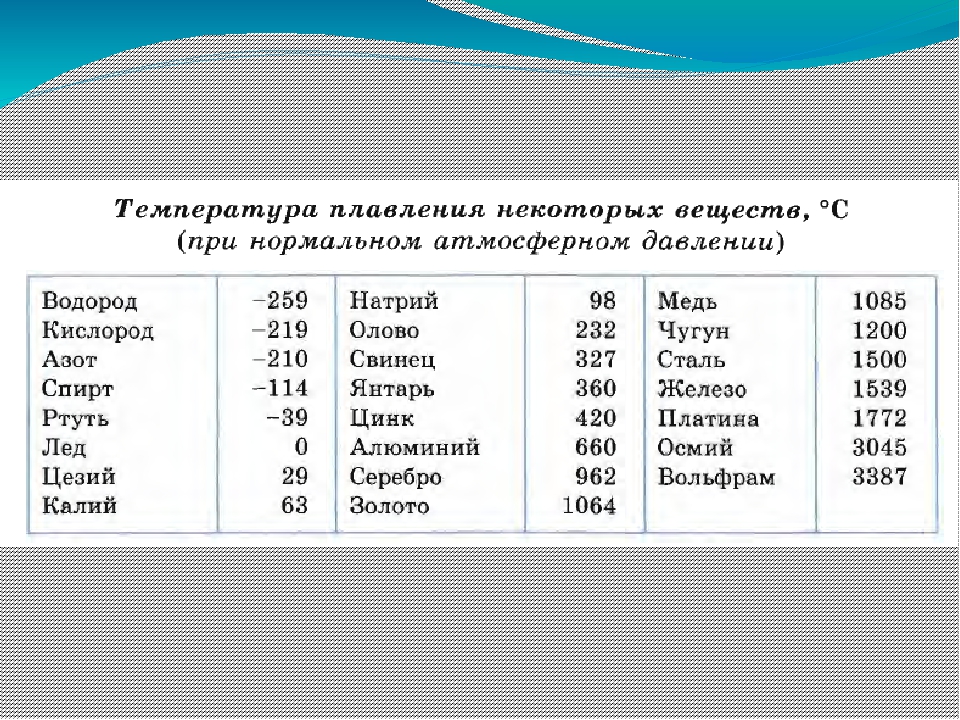 Как мы видим, температура плавления наночастиц золота может быть даже ниже комнатной температуры (~ 23-25 ° C), когда размер уменьшается до менее 1.4 нм. При таком размере в каждой наночастице присутствует всего около 85 атомов, и большинство атомов находятся на поверхности. 6 (Напротив, в частице размером 4 нм имеется почти 2000 атомов золота, поэтому большинство атомов все еще находится внутри частицы. Хотите знать, откуда мы это знаем? См. Нашу запись в блоге «Как можно подсчитать, сколько атомов находятся в наночастице? »)
Как мы видим, температура плавления наночастиц золота может быть даже ниже комнатной температуры (~ 23-25 ° C), когда размер уменьшается до менее 1.4 нм. При таком размере в каждой наночастице присутствует всего около 85 атомов, и большинство атомов находятся на поверхности. 6 (Напротив, в частице размером 4 нм имеется почти 2000 атомов золота, поэтому большинство атомов все еще находится внутри частицы. Хотите знать, откуда мы это знаем? См. Нашу запись в блоге «Как можно подсчитать, сколько атомов находятся в наночастице? »)
Разницу между твердым телом и жидкостью легко увидеть для объектов нормального размера: жидкости движутся, текут и принимают форму любого контейнера, в который они помещены, но твердые тела жесткие и не всплывают. 7 Но есть ли способ непосредственно визуализировать «жидкие наночастицы», которые мы здесь описывали?
Рис. 7. В отличие от наночастиц, кошек легко увидеть, если они обладают свойствами жидкости. 8 (изображение Peregrino Will Reign) Просвечивающая электронная микроскопия (ПЭМ) очень хорошо подходит для этой цели. Когда электронные лучи попадают на образец, они могут нагреваться и расплавлять наночастицы. Атомы в образце также могут вызывать дифракцию падающих электронных лучей во многих конкретных направлениях.Измеряя углы и интенсивность этих дифрагированных лучей, можно создавать дифракционные картины и определять положение атомов в образце. В твердых телах атомы обычно сильно упорядочены, но движутся в жидкостях, что приводит к разным дифракционным картинам. Пятнистые образцы обычно наблюдаются для твердых образцов, тогда как образцы ореолов обычно наблюдаются для жидких образцов. Затем мы можем отличить твердое состояние от жидкого состояния, глядя на их электронограммы.(Подробнее об электронной микроскопии см. В нашем посте «Природа под микроскопом: исследование красоты нанонауки».)
Когда электронные лучи попадают на образец, они могут нагреваться и расплавлять наночастицы. Атомы в образце также могут вызывать дифракцию падающих электронных лучей во многих конкретных направлениях.Измеряя углы и интенсивность этих дифрагированных лучей, можно создавать дифракционные картины и определять положение атомов в образце. В твердых телах атомы обычно сильно упорядочены, но движутся в жидкостях, что приводит к разным дифракционным картинам. Пятнистые образцы обычно наблюдаются для твердых образцов, тогда как образцы ореолов обычно наблюдаются для жидких образцов. Затем мы можем отличить твердое состояние от жидкого состояния, глядя на их электронограммы.(Подробнее об электронной микроскопии см. В нашем посте «Природа под микроскопом: исследование красоты нанонауки».)
Еще в 1954 году Takagi впервые применил эту стратегию для проверки «подавления точки плавления» (Рисунок 8). Он выбрал свинец для изучения, потому что он имеет относительно низкую температуру плавления и может быть легко превращен в пленку толщиной 5 нм.Под TEM Такаги и его команда увидели, что температура плавления свинцовой пленки толщиной 5 нм снизилась с обычных 327 ° C до 170 ° C. 9
Он выбрал свинец для изучения, потому что он имеет относительно низкую температуру плавления и может быть легко превращен в пленку толщиной 5 нм.Под TEM Такаги и его команда увидели, что температура плавления свинцовой пленки толщиной 5 нм снизилась с обычных 327 ° C до 170 ° C. 9
Хотя результаты Такаги были впечатляющими, они не смогли зафиксировать переход твердого вещества в жидкость в реальном времени. В настоящее время это возможно благодаря разработке так называемого ТЭМ in situ . 10 Когда наночастицы серебра размером менее 10 нм были помещены на вольфрамовый наконечник, исследователи наблюдали «жидкое» поведение при определенных обстоятельствах.Наночастицы серебра оставались высококристаллическими внутри, предполагая, что они не плавились — если бы частицы действительно расплавились, мы бы ожидали увидеть не кристаллические узоры и полностью случайное расположение атомов (как узор ореола на рисунке 8). Такое интересное «жидкое» поведение было приписано атомам наночастицы серебра, движущимся под давлением, создавая иллюзию, что она расплавилась (рис. 9).
Такое интересное «жидкое» поведение было приписано атомам наночастицы серебра, движущимся под давлением, создавая иллюзию, что она расплавилась (рис. 9).
Все это помогает нам понять, что, несмотря на то, что раньше люди думали, что «настоящее золото не боится огня», теперь мы знаем, что наноразмерные металлы, включая золото , может вести себя как жидкость при комнатной температуре!
С одной стороны, понижение температуры плавления может сделать некоторые наночастицы менее полезными, если они должны находиться в твердом состоянии, чтобы функционировать в своих технологических приложениях. С другой стороны, снижение температуры плавления также очень полезно для приложений, в которых наночастицы лучше работают в жидком состоянии.Например, мы можем легко изменить форму наноразмерных материалов при гораздо более низких температурах, чем можно было бы предположить по их температуре плавления.
Таким образом, ответ на вопрос, с которого мы начали: Да! Теоретически золото или любой другой материал можно рассматривать как «расплавленный» благодаря удивительным свойствам материалов в наномасштабе.
ОБРАЗОВАТЕЛЬНЫЕ РЕСУРСЫ
ССЫЛКИ
- Красимиров, А. Возможно, только что был обнаружен старейший в мире золотой артефакт.Huffington Post, 10 августа, , 2016, .
- Чой, К.К. Астероиды могли доставить на Землю драгоценные металлы. Live Science.com 7 сентября, , 2011, .
- Мотт, С. М. Размер материи: почему свойства меняются в наномасштабе. Йельская национальная инициатива.
- Томсон, В. О равновесии пара на искривленной поверхности жидкости.
Лондонский, Эдинбургский и Дублинский философский журнал и научный журнал. 1871 , 42, 448. - Лу, Х.М., et al. Температуры плавления нанокристаллов, зависящие от размера, формы и размерности.
 Физическая химия С. 2009 , 113, 7598-7602.
Физическая химия С. 2009 , 113, 7598-7602. - Шмид, Г., Коран, Б. Наночастицы золота: синтез, структуры, электроника и реакционная способность. Журнал неорганической химии. 2003 , 17, 3081-3098.
- Йирка, Б. Исследователи, стремящиеся заново определить разницу между твердыми телами и жидкостями. Phys.org, 8 апреля, 2013 .
- Фардин, М.Отвечая на вопрос, за который я получил Шнобелевскую премию: кошки жидкие? The Conversation, 8 ноября, , 2017, .
- Такаги, М. Исследование дифракции электронов перехода жидкость-твердое тело в тонкие металлические пленки. Журнал Физического общества Японии . 1954 , 9, 359-363. DOI: 10.1143 / JPSJ.9.359.
- Sun, J., et al. Жидкоподобная псевдоупругость кристаллических частиц серебра размером менее 10 нм. Природные материалы. 2014 , 13, 1007-1012.
Можно ли расплавить золото пропаном?
Пламя пропана достаточно горячее, чтобы плавить чистое золото. Он также будет плавить сплавы золота, но процесс плавления не отделяет золото от других элементов, таких как серебро или медь. Золото — один из самых дорогих элементов в мире, и его широко используют в ювелирных изделиях. Старые золотые украшения можно переработать, расплавив их, чтобы использовать их в других целях. Есть несколько различных методов плавления золота, и они должны выполняться профессионалом.
Он также будет плавить сплавы золота, но процесс плавления не отделяет золото от других элементов, таких как серебро или медь. Золото — один из самых дорогих элементов в мире, и его широко используют в ювелирных изделиях. Старые золотые украшения можно переработать, расплавив их, чтобы использовать их в других целях. Есть несколько различных методов плавления золота, и они должны выполняться профессионалом.
Физические свойства золота
Золото — это металлический элемент с атомным номером 79.Это очень хороший проводник тепла и электрического тока, поэтому его часто используют в качестве проводов на печатных платах. Золото имеет очень высокую температуру плавления — 1 943 градуса по Фаренгейту (1062 градуса по Цельсию). Это означает, что плавление золота может быть достигнуто только с помощью пламени, достигающего этой температуры.
Пропан
Пропан — горючее топливо, состоящее из трех атомов углерода и восьми атомов водорода.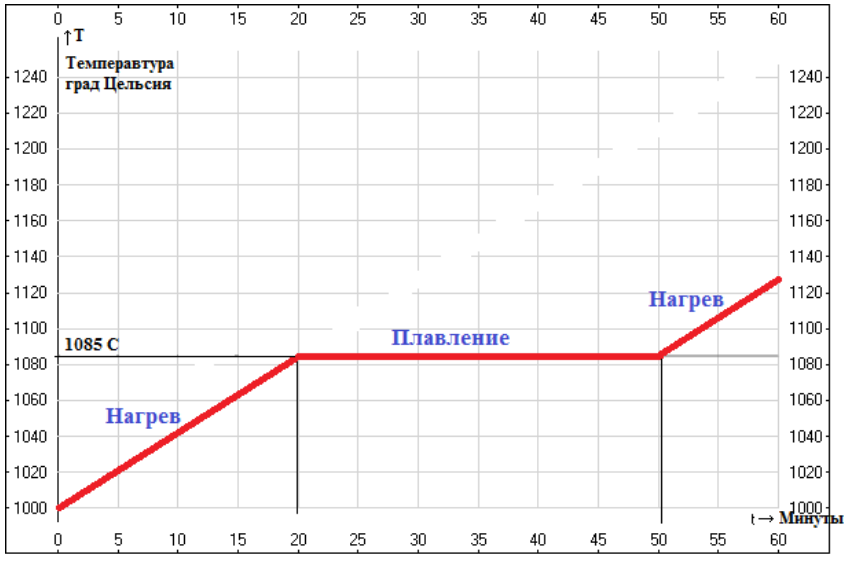 Обычно его получают в небольших цилиндрах и используют для различных целей, включая приготовление пищи и нагревание.Максимальная температура пламени, которую можно получить с помощью пропана, составляет 1 979 градусов Цельсия (3595 градусов по Фаренгейту). Он достаточно горячий, чтобы нагреть тигель и расплавить чистое золото, а также золотые сплавы, обычно используемые в ювелирных изделиях.
Обычно его получают в небольших цилиндрах и используют для различных целей, включая приготовление пищи и нагревание.Максимальная температура пламени, которую можно получить с помощью пропана, составляет 1 979 градусов Цельсия (3595 градусов по Фаренгейту). Он достаточно горячий, чтобы нагреть тигель и расплавить чистое золото, а также золотые сплавы, обычно используемые в ювелирных изделиях.
Плавка золота с помощью горелки
Плавка золота должна выполняться квалифицированным персоналом, имеющим необходимую защитную одежду. Золото помещают в тигель, который представляет собой контейнер, способный выдерживать температуры выше точки плавления золота.Тигли, в которых плавят золото, обычно делают из графита. Тигель помещают на огнестойкую поверхность, и горелку направляют на золото внутри тигля. Золото должно расплавиться в течение нескольких минут.
Плавление золотых сплавов
Золотые украшения обычно не изготавливают из чистого 24-каратного золота, которое слишком мягкое, чтобы быть прочным. Золотые изделия ниже 24 карат не являются чистыми и содержат небольшой процент серебра, меди или цинка. Добавление этих элементов немного изменяет температуру плавления, что означает, что пропановая горелка должна быстрее плавить золото более низкой чистоты.Например, 18-каратное золото имеет температуру плавления 1700 градусов по Фаренгейту (926 градусов по Цельсию), а 14-каратное золото имеет температуру плавления 1615 градусов по Фаренгейту (879 градусов по Цельсию).
Золотые изделия ниже 24 карат не являются чистыми и содержат небольшой процент серебра, меди или цинка. Добавление этих элементов немного изменяет температуру плавления, что означает, что пропановая горелка должна быстрее плавить золото более низкой чистоты.Например, 18-каратное золото имеет температуру плавления 1700 градусов по Фаренгейту (926 градусов по Цельсию), а 14-каратное золото имеет температуру плавления 1615 градусов по Фаренгейту (879 градусов по Цельсию).
Ученые плавят золото при комнатной температуре
Большинство металлов имеют очень высокие температуры плавления, не в последнюю очередь золото, которое превращается в жидкость при температурах выше 1 947 градусов по Фаренгейту (1064 градуса Цельсия).
Но теперь исследователи из Технологического университета Чалмерса в Швеции нашли способ плавить золото при комнатной температуре.Неожиданное открытие произошло, когда исследователи изучали образцы золота с помощью электронного микроскопа (ЭМ).
В отличие от оптических микроскопов, в которых используется видимый свет и система линз для увеличения небольших объектов, электромагнитные микроскопы используют электроны для получения изображений очень маленьких объектов.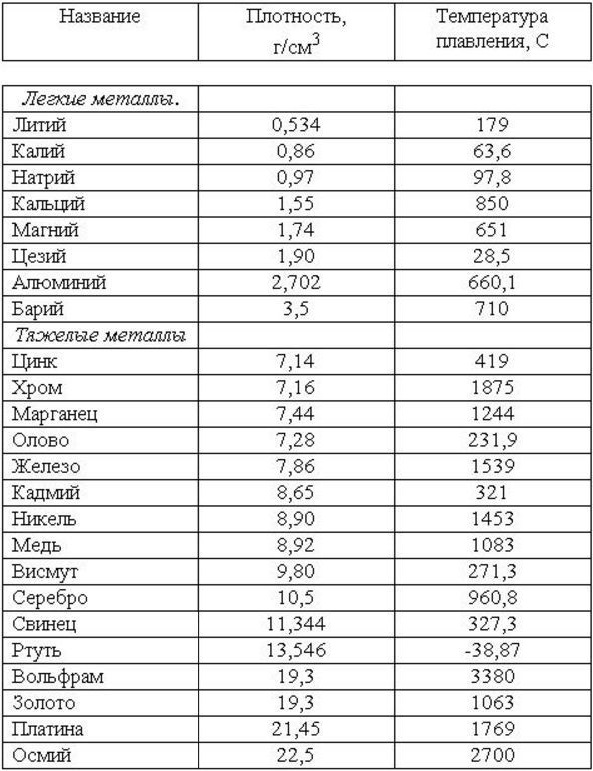 Фактически, с помощью этой техники можно изучать отдельные атомы.
Фактически, с помощью этой техники можно изучать отдельные атомы.
В ходе эксперимента Людвиг де Кнуп из физического факультета Чалмерса поместил небольшой кусочек золота в электронный микроскоп, чтобы увидеть, как электрическое поле влияет на атомы золота.Он постепенно увеличивал электрическое поле, используя максимальное увеличение.
«Мы хотели посмотреть, что происходит с золотом, когда оно находится под воздействием чрезвычайно сильного электрического поля», — сказал де Кнуп Newsweek . «Известный эффект воздействия таких сильных электрических полей на металлы состоит в том, что они испаряются, то есть выкипают из твердого металла».
Когда он изучал атомы в записях, сделанных с помощью микроскопа, он заметил нечто совершенно неожиданное — поверхностные слои золота расплавились, несмотря на то, что они находились при комнатной температуре.
«Только позже, когда мы проанализировали данные и записанные фильмы, мы поняли, что стали свидетелями чего-то нового и захватывающего», — сказал он.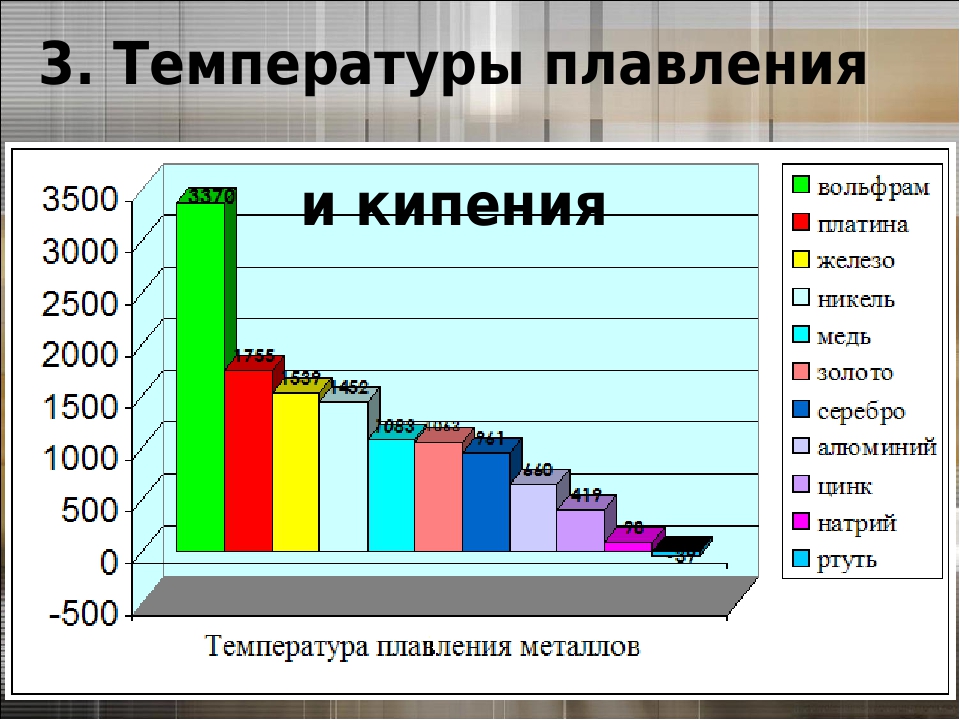 «Большой сюрприз в нашей работе заключается в том, что несколько внешних атомных поверхностных слоев золота расплавляются перед испарением. Далее мы поняли, что можем контролируемым образом переключать структуру с плавления поверхности обратно на упорядоченную, переключая электрическое поле».
«Большой сюрприз в нашей работе заключается в том, что несколько внешних атомных поверхностных слоев золота расплавляются перед испарением. Далее мы поняли, что можем контролируемым образом переключать структуру с плавления поверхности обратно на упорядоченную, переключая электрическое поле».
«Это необычное явление, которое дает нам новые фундаментальные знания о золоте», — сказал он в заявлении.
На иллюстрации показаны атомы золотого конуса, подвергнутые воздействию сильного электрического поля. Мы также видим поле (вокруг кончика конуса), которое возбуждает атомы золота. Они разрывают практически все связи друг с другом, и поверхностные слои начинают плавиться. Александр Эриксон По словам исследователей, атомы золота возбудились под действием электрического поля, которое заставило их внезапно потерять свою упорядоченную структуру, разорвав связи между ними. Было установлено, что электрическое поле вызывает образование дефектов в поверхностных слоях золота, плавление поверхности.
«Мы тесно сотрудничали с теоретиками, которые в ходе моделирования обнаружили, что при таких высоких электрических полях атомы на поверхности гораздо более слабо связаны друг с другом и поэтому могут свободно перемещаться», — сказал де Кнуп. «Важно отметить, что только 2-3 крайних атомных слоя испытывают электрическое поле, дальше в золотой конус электрическое поле равно нулю, а атомы упорядочены и структурированы обычным образом. Это важное отличие по сравнению с плавлению золота за счет повышения температуры.«
Группа также предполагает, что наблюдение может быть связано с явлением, известным как« низкоразмерный фазовый переход », согласно статье, описывающей открытие, опубликованной в журнале Physical Review Materials .
Последние результаты могли иметь По словам исследователей, значительные последствия для области материаловедения, открывающие возможности для различных приложений в будущем.
«В первую очередь, открытие важно для фундаментальной науки», — сказала Эва Олссон, другой автор исследования из Чалмерса. .«Все, что дает нам новые знания о том, как в данном случае ведет себя металл, интересно и важно. Мы могли бы увидеть ряд возможных применений. Возможность управлять несколькими атомными слоями металла таким образом могла бы для Например, открываются новые возможности для применения в датчиках, катализаторах или полевых транзисторах, или для новых концепций бесконтактных компонентов. Важно распространять новости об эффекте, поскольку он может вдохновить на создание новых приложений ».
.«Все, что дает нам новые знания о том, как в данном случае ведет себя металл, интересно и важно. Мы могли бы увидеть ряд возможных применений. Возможность управлять несколькими атомными слоями металла таким образом могла бы для Например, открываются новые возможности для применения в датчиках, катализаторах или полевых транзисторах, или для новых концепций бесконтактных компонентов. Важно распространять новости об эффекте, поскольку он может вдохновить на создание новых приложений ».
Новый процесс плавления золота при комнатной температуре.
По мере увеличения напряжения на атомном уровне начинают происходить странные вещи.Особенно это касается атомов золота. Ученым из технологического университета Чалмерса удалось расплавить поверхность золотого объекта при комнатной температуре. Золото в чистом виде — это яркий, слегка красновато-желтый, плотный, мягкий, ковкий и пластичный металл. Температура плавления золота 1064,18 градуса по Цельсию. Для практического использования золото обычно легируют неблагородными металлами для использования в ювелирных изделиях, изменяя его твердость и пластичность, температуру плавления, цвет и другие свойства. Новый способ плавления золота был обнаружен, когда исследователь Людвиг де Кнуп изучал фрагмент золота с помощью электронного микроскопа.де Кнуп отметил, что на самом высоком уровне увеличения с увеличенным электрическим полем атомы золота менялись. При более внимательном изучении записей, сделанных под микроскопом, де Кнуп заметил, что поверхностные слои золота плавятся при комнатной температуре. Это было явление, которое ранее не наблюдалось. Это побудило де Кнупа заявить в исследовательской заметке: «Я был действительно ошеломлен этим открытием. Это необычное явление, и оно дает нам новые фундаментальные знания о золоте».
Золотая монета
Новый способ плавления золота был обнаружен, когда исследователь Людвиг де Кнуп изучал фрагмент золота с помощью электронного микроскопа.де Кнуп отметил, что на самом высоком уровне увеличения с увеличенным электрическим полем атомы золота менялись. При более внимательном изучении записей, сделанных под микроскопом, де Кнуп заметил, что поверхностные слои золота плавятся при комнатной температуре. Это было явление, которое ранее не наблюдалось. Это побудило де Кнупа заявить в исследовательской заметке: «Я был действительно ошеломлен этим открытием. Это необычное явление, и оно дает нам новые фундаментальные знания о золоте».
Золотая монета$ 100 24 карата будет выпущена в апреле 2017 года.
Монетный двор США
Процесс осуществлялся путем воздействия на атомы золотого конуса сильного электрического поля. Поле возбуждает атомы золота, разрывая их связи друг с другом и заставляя поверхностные слои плавиться. Произошло то, что электрическое поле заставляло атомы золота терять свою упорядоченную структуру и высвобождать почти все свои связи друг с другом. Что еще представляло интерес, так это то, что с помощью дальнейших испытаний можно было также переключать золото между твердой и расплавленной структурой.Основываясь на ряде теоретических расчетов, проведенных исследователями, теперь можно плавить золото при комнатной температуре на основе процесса, называемого низкоразмерным фазовым переходом. Это нужно будет проверить в большем масштабе. Как бы то ни было, эти открытия могут открыть новые возможности в материаловедении. Исследование было опубликовано в журнале Physical Review Materials с исследовательской статьей под названием «Управляемое электрическим полем обратимое переключение порядка-беспорядка на поверхности металлического наконечника».”
Что еще представляло интерес, так это то, что с помощью дальнейших испытаний можно было также переключать золото между твердой и расплавленной структурой.Основываясь на ряде теоретических расчетов, проведенных исследователями, теперь можно плавить золото при комнатной температуре на основе процесса, называемого низкоразмерным фазовым переходом. Это нужно будет проверить в большем масштабе. Как бы то ни было, эти открытия могут открыть новые возможности в материаловедении. Исследование было опубликовано в журнале Physical Review Materials с исследовательской статьей под названием «Управляемое электрическим полем обратимое переключение порядка-беспорядка на поверхности металлического наконечника».”Исследователи плавят золото при комнатной температуре с помощью электрических полей
Ученые из Технологического университета Чалмерса в Швеции открыли, как плавить золото при комнатной температуре. Эксперименты исследователя заключались в приложении электрического поля к коническому объекту из золота.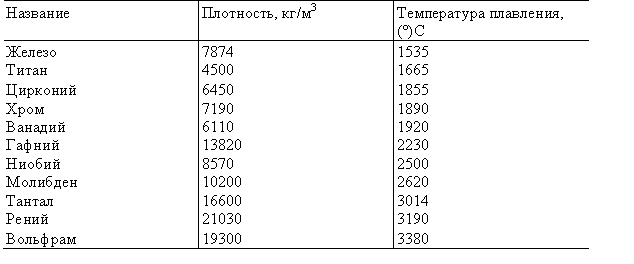 Используемые объекты представляют собой наноконусы из чистого золота с диаметром кончика чуть более двух нанометров.
Используемые объекты представляют собой наноконусы из чистого золота с диаметром кончика чуть более двух нанометров.Наблюдения, проведенные с помощью просвечивающего электронного микроскопа, показали, что молекулярная структура поверхности золотого объекта начала терять порядок, который они ранее поддерживали.Они обнаружили три слоя атомов золота, которые начали двигаться, что является явным свидетельством процесса плавления.
До этого исследователи использовали электрические поля для сублимации золота из твердого тела в газ.
Ученые, охваченные благоговением перед невиданным ранее феноменом, также обнаружили, что уменьшение электрического поля может вернуть золотой объект в его первоначальное твердое состояние. Команда Chalmers также планирует узнать, можно ли применить этот метод к более твердым типам металлов.
Их результаты были опубликованы в виде статьи в журнале « Physical Review Materials ».
Тепло
Плавить золото — дело непростое. Температура плавления чистого золота составляет 1064 градуса по Цельсию (или 1948 градусов по Фаренгейту), а температура кипения этого элемента составляет колоссальные 2700 градусов по Цельсию (5173 градуса по Фаренгейту). На практике температура плавления золотых предметов и руды может значительно варьироваться в зависимости от присутствия других металлических элементов.
Температура плавления чистого золота составляет 1064 градуса по Цельсию (или 1948 градусов по Фаренгейту), а температура кипения этого элемента составляет колоссальные 2700 градусов по Цельсию (5173 градуса по Фаренгейту). На практике температура плавления золотых предметов и руды может значительно варьироваться в зависимости от присутствия других металлических элементов.
Однако исследователи из Института Чалмерса указывают на альтернативный способ разжижения твердых металлов, таких как золото. Компьютерное моделирование и изображения с микроскопа показывают, что результаты эксперимента были получены не из-за повышения температуры, а из-за приложения сильных электрических полей к поверхности золотых предметов. Электрическое поле, когда-то достаточно высокое, нарушает кристаллическую структуру золота, заставляя атомы перемещаться и разжижаться.
Кроме того, золото возвращается в свое кристаллическое твердое состояние после уменьшения напряженности электрического поля.
Практические соображения
Продемонстрированный принцип плавления золота и возврата к его первоначальной структуре без применения тепла может проложить путь к новым интересным разработкам. Эта новая технология может применяться в самых разных областях, от химической инженерии до оптики. Некоторые из перспективных новых технологий, которые могут быть получены из плавления в электрическом поле, включают датчики, бесконтактные компоненты в машинах и химические катализаторы для различных применений.
Эта новая технология может применяться в самых разных областях, от химической инженерии до оптики. Некоторые из перспективных новых технологий, которые могут быть получены из плавления в электрическом поле, включают датчики, бесконтактные компоненты в машинах и химические катализаторы для различных применений.
Однако, несмотря на захватывающие перспективы, практическое применение нового открытия на данный момент далеко не ясно, и одной из проблем является масштаб, которого необходимо достичь, чтобы стать практической технологией.
Среди этих масштабных задач можно отметить размер энергетического поля, необходимого для плавки золота. Для плавления первых двух или трех атомных слоев в наноконусах требовалось более 25 000 000 000 вольт на метр, даже если они использовали максимум 100 вольт. А поскольку золото мягче большинства металлов, напряжение, необходимое для плавления других металлов таким способом, может быть даже выше.
Использованные золотые конусы также были очень маленькими.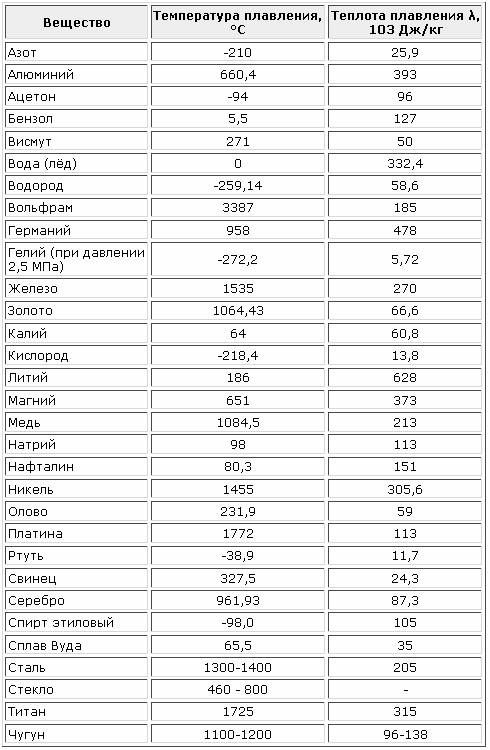 Это означает более сложную задачу по масштабированию этой новой технологии. Двигатели энергетического поля, которые могут плавить большие металлические объекты, вероятно, слишком непрактичны, чтобы их можно было реально рассматривать из-за отсутствия достаточного напряжения, чтобы это стало реальностью. Реальные проекты, основанные на этом принципе, сделали бы их в значительной степени идеальными для нанотехнологий, где существующие механизмы слишком малы, чтобы люди могли их увидеть.
Это означает более сложную задачу по масштабированию этой новой технологии. Двигатели энергетического поля, которые могут плавить большие металлические объекты, вероятно, слишком непрактичны, чтобы их можно было реально рассматривать из-за отсутствия достаточного напряжения, чтобы это стало реальностью. Реальные проекты, основанные на этом принципе, сделали бы их в значительной степени идеальными для нанотехнологий, где существующие механизмы слишком малы, чтобы люди могли их увидеть.
Ученые нашли способ плавить золото при комнатной температуре.
Для плавления золота обычно требуется температура выше 1064 ° C (1947 ° F), но физика никогда не бывает такой простой.Группа исследователей нашла способ плавить золото при комнатной температуре с помощью электрического поля и электронного микроскопа.
Хотя мы все знакомы с явлением плавления, большинство из нас на самом деле не задумывается о физике этого процесса. По сути, когда что-то тает, все, что происходит, — это разрыв связей между его молекулами, и они начинают двигаться более свободно. Например, они могут перейти от хорошо упорядоченной структуры кубика льда к менее упорядоченному состоянию бесформенной лужи воды.
Например, они могут перейти от хорошо упорядоченной структуры кубика льда к менее упорядоченному состоянию бесформенной лужи воды.
Тепло — обычный спусковой механизм для изменений, но не единственный — давление тоже играет роль. Эксперименты с этими условиями позволили ученым в последнее время делать самые разные неожиданные вещи, например, заставлять воду замерзать при температурах, значительно превышающих ее обычную точку кипения.
В новом исследовании исследователи проверили еще один триггер: электрическое поле. Команда поместила небольшой кусочек золота в электронный микроскоп и наблюдала его с максимальным увеличением. Затем они медленно увеличили напряженность электрического поля, чтобы увидеть, как реагируют атомы золота.
Когда они потом посмотрели на данные, исследователи поняли, что электрическое поле возбуждало атомы в верхних слоях золота. Это заставило их вырваться из основной массы объекта, эффективно расплавив материал при комнатной температуре. Это изменение было также обратимым, поскольку отключение электрического поля может снова затвердеть золото.
«Я был действительно ошеломлен этим открытием, — говорит Людвиг де Кнуп, первый автор исследования. «Это необычное явление, которое дает нам новые фундаментальные знания о золоте.»
Команда не совсем уверена, как работает метод плавления золота при температуре окружающей среды, но это может быть связано с явлением, известным как низкоразмерный фазовый переход. Исследователи планируют изучить это в будущем, что может помочь разблокировать некоторые приложения для открытия.
«Поскольку мы можем контролировать и изменять свойства поверхностных слоев атомов, это открывает двери для различных видов приложений», — говорит Эва Олссон, автор исследования. «Например, технология могут использоваться в различных типах сенсоров, катализаторов и транзисторов.Также могут появиться возможности для новых концепций для бесконтактных компонентов ».
Исследование было опубликовано в журнале« Physical Review Materials ».
Источник: Технологический университет Чалмерса
Шведские исследователи« плавят золото при комнатной температуре »Kids News Статья
На рисунке показаны атомы золотого конуса, подвергнутые воздействию сильного электрического поля.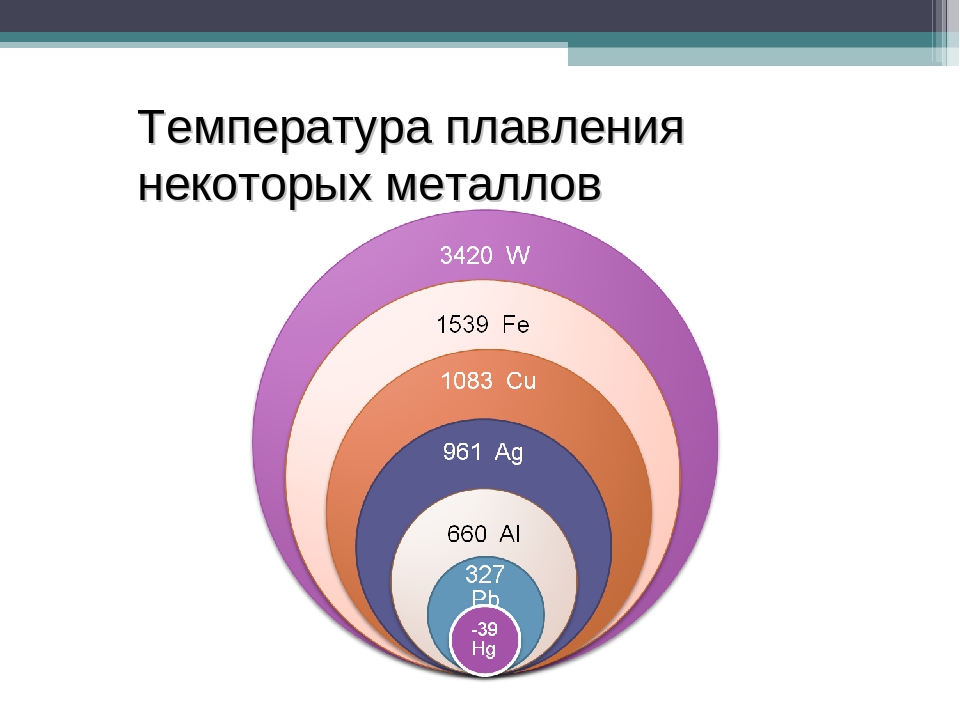 Мы также видим поле (вокруг кончика конуса), которое возбуждает атомы золота. Они разрывают почти все свои связи друг с другом, и поверхностные слои начинают плавиться. .(Фото: Александр Эриксон)
Мы также видим поле (вокруг кончика конуса), которое возбуждает атомы золота. Они разрывают почти все свои связи друг с другом, и поверхностные слои начинают плавиться. .(Фото: Александр Эриксон)В чистом виде золото обычно требует температуры 1 948 градусов по Фаренгейту (1064 градуса Цельсия) для разжижения. Теперь команда исследователей из Технологического университета Чалмерса в Швеции, возможно, наткнулась на способ плавления драгоценного металла при комнатной температуре.
Для тех, кто не понимает физику явления плавления, вот краткое руководство. Твердые тела, как вы, возможно, знаете, могут сохранять размер и форму при постоянных условиях, потому что их атомы или молекулы не имеют достаточно энергии для разрыва.Когда вводится внешний источник энергии, он возбуждает молекулы и вызывает разрушение плотной структуры, позволяя им начать свободное движение. Это приводит к изменению состояния с твердого на жидкое, или к тому, что мы называем плавлением. Исследователи в основном используют тепло или, в некоторых случаях, давление, чтобы вызвать изменение. Однако шведской команде удалось совершить подвиг, используя другой источник энергии — электрическое поле.
Однако шведской команде удалось совершить подвиг, используя другой источник энергии — электрическое поле.
Для своего исследования доктор Людвиг де Кнуп и его команда поместили образец золота под электронный микроскоп (ЭМ). В отличие от оптических микроскопов, которые зависят от видимого света, ЭМ используют пучок ускоренных электронов в качестве источника освещения, что делает их достаточно мощными, чтобы видеть отдельные атомы. Чтобы выяснить, влияет ли электрическое поле на молекулы металла, исследователи постепенно увеличивали его интенсивность, используя максимальное увеличение.
«Мы хотели посмотреть, что происходит с золотом, когда оно находится под воздействием чрезвычайно сильного электрического поля», — сказал де Кноп « Newsweek ».«Известный эффект воздействия таких сильных электрических полей на металлы состоит в том, что они испаряются, то есть выкипают из твердого металла».
Изучив атомы на записях, сделанных с ЭМ, де Кнуп заметил кое-что очень неожиданное — поверхностные слои образца золота расплавились, хотя эксперимент проводился при комнатной температуре. Это изменение было легко отменить, просто отключив электрическое поле.
Сравнение оптического микроскопа и электронного микроскопа (Источник: эмбриология.med.unsw.edu.au/CC BY-SA 3.0)«Только позже, когда мы проанализировали данные и записанные фильмы, мы поняли, что стали свидетелями чего-то нового и захватывающего», — сказал де Кноп. «Большим сюрпризом в нашей работе было то, что несколько внешних атомных поверхностных слоев золота расплавились, прежде чем испариться».
Исследователи, опубликовавшие свои результаты в журнале Physics Review Materials 22 августа 2018 года, полагают, что электрическое поле заставило атомы золота возбудиться и потерять свою структуру, нарушив прочную связь между ними.Однако де Кнуп сказал: «Это]. Важно отметить, что только 2-3 крайних атомных слоя испытывают электрическое поле, дальше в золотой конус электрическое поле равно нулю, а атомы упорядочены и структурированы в своих местах.


 И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.
И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.


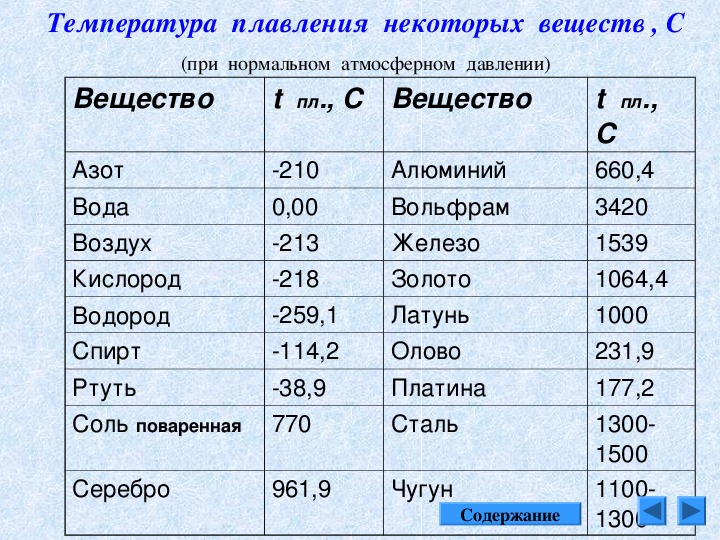
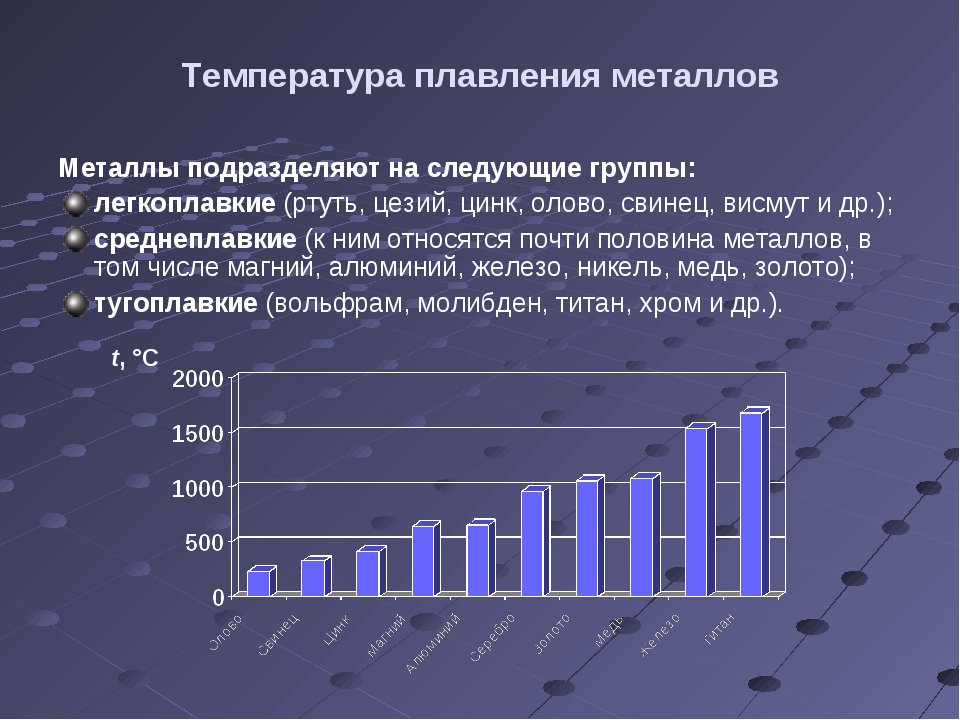 Бронза не утратила своей актуальности даже с наступлением века железа, например, ещё в начале 20 века стволы пушек изготавливали из так называемой орудийной бронзы. Температура, при которой бронза начинает плавиться, составляет 930 — 1140 градусов.
Бронза не утратила своей актуальности даже с наступлением века железа, например, ещё в начале 20 века стволы пушек изготавливали из так называемой орудийной бронзы. Температура, при которой бронза начинает плавиться, составляет 930 — 1140 градусов. Поэтому он не теряет своей прочности после нескольких лет эксплуатации, как другие металлы. В настоящее время этот сплав является основой самолётостроения.
Поэтому он не теряет своей прочности после нескольких лет эксплуатации, как другие металлы. В настоящее время этот сплав является основой самолётостроения. Но в этом случае невозможно достигнуть относительно высоких температур, поэтому он годится для переплавки сплавов меди, которые обладают меньшей температурой плавления, чем чистая медь.
Но в этом случае невозможно достигнуть относительно высоких температур, поэтому он годится для переплавки сплавов меди, которые обладают меньшей температурой плавления, чем чистая медь.


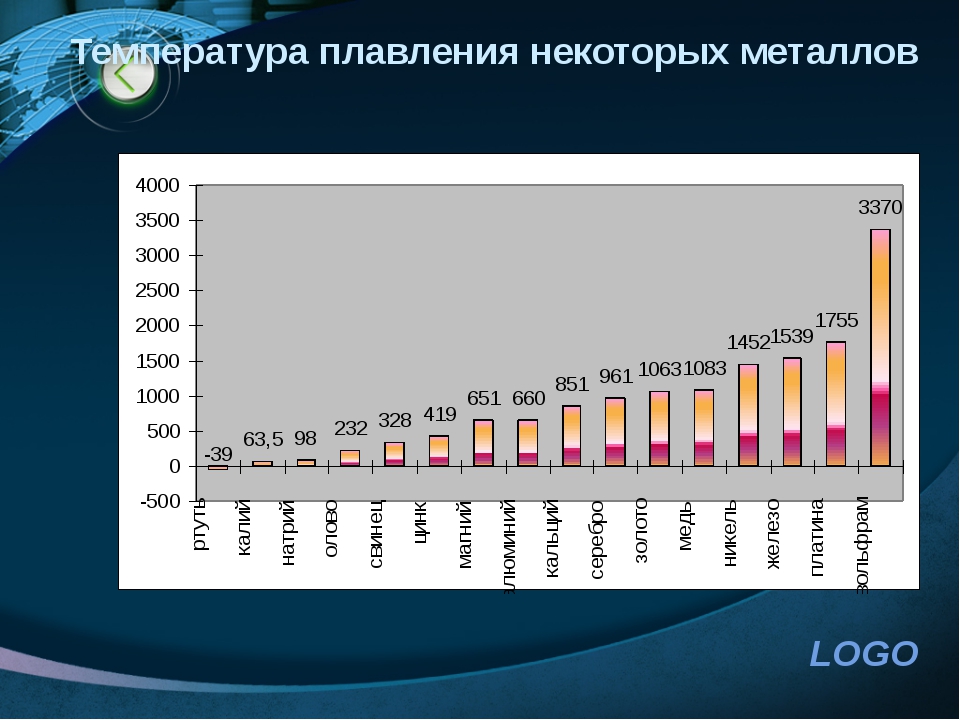

 Последующий нагрев содействует изменению цвета, что происходит при удалении верхнего оксида.
Последующий нагрев содействует изменению цвета, что происходит при удалении верхнего оксида.

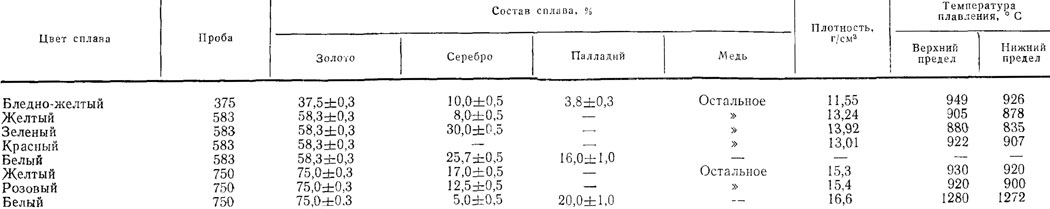 Физическая химия С. 2009 , 113, 7598-7602.
Физическая химия С. 2009 , 113, 7598-7602.