свойства элемента и его сфера применения
Все металлы имеют свои особые свойства и характеристики. Еще со школьной программы многие из нас знают, что каждый металл имеет свою температуру плавления. В термодинамическом процессе кристаллическая решетка в металлах разрушается, и они из твердого состояния переходят в жидкое.Металлы делятся на группы, в зависимости от их температуры плавления — легкие, средние и тугоплавкие. К первой группе легкоплавких металлов относится олово, а вот при какой температуре плавится этот редкий химический элемент мы и попытаемся выяснить.
Олово
Редкий металл олово в периодической таблице Д. Менделеева занимает 50-е место, относится к главной подгруппе IV группы в таблице пятого периода. Его масса составляет 118,710, в чистом виде он выглядит как серебристо-белый металл, мягкий, пластичный и ковкий, он отличается высокой коррозийной стойкостью. Редкий элемент по распространению в земной коре занимает 47-е место.
Основные месторождения в мире находятся в странах Юго-Восточной Азии — Китае, Таиланде, Малайзии, Индонезии. Есть также крупные месторождения в странах Южной Америки и Австралии. На территории России запасы руды олова есть на Чукотке, в Хабаровском и Приморском крае, в Якутии.
Немного истории
Людям этот редкий металл стал знаком еще до нашей эры, поскольку упоминается еще в Библии. Он был малодоступен людям, поэтому стоил очень дорого, изделия из олова встречаются редко среди изделий археологических раскопок Древнего Рима и Греции.Его начали применять в бронзовом веке, олово в то время являлось стратегическим металлом, поскольку он входил в состав бронзовых изделий. Рецептура сплава меди и олова сохранилась и сейчас, но в настоящее время стали добавлять еще алюминий, свинец и кремний. Полученный сплав был очень твердым, замечательно отливался в формы, легко ковался и обрабатывался. В то далекое время бронза считалась наиболее прочным металлом, который был известен людям того времени.
Из этого сплава делали украшения, посуду, но стоила она очень дорого. С редким элементом связано многое в длительном периоде развития общества с момента открытия олова.
Свойства олова, его температура плавления
В природе редкий металл может быть в двух формах нахождения — в горных породах и минералах. Чаще всего элемент встречается в виде оловянного камня — окисного соединения. Раньше его выплавляли из руды, которую находили в верхних слоях земной коры. В настоящее время такие полезные ископаемые практически исчезли, поэтому процесс добычи олова стал намного сложней.
- До того момента, когда металл попадает в плавильное отделение, руда и россыпи, в составе которых есть олово проходят процесс обогащения. После этого концентрат направляют в обжиговые печи и только затем плавят.
- Редкий элемент имеет невысокую планку плавления, процесс плавления начинается при +231,9оС, при температуре +231,0оС металл остается твердым. Даже в охлажденном состоянии он легко гнется, а при нагревании становится податливым как пластилин. Процесс кипения олова начинается, когда температура во много раз превышает показатели плавления — 2630оС.
- Элемент бывает белого и серого цвета, более темный цвет он приобретает, когда переходит в порошкообразное состояние, в порошке плотность элемента значительно ниже, чем когда он находится в твердом состоянии.
В процессе плавки используются шлаки, флюсы, присадки для того, чтобы получить нужного сорта и качества металл. Низкая температура плавления сделала его стратегически важным металлом. Он легко может участвовать в образовании сплавов с другими материалами, благодаря низкой температуре плавления. В конечном итоге сплавы легко обрабатываются, затем они участвуют в соединении конструктивных узлов и деталей с хорошим герметичным швом.
Применение олова
- Этот элемент часто используют в качестве защитного слоя в атомной промышленности.

- Его также применяют в стекольной промышленности как полировку для стекла, оно в жидком состоянии выливается в емкость с расплавом.
- В печатной промышленности используется сплав олова с сурьмой и свинцом для создания печатного шрифта.
- Оловом прокатывают фольгу, элемент применяют в производстве труб и различных деталей, чтобы придать им антикоррозийную стойкость, ведь олово не ржавеет.
- Редкий элемент отлично проводит тепло, например, в производстве консервных банок он часто используется. В такой таре можно длительное время хранить продукты, поскольку олово нетоксичный элемент. Посуда долгий промежуток времени не подвергается разрушению.
- В ткацкой промышленности он также используется, но только соли металла. В основном это находит применение в производстве натурального шелка и для печати на ситцевой ткани.
- Элемент нашел применение и в медицине, например, в стоматологии для армирования некоторых видов пломб. Редкий металл есть даже в организме человеке, его нехватка может отрицательно сказаться на росте, по этой причине он начинает замедляться.
Вывод
На сегодняшний день олово находит применение во многих отраслях промышленности, поскольку металл обладает целым рядом уникальных свойств. Спустя тысячелетия редкий химический элемент все так же востребован как в чистом виде, так и в сплавах с другими металлами.
Оцените статью: Поделитесь с друзьями!Олово температура плавления — Справочник химика 21
Изобразите фазовую диаграмму для биметаллического сплава свинца и олова с эвтектическим составом, содержа-шим 62% олова. Температура плавления свинца 327 С, олова 232°С температура эвтектики 180°С. [c.401]Удельный вес 7,3 (Р)—олово и 7,75 (а) олово температура плавления 231,9° С. [c.226]
Приготовление сплава Вуда.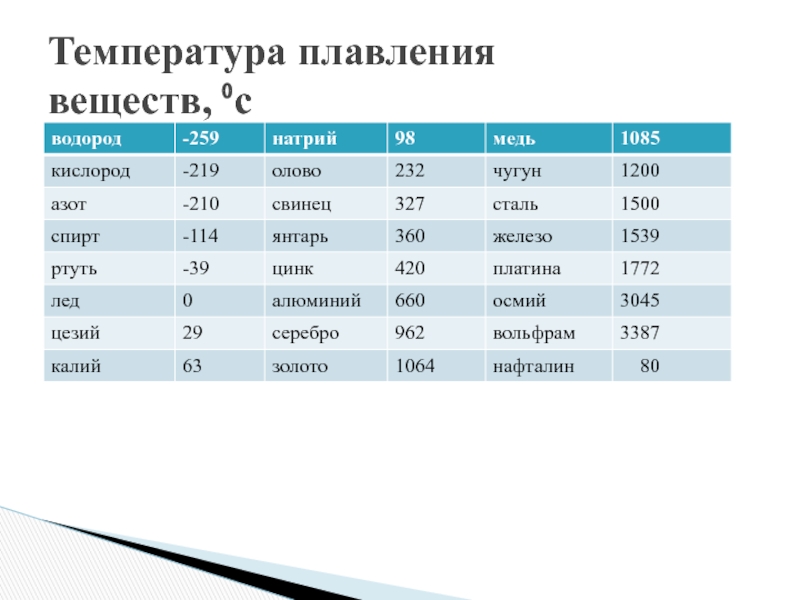 Для приготовления этого сплава смешивают в определенных отношениях и расплавляют необходимые для этого металлы. Например, можно пользоваться следующим рецептом олово (температура плавления 232° С) — 10 г, свинца (температура плавления 328° С) —10 г, кадмия (температура плавления 321° С)—7 г, висмута (температура плавления 271°С)—40г, [c.252]
Для приготовления этого сплава смешивают в определенных отношениях и расплавляют необходимые для этого металлы. Например, можно пользоваться следующим рецептом олово (температура плавления 232° С) — 10 г, свинца (температура плавления 328° С) —10 г, кадмия (температура плавления 321° С)—7 г, висмута (температура плавления 271°С)—40г, [c.252]
Кроме ртути резкое уменьшение прочности и пластичности цинковых монокристаллов вызывают другие легкоплавкие металлы, например галлий и олово (температура плавления 30 и 232 С). Присутствие пленки жидкого свинца заметно не изменяет механических свойств цинка, если растяжение проводится 2 с небольшой скоростью. При раство- / рении олова в пленке жидкого евин- ца, нанесенной на поверхность цин- кового монокристалла, разрушение
Бронза — сплав меди с оловом. Температура плавления оловянистых бронз 900—950° С. Имеются также безоловянистые бронзы, представляющие собой сплавы меди с алюминием, с марганцем или с другими элементами. Температура плавления безоловянистых бронз 950—10802 С. [c.37]
Изготовление припоя или третника. Отвешивают на 2 вес. ч. олова 1 вес. ч. свинца. Навески металлов при помешивании расплавляются в железном тигельке. Сначала плавится олово (температура плавления 232°С), а затем —свинец (температура плавления 328° С) полученный сплав выливают в сделанную из бумаги форму (на стеклянную трубку навертывают плотную бумагу, обвязывают ниткой, снимают с трубки, закрывают пробкой или отрезком деревянной палочки).
Металлические покрытия горячим методом наносят на изделие или заготовку путем их погружения на несколько секунд в ванну с расплавленным металлом. Этим способом на изделия наносят цинк (температура плавления 419°С), олово (температура плавления 232°С), свинец (температура плавления 327°С), алюминий (температура плавления 658°С), т. е. металлы, имеющие низкую температуру плавления.
Практически этим методом железо защищается от коррозии цинком (температура плавления 419°), оловом (температура плавления 232°) и свинцом (температура плавления 327°). [c.285]
Если нужно изготовлять изделия очень сложной конфигурации, что требует применения дорогостоящих стальных форм, то в случае термотвердеющих смол можно обойтись формами из специальных сплавов, которые используют для изготовления только одной отливки и затем расплавляют. Температура плавления материала формы должна превышать температуру твердения смолы примерно на 20 » G. Если температура твердения 140° С, то можно использовать форму из сплава 16% висмута, 36% свинца и 48% олова температура плавления такого сплава составляет 155° С. Отдельные части такой формы легко отливаются, после чего форму собирают.
При какой температуре плавится и кристаллизуется олово
К одному из самых первых металлов, открытых в древности, относится олово. Оно имеет серебристо-белый цвет с небольшой массой. Посуда из него прекрасно сохраняет запах, а также вкус напитков. Данный металл использовался намного раньше открытого впоследствии железа, а его сплав с медью (бронза) является первым сплавным веществом, созданным человеком. Это получилось из-за того, что температура плавления олова весьма низкая, что позволяло обрабатывать металл еще при зарождении металлургии.
Свойства и особенности олова
Оловянные сплавы имеют малый коэффициент трения, из-за чего их используют в разнообразных антифрикционных материалов. Помимо этого, данным свойством они могут наделять и прочие вещества. Это значительно продлевает период эксплуатации механизмов, машин, значительно снижая потери на трение. К интересной особенности данного материала относится его увеличение объема на 25,6 % при температуре + 13,2 °С. Этот металл называется серым.
К интересной особенности данного материала относится его увеличение объема на 25,6 % при температуре + 13,2 °С. Этот металл называется серым.
При снижении температуры до — 33,0 °С вещество кристаллизуется и переходит в порошкообразное состояние. При взаимодействии серого и белого олова происходит передача свойств белому металлу. Разнообразные оловянные сплавы широко используются электротехнической промышленностью. На вопрос при какой температуре плавится олово существует однозначный ответ: + 231,9 °С или же 505,1 по кельвину. Это весьма удобно для радиолюбителей, ведь паять детали с такой температурой можно без особых проблем даже в домашних условиях. Температура плавления, при которой олово переходит в жидкое состояние невысока, что облегчает его использование.
Высокий интерес представляет данное вещество из-за своей хорошей коррозийной стойкости. Именно оловянное покрытие является древнейшим способом защиты разнообразных предметов из металлов, в том числе и консервных банок. Помимо этого, данный элемент имеет свойство объединять многие металлы с приданием им устойчивости к внешним воздействиям. Это используется при лужении различной посуды и прочих бытовой утвари, а также электротехниками. Оловянно-свинцовые сплавы относятся к мягким компонентам, что удобно при пайке радиотехнических деталей. Эти припои могут иметь различное количество компонентов и соответствующее обозначение. К примеру, пос-61 означает, что оловянная составляющая имеет 61 %, а свинцовая – 39 %.
Человеческое тело содержит оловянные вещества в костях, где они помогают обновлению костной ткани. Для нормальной жизнедеятельности организму необходимо получать ежедневно порядка 2-10 мг металла в сутки. Этот макроэлемент содержится в принимаемой пище, однако усваивается всего лишь до 5 % от общего поступающего количества.
Температура плавления
Особую известность имеют соединения, использующиеся в качестве припоя радиолюбителями. Температура плавления в сплаве ПОС-40 составляет + 235,0 °С. Содержащийся в припоях свинец является довольно мягким материалом, имеющий серый цвет со светлым оттенком. Он плавится при значении + 327,0 °С, что делает его идеальной составляющей для олова. Припой ПОС-61 может плавиться при температуре + 191,0 °С, чем весьма удобен для пайки небольших радиодеталей.
Температура плавления в сплаве ПОС-40 составляет + 235,0 °С. Содержащийся в припоях свинец является довольно мягким материалом, имеющий серый цвет со светлым оттенком. Он плавится при значении + 327,0 °С, что делает его идеальной составляющей для олова. Припой ПОС-61 может плавиться при температуре + 191,0 °С, чем весьма удобен для пайки небольших радиодеталей.
Специалисты знают, при какой температуре олово плавится. Данная величина составляет + 231,9 °С, а при + 231,0°С оно остается твердым. Температурный показатель кипения этого вещества намного выше – 2 600 градусов Цельсия. В зависимости от компонентов, входящих в состав оловянного сплава изменяется температурный показатель плавления. Этот материал превосходно гнется даже в холодном состоянии, а нагреваясь, он начинает приобретать свойства пластилина. Температура плавления свинца и оловянной составляющей разнится, однако их сплавы обладают широким применением. При плавке применяются специальные флюсы, шлаки, а также присадки для получения необходимой степени качества и сорта металла. Из-за его возможности расплавляться при низкой температуре он является стратегически важным сырьем. Сплавы с участием оловянного компонента очень легко обрабатываются и применяются при соединении конструктивных деталей и узлов с герметичным швом. К наиболее известным бытовым соединениям относятся припои, температура плавления в которых олова и свинца зависит от их количества.
Применение и вторичная переработка
Главным достоинством, определяющим область применения оловянного вещества, является его высокая стойкость к коррозии. Это свойство оно передает и прочим металлам, участвующим в сплаве. Данная способность противодействия химически агрессивным веществам делает материал весьма ценным при защите стальных изделий. Тончайший слой покрывает практически половину всей производимой стальной жести.
Данный металл используется при производстве тонкостенных труб, которые применяются исключительно при положительных температурных показателях. К ограничению сферы применения относится низкая температура кристаллизации олова. Бытовые изделия содержат олово в сантехническом оборудовании, разнообразной фурнитуре и прочих аксессуарах. Материал обладает высокой гигиеничностью, низким температурным показателем плавления олова, а также весьма низкой теплопроводностью по сравнению со сталью. По этим характеристикам его активно используют для изготовления умывальников и ванн.
К ограничению сферы применения относится низкая температура кристаллизации олова. Бытовые изделия содержат олово в сантехническом оборудовании, разнообразной фурнитуре и прочих аксессуарах. Материал обладает высокой гигиеничностью, низким температурным показателем плавления олова, а также весьма низкой теплопроводностью по сравнению со сталью. По этим характеристикам его активно используют для изготовления умывальников и ванн.
Это вещество присутствует в домашней посуде, ювелирных украшениях, а также небольших элементах декора и быта. Это обусловлено хорошим плавлением материала при невысокой температуре, ковкости и мягкому цвету. Бронзовые сплавы имеют отличную прочность, а также высокую стойкость к коррозии. Это делает бронзу превосходным строительно-декоративным материалом.
Помимо припоев, которые удобно расплавлять в домашних условиях и промышленном производстве, сплавы применяются даже для производства музыкальных инструментов. Из различных сплавов отливаются церковные колокола и органные трубы. От количества составляющих элементов зависит тон изделий. Невысокая температура затвердевания материала и простота обработки позволяют изготавливать уникальные изделия музыкального направления.
Для вторичной переработки используют старые консервные жестяные баночки. Они имеют защитное оловянное покрытие с некоторыми примесями. Их количество для продуктовой тары имеет строгое ограничение. Величина оловянного состава при лужении жестяной баночки не должна превышать 0,14 %, а по свинцу данный показатель составляет 0,04 %. Для безопасности здоровья дополнительно применяются специальные лаки, которые предохраняют металлическую основу от разрушения под воздействием соли, сахара, а также органических кислот. Средняя банка содержит порядка 0,5 г оловянного компонента. Для мировых масштабов это весьма внушительная цифра. Доля этого вторично использованного сырья в развитых государствах доходит до 30 %.
Олово используется практически во всех направлениях современного производства. Спустя тысячелетия после своего открытия, металл остается востребованным веществом, обладающим широким спектром уникальных свойств.
Спустя тысячелетия после своего открытия, металл остается востребованным веществом, обладающим широким спектром уникальных свойств.
Припои марки А ПОС-30ф 8мм, П -14 ф 2,8мм ТУ 48-1728138/ОПП-006-2000 ООО Дон-энергокомплект г. Ростов-на-Дону
Харакетристики:
Припой ПОС-61 в классификации припоев занимает особенное место. Это обусловлено тем, что в этом сплаве отмечается содержание канифоли, поэтому его можно с успехом использовать для лужения и пайки самых разных контрольно-измерительных приборов.Припой ПОС 61 — это по-своему универсальный материал, который идеально подойдет для любой разновидности проводов. Также отмечается, что он неплохо себя показывается при пайке микросхем. Кроме того, если нельзя во время работы допустить перегрев места пайки, то припой ПОС-61 справится с задачей куда эффективнее, чем многие другие сплавы. Производитель отмечает, что основной сферой использования припоя ПОС61 является пайка жил к полупроводниковым устройствам, выводам разъемов, медных проводов. Стоит отметить, что это оптимальный выбор для соединения следующих металлов: сталь, латунь, бронза, медь. Припой ПОС 61, если сравнивать с другими оловянно-свинцовыми припоями, представленными на рынке, имеет более высокий уровень чистоты и рассчитан на пайку электромонтажа. За счет повышенного содержания меди в припое снижается интенсивность растворения проводов из меди, а также во много раз увеличивается степень износостойкости медных стержней электрических паяльников.
Состав припоя ПОС 61: свинец (39-50%), олово (50-61%). Одновременно с этим, по ГОСТу 21930-76 главным фактором, который определяет характеристики припоя, является химический состав. Помимо свинца и олова в припое ПОС 61 содержатся следующие примеси: Sb, Cu, As, Bi, Ni, S, Zn, Al, Fe.
Харакетристики:
Припой ПОС-40 является оловянно-свинцовым припоем, поэтому его область использования довольно-таки широка. С помощью припоя этой марки осуществляется пайка железа, латуни медных проводов, элементов из оцинкованного железа с полностью герметичными швами. Именно поэтому припой активно используется в сфере электрооборудования, при ремонте медных и латунных трубопроводов, ремонте радиаторов.Припой ПОС-40 может быть использован с любым видом паяльного оборудования, поэтому, в большинстве случаев, именно он выбирается для проведения пайки и лужения различных элементов не только в локальном ремонте, но и в заводских масштабах.
Припой ПОС 40 великолепно подходит для формирования прочного (если требуется, и полностью герметичного) шва, а также для получения электроконтакта с небольшим переходным сопротивлением. За счет того, что имеет температуру плавления намного меньшую, чем соединяемые металлы, то он плавится, оставляя при этом основной металл абсолютно твердым. Компоненты будут диффундировать в основной металл, который будет растворяться в припое, за счет чего начнет формироваться промежуточная прослойка, соединяющая все элементы в одно целое после застывания.
Производители выпускает припой ПОС 40 в виде проволоки (без канифоли) и трубок (с сосновой канифолью).
Осуществлять пайку этим припоем можно простым паяльным инструментом, не опасаясь при этом перегрева элементов, потому что припой полностью расплавляется уже при температуре в 238 градусов. Если требуется припой, который будет плавиться при более низких температурах, то рекомендуется выбирать модель ПОС 61 и другие соответствующие виды.
Харакетристики:
Припой ПОС-30 — оловянно-свинцовый припой, используемый для пайки и лужения радио- и электроаппаратуры приборов с герметичными швами, печатных схем, внутренних швов и медицинских устройств, деталей с герметическими швами из оцинкованного железа. Припой ПОС 30 не имеет достойных зарубежных аналогов и относится к категории мягких припоев, потому что температура его плавления не превышает 300 0С. Сплав является бессурьмянистым.Отлично подходит для пайки меди, латуни и железа. В промышленных масштабах применяется в энергетической сфере. Во время пайки ПОС 30 с поверхностью детали формируют высококачественную зону промежуточного сплава. Любители и профессионалы используют припой ПОС-30 для пайки электроприборов и радиоаппаратуры.
Пруток припоя ПОС 30 диаметром 8 мм будет легко гнуться руками, потому что в нем отмечается высокое содержание свинца. В отличие от свинца олово будет придавать припою повышенную степень жесткости и прочности. В состав ПОС 30 входит олово (29-31%) и свинец (69-71%). Температура плавления припоя составляет 256 оС (начало плавления отмечается на 183 градусах). Для большинства радиоэлектронных элементов подобная температура считается предкритической, что обязательно нужно учитывать перед проведением паяльных работ.
Харакетристики:
Припой ПОС-61 в классификации припоев занимает особенное место. Это обусловлено тем, что в этом сплаве отмечается содержание канифоли, поэтому его можно с успехом использовать для лужения и пайки самых разных контрольно-измерительных приборов.Припой ПОС 61 — это по-своему универсальный материал, который идеально подойдет для любой разновидности проводов. Также отмечается, что он неплохо себя показывается при пайке микросхем. Кроме того, если нельзя во время работы допустить перегрев места пайки, то припой ПОС-61 справится с задачей куда эффективнее, чем многие другие сплавы. Производитель отмечает, что основной сферой использования припоя ПОС61 является пайка жил к полупроводниковым устройствам, выводам разъемов, медных проводов. Стоит отметить, что это оптимальный выбор для соединения следующих металлов: сталь, латунь, бронза, медь. Припой ПОС 61, если сравнивать с другими оловянно-свинцовыми припоями, представленными на рынке, имеет более высокий уровень чистоты и рассчитан на пайку электромонтажа. За счет повышенного содержания меди в припое снижается интенсивность растворения проводов из меди, а также во много раз увеличивается степень износостойкости медных стержней электрических паяльников. Температура плавления припоя ПОС 61 составляет 183 0С, в то время как полностью он расплавляется при 190 градусах. Пайка с помощью этого припоя может быть выполнена при помощи традиционного паяльного инструмента.
Пайка с помощью этого припоя может быть выполнена при помощи традиционного паяльного инструмента.
Состав припоя ПОС 61: свинец (39-50%), олово (50-61%). Одновременно с этим, по ГОСТу 21930-76 главным фактором, который определяет характеристики припоя, является химический состав. Помимо свинца и олова в припое ПОС 61 содержатся следующие примеси: Sb, Cu, As, Bi, Ni, S, Zn, Al, Fe.
Применение: Электроаппаратура, детали из оцинкованного железа с герметичными швами.Температура плавления: 183-238°CХимический состав: Олово 40% Свинец 60%Пайка металлов: Бронза, Латунь, Медь, СтальХаракетристики:
Припой ПОС-40 является оловянно-свинцовым припоем, поэтому его область использования довольно-таки широка. С помощью припоя этой марки осуществляется пайка железа, латуни медных проводов, элементов из оцинкованного железа с полностью герметичными швами. Именно поэтому припой активно используется в сфере электрооборудования, при ремонте медных и латунных трубопроводов, ремонте радиаторов.Припой ПОС-40 может быть использован с любым видом паяльного оборудования, поэтому, в большинстве случаев, именно он выбирается для проведения пайки и лужения различных элементов не только в локальном ремонте, но и в заводских масштабах.
Припой ПОС 40 великолепно подходит для формирования прочного (если требуется, и полностью герметичного) шва, а также для получения электроконтакта с небольшим переходным сопротивлением. За счет того, что имеет температуру плавления намного меньшую, чем соединяемые металлы, то он плавится, оставляя при этом основной металл абсолютно твердым. Компоненты будут диффундировать в основной металл, который будет растворяться в припое, за счет чего начнет формироваться промежуточная прослойка, соединяющая все элементы в одно целое после застывания.
Производители выпускает припой ПОС 40 в виде проволоки (без канифоли) и трубок (с сосновой канифолью).
Осуществлять пайку этим припоем можно простым паяльным инструментом, не опасаясь при этом перегрева элементов, потому что припой полностью расплавляется уже при температуре в 238 градусов. Если требуется припой, который будет плавиться при более низких температурах, то рекомендуется выбирать модель ПОС 61 и другие соответствующие виды.
Припой ПМФОЦр 6-4-0,03 купить Припой ПМФОЦр 6-4-0,03 ТУ 48-17228138
Применение: Пайка кондиционеров, холодильников, теплообменников, волноводов.Температура плавления: 640-680°CХимический состав: Медь 89% Фосфор 6% Олово 4% Цирконий 0,03%Пайка металлов: Бронза, Латунь, Медь, СереброХаракетристики:
Припой ПМФОЦр 6-4-0.03 относится к категории медно-фосфорных. В припое этой марки отмечается высокое содержание фосфора и меди, а также значительное количество циркония и олова.Это среднеплавкий припой, который имеет повышенную текучесть, отличную устойчивость к коррозийным процессам и агрессивной среде. Основная сфера использования сплава — пайка меди и ее различных сплавов (мельхиора, латуни, бронзы).
Одновременно с этим, ПМФОЦр зачастую применяется как заменитель серебряных припоев в процессе ремонта ювелирных изделий. Запрещено осуществление пайки чугуна и стали припоями с содержанием фосфора, потому что соединение получается хрупким и не способно выдержать нагрузки вибрационного, ударного и изгибающего типа. Это обусловлено тем, что по границе шва фосфоритов образуется видимая пленка. Особенностью припоя ПМФОЦр можно назвать то, что он является самофлюсующимся. Именно поэтому, если им осуществляется пайка изделий из меди, то в этом случае нет никакой необходимости использовать флюс. Как правило, припой этой марки применяется в ремонте бытовых смесителей, кондиционеров, при изготовлении климатического оборудования, электромашин высокой мощности. В классификации припоев ПМФОЦр относится к категории среднеплавких самофлюсующихся припоев, что допускает осуществление пайки без использования флюса. Пайка с помощью этого припоя может выполняться горелкой любого типа (ацетиленовой, пропановой горелкой, паяльной лампой), с помощью аргонодуговой сварки. Основное условие в этом случае — спаиваемые детали должны нагреться до темно-красного свечения (вишневый оттенок). Затем необходимо нагревать припой до того момента, пока он не начнет растекаться должным образом.
В классификации припоев ПМФОЦр относится к категории среднеплавких самофлюсующихся припоев, что допускает осуществление пайки без использования флюса. Пайка с помощью этого припоя может выполняться горелкой любого типа (ацетиленовой, пропановой горелкой, паяльной лампой), с помощью аргонодуговой сварки. Основное условие в этом случае — спаиваемые детали должны нагреться до темно-красного свечения (вишневый оттенок). Затем необходимо нагревать припой до того момента, пока он не начнет растекаться должным образом.
Харакетристики:
Припой П-81 рассчитан на пайку при изготовлении климатического оборудования, теплообменников, калориферов, термодатчиков, производстве часов и т.п. Пайка с помощью этого припоя может осуществляться только с применением флюса. Допускается изготовление закладных элементов различной формы и колец для осуществления автоматической пайки (подобные работы должны проводиться только в заводских условиях на походящем для этого оборудовании).П-81 в своем составе содержит несколько основных элементов: цинк (32-36%), медь (52-54%), никель и фосфор (по 6-7%). При помощи припоя П-81 допускается соединение следующих материалов: никель и никелевые сплавы (в том числе и латунь), медь, чугун, серебро, сталь (в том числе нержавейка), твердые сплавы и их всевозможные комбинации. С помощью припоя П-81 разрешается пайка с использованием флюса. П-81 может похвастать особенными свойствами и некоторыми конкурентными преимуществами. Среди них необходимо выделить высокий уровень надежности и долговечности фреоновых элементов, повышенный предел прочности на срез, высокое качество в процессе ремонта твердосплавных инструментов, высокая степень герметичности паяных конструкций в условиях повышенного давления. Нельзя не отметить и то, что П-81 производитель считает столь же эффективным, как и некоторые высокосеребряные припои. При работе с припоем этой марки рекомендуется использовать флюсы, которые соответствуют следующим припоям: ФК-250 (235), ПВ-209.
Нельзя не отметить и то, что П-81 производитель считает столь же эффективным, как и некоторые высокосеребряные припои. При работе с припоем этой марки рекомендуется использовать флюсы, которые соответствуют следующим припоям: ФК-250 (235), ПВ-209.
Температура плавления припоя составляет 630-660 оС, в том время как рекомендованная температура пайки варьируется от 680 до 700 оС. Предел прочности сплава находится в пределах 170 Мпа.
Припой П-81 показывает себя особенно эффективным, если его использовать взамен высокосеребряных припоев марок ПСр40, ПСр29.5, ПСр25, ПСр45.
Применение: Пайка холодильников, кондиционеров, теплообменников, волноводов, бытовых смесителей.Температура плавления: 640-680°CХимический состав: Медь 90% Фосфор 6% Олово 4%
Харакетристики:
Припой П-14 представляет собой соединение, в котором присутствует значительное количество меди (основа), олова (от 3,5 до 4,5%) и фосфора (от 5,3 до 6,3%). Все это делает его уместным для использования в процессе пайки калориферов, теплообменников, холодильников, кондиционеров, электрических машин высокой мощности, волноводов и бытовых смесителей. Идеально он способен соединять такие материалы, как серебро, медь и медные сплавы. Отметим, что пайка меди при помощи припоя марки П-14, осуществляется даже без добавления флюса.Изготавливают припой этого типа в виде проволоки с различным диаметром, прутка с различным диаметром, ленты с различной толщиной и шириной. Если припой выполнен в виде проволоки, то в ней может присутствовать продольный паз с флюсом марки ФК-320 и марки ФК-235. Поэтому осуществляя пайку той или иной детали можно легко подбирать оптимальный для каждого случая вариант.
В процессе пайки следует придерживаться определенной температуры. Если пайка проводится в газовом пламени, то она должна быть не выше 740 и не ниже 720 градусов, а если пайка в печи — то не менее 800 и не более 820 градусов.
 Ударная вязкость разрушения составляет порядка 1,5-3 кДж.м/см2, а прочность паяных соединений равна 290-320 МПа.Применение: Лужение алюминиевых оболочек и пайка алюминиевых жил.Температура плавления: 300-320°CХимический состав: Олово 42-45% Цинк 54% Медь 1,2-1,5%Пайка металлов: Алюминий
Ударная вязкость разрушения составляет порядка 1,5-3 кДж.м/см2, а прочность паяных соединений равна 290-320 МПа.Применение: Лужение алюминиевых оболочек и пайка алюминиевых жил.Температура плавления: 300-320°CХимический состав: Олово 42-45% Цинк 54% Медь 1,2-1,5%Пайка металлов: АлюминийХаракетристики:
Припой марки А представляет собой одну из востребованных разновидностей оловянно-медно-цинковых припоев. Именно эти три главных компонента составляют его основу и предопределяют и главные свойства, и сферы, в которых его использование будет отличаться максимальной эффективностью.Идеально подходит припой марки А для использования в процессе проведения пайки алюминиевых жил и выполнения лужения алюминиевых оболочек. Этому благоволит и то, что он вполне стоек к негативному воздействию коррозии и обладает превосходными технологическими свойствами. Важна и температура плавления этого соединения. Она варьируется в диапазоне от 400 до 400 градусов Цельсия. В то время, как плотность припоя этого типа составляет 7,2 г/см3. Все это следует учитывать при проведении пайки и лужения изделий.
В составе припоя преобладает содержание цинка, его количество варьируется от 56% до 59%, олова в соединении не более 42,1% и не менее 38,6%. Меди в разы меньше — не более 2%, в некоторых случаях ее присутствие может не превышать показателя в 1,5%. И это предопределяет большую часть свойств припоя, уместность его использования в определенных сферах, а также ряд других важных показателей.
Применение: Пайка генераторов, шинопроводов, электродвигателей большой мощности, трансформаторовТемпература плавления: 714-850°CХимический состав: Медь 93% Фосфор 7%Пайка металлов: Латунь, Медь, Серебро
Характеристики:
Припой МФ-7 входит в категорию медно-фосфорных припоев и предполагает наличие в своем составе порядка 7% фосфора, о чем и свидетельствует маркировка изделия. Он превосходно показывает себя при пайке латуней и бронз, нейзильбера и медно-никелевых сплавов. Хотя, основной сферой использования в данном случае принято считать пайку меди и разнообразных медных сплавов без применения флюсов. Необходимость во флюсах отсутствует, поскольку припой этой марки относится к самофлюсующим припоям.
Он превосходно показывает себя при пайке латуней и бронз, нейзильбера и медно-никелевых сплавов. Хотя, основной сферой использования в данном случае принято считать пайку меди и разнообразных медных сплавов без применения флюсов. Необходимость во флюсах отсутствует, поскольку припой этой марки относится к самофлюсующим припоям. Применять припой, изготовленный под маркой МФ-7, для пайки сталей и чугуна не рекомендуется. В этих сферах он зарекомендовал себя не самым лучшим образом. В этих случаях возникает образование хрупких фосфидов железа непосредственно в паяном шве и как следствие — утрачивается пластичность.
Идеально подходит данный вид припоя для пайки кондиционеров и холодильников. В обоих случаях необходимо применять газопламенный нагрев и придерживаться температуры пайки в диапазоне от 732 до 816 градусов Цельсия. Припою характерна высокая жидкотекучесть и низкая температура плавления, что приравнивает его по свойствам к серебряным и медно-цинковым припоям, востребованным при пайке медных сплавов и самой меди.
Температура плавления: 700-900°CПайка металлов: Медь, Серебро, Сталь
Харакетристики:
Флюс Бура в промышленной сфере используется достаточно часто. Также сферой его применения считается пайка ювелирных изделий, где необходимо точно рассчитать состав используемых материалов и тип инструментов для пайки. Универсальным решением в этом случае является именно флюс, созданный на основе борной кислоты или буры.Бура — важнейшая добавка при плавке, которая позволяет обеспечить формирование тигля глазури на стенках, растворение окислов металлов и предохранить расплав от проникновения кислорода. Бура — это соль тетраборной кислоты, которая существует в виде декагидрата в свободной форме. Изготовление флюса такого типа ведется с помощью борной кислоты и буры, которые в соотношении 1:1 по массе растворяются в воде. Чтобы приготовить 1 л флюса бура, необходимо смешать 100 г борной кислоты и 100 г буры, добавив их в 1 л воды, после чего довести до кипения. После естественного остывания массы ее следует отфильтровать. Соотношение борной кислоты и буры в составе флюса необходимо варьировать в зависимости от того, с каким именно металлом предполагается работать. Если это золото, то основу флюса должна составлять борная кислота, а не бура. Обратная ситуация с серебром.
После естественного остывания массы ее следует отфильтровать. Соотношение борной кислоты и буры в составе флюса необходимо варьировать в зависимости от того, с каким именно металлом предполагается работать. Если это золото, то основу флюса должна составлять борная кислота, а не бура. Обратная ситуация с серебром.
Флюс бура считается нейтральным флюсом. Он также может быть использован для высокотемпературной пайки меди, стали, чугуна, твердых сплавов с серебряными и медными паяльными сплавами.
Флюс ЛТИ-120 купить Флюс ЛТИ-120 500 мл.
Применение: Лужение сплавов меди, стали, никеля, свинца, цинка, серебра, олова, кадмия, палладия.
Температура плавления: 200-300°C
Пайка металлов: Медь, Никель, Олово, Свинец, Серебро, Сталь, Цинк
Харакетристики: Флюс ЛТИ-120 на отечественном рынке представлен достаточно давно. Он относится к категории активированных флюсов, в которой ЛТИ-120 считается уже давно одним из лучших. В состав этого флюса входят уникальные добавки, которые позволяют в разы увеличить его эффективность. Кроме того, предусмотрено наличие полностью пасивирующих добавок. Взаимодействие флюса в полной мере будет зависеть от температуры, при которой проводятся работы. При обычной температуре флюс не проявляет никакой активности и не способен проводить ток даже на повышенных частотах. По завершению паяльных работ остатки флюса можно не убирать, потому что они будут представлены в виде твердого вещества, не подверженного каким-либо внешним факторам. Зачастую остатки флюса выступают в качестве защитного покрытия паяльных соединений. По уровню активности флюс марки ЛТИ-210 схож с современными паяльными кислотами. В состав флюса входят следующие вещества: этиловый спирт, канифоль, диэтиламин солянокислый, триэтаноламин. Именно поэтому допускается его использование при пайке железа, нержавейки, бронзы, меди, стали, никеля, серебра и ряда других веществ.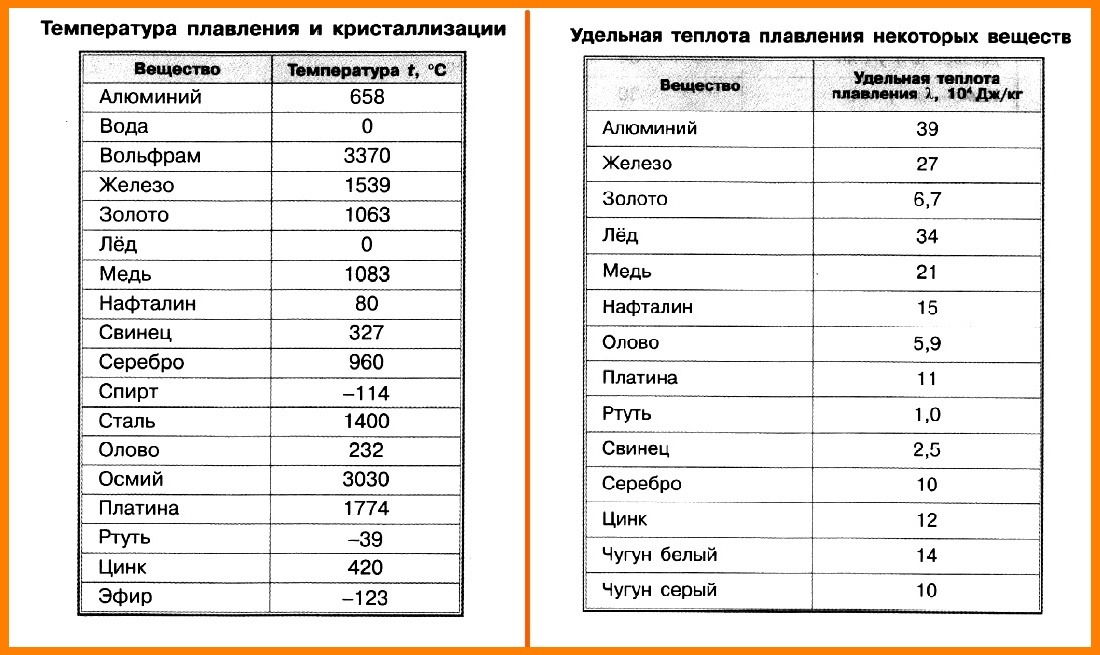 После того, как работы будут завершены, вентилировать помещение необязательно. Если необходимо смыть остатки, то это можно сделать при помощи ацетона или спирта.
После того, как работы будут завершены, вентилировать помещение необязательно. Если необходимо смыть остатки, то это можно сделать при помощи ацетона или спирта.
Флюс ПВ-209 купить Флюс ПВ-209
Применение: Пайка меди, твердых сплавов, нержавеющих и конструкционных сталей.
Температура плавления: 600-900°C
Пайка металлов: Медь, Нержавейка, Серебро, Сталь
Харакетристики: Флюс ПВ-209 рассчитан на высокотемпературную пайку серебряными и медными припоями никеля, меди, серебра и сплавов, а также особо твердых и жаропрочных сплавов. Флюс позволяет полностью удалить окисные пленки, а также предотвратить их формирование при нагреве. Флюс также способствует уменьшению поверхностного натяжения жидкого припоя, защите поверхностей, подготовленных к пайке, от негативных внешних воздействий.
Производство флюса ПВ-209 ведется по оригинальной технологии. Нанесение флюса на поверхности, подготовленные к пайке, удобнее всего производить в виде пасты. Ее можно получить с помощью замешивания флюса в воде (пропорция 1:1 в соответствии с массой). Текучесть пасты регулируется добавлением воды.
Если флюс используется в виде порошка и осуществляется пайка нелегированной стали, то разрешен нагрев до побежалости с дальнейшим нанесением флюса. В процессе пайки нержавеющей стали флюс рекомендуется наносить пастой и контролировать целостность поверхности. При пайке твердосплавных поверхностей их требуется нагревать равномерно и полностью. Остатки флюса после пайки могут быть удалены с помощью кипячения в воде или 10%-ным раствором лимонной кислоты.
Паяльная кислота Флюс и реактивы для пайки
Характеристики:
Паяльная кислота — это хлорид цинка, что является химическим соединением цинка и хлора (формула — ZnCl2).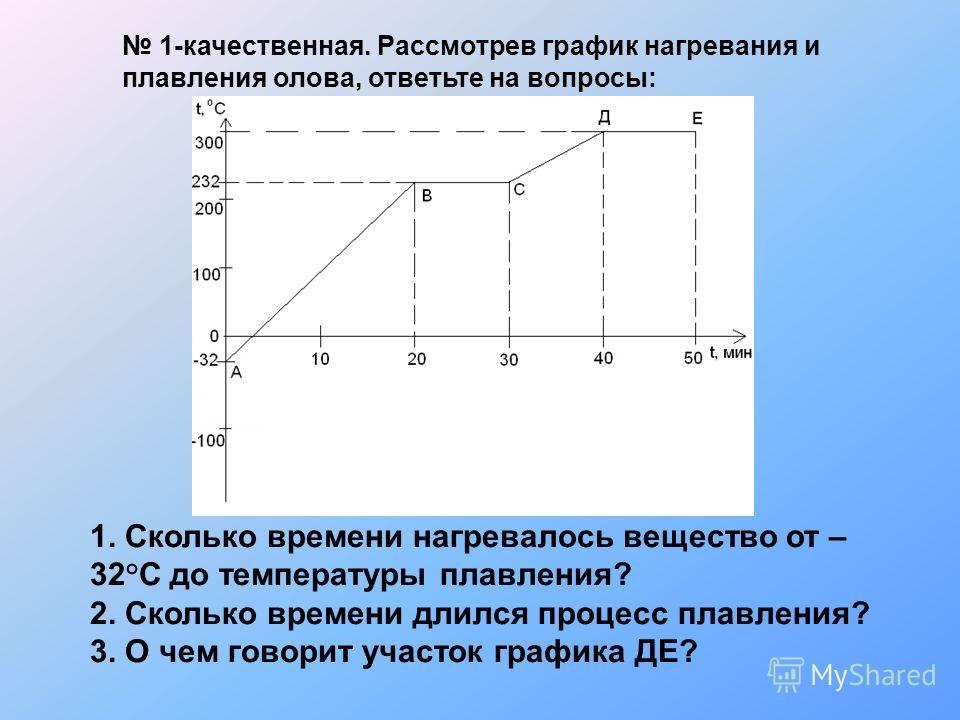 Паяльная кислота активно используется для пайки меди, углеродистых сталей, никеля и сплавов с помощью легкоплавких припоев в диапазоне температур от 150 до 320 оС. Также в состав паяльной кислоты (помимо хлорида цинка) входят: соляная кислота, хлорид аммония, специальная смачивающая присадка. Кроме того, паяльную кислоту часто называют активным флюсом в жидком агрегатном состоянии.
Паяльная кислота активно используется для пайки меди, углеродистых сталей, никеля и сплавов с помощью легкоплавких припоев в диапазоне температур от 150 до 320 оС. Также в состав паяльной кислоты (помимо хлорида цинка) входят: соляная кислота, хлорид аммония, специальная смачивающая присадка. Кроме того, паяльную кислоту часто называют активным флюсом в жидком агрегатном состоянии.
Паяльная кислота может быть получена с помощью растворения цинка (либо его окиси) в растворе соляной кислоты с дальнейшим выпариванием раствором. Кроме того, вещество получается по средствам нагревания жидкого цинка в токе хлора.
Физические и химические свойства паяльной кислоты:
• Температура кипения — 730 оС;
• Температура плавления — 315-320 оС;
• Молекулярная масса — 136,2954;
• Растворимость в воде — 79.8% при 0 оС;
• Концентрированные составы обладают кислой средой, потому при диссоциации в воде наблюдается образование соляной кислоты.
Паяльная кислота также используется для лужения проводов и пайка радиодеталей микросхем. Срок годности паяльной кислоты не превышает 12 месяцев с условием соблюдения стандартов хранения. Хранение вещества нужно производить в плотной закрытой таре, не допуская воздействия прямых солнечных лучей и тепла. Если в помещении проводились работы с использованием паяльной кислоты, его нужно хорошенько проветрить по их завершению.
Флюс паяльный ФКСп купить Флюс ФКСп 500 мл.
СПИРТОКАНИФОЛЬНЫЙ ФЛЮС (он же КЭ, СКФ, и ФКЭт -на этилацетате, жидкая канифоль).
Применение: Для пайка элементов радиомонтажа и печатных плат легкоплавкими припоями при температурах 250-280ºC.
Состав: канифоль сосновая не менее 30%, АИПС-70%.
Пайка металлов: медь; серебряное, оловянное, оловянно-свинцовое, оловянно-висмутовое, оловянно-никелевое, кадмиевое, золотое покрытия.
Характеристики : ручная и механизированная пайка и лужение электромонтажных элементов печатных плат и элементов радио электроники в изделиях радио и бытовой электронной аппаратуры. Консервация изделий радио и бытовой электронной аппаратуры для сохранения паяемости в условиях складского хранения и хранения в условиях сборочного цеха в течение одного года. Остатки флюса при ручной пайке изделий бытовой радио аппаратуры (пайке подстроечных элементов, подпайке, исправлении дефектов) допускается не удалять. Остатки флюса при групповой пайке изделий бытовой радио аппаратуры («волной» припоя, погружением, протягиванием) следует удалять.
Консервация изделий радио и бытовой электронной аппаратуры для сохранения паяемости в условиях складского хранения и хранения в условиях сборочного цеха в течение одного года. Остатки флюса при ручной пайке изделий бытовой радио аппаратуры (пайке подстроечных элементов, подпайке, исправлении дефектов) допускается не удалять. Остатки флюса при групповой пайке изделий бытовой радио аппаратуры («волной» припоя, погружением, протягиванием) следует удалять.
При каких температурах плавится свинец и олово: физические свойства
Свинец – серебристо-серое вещество с синим отливом. В периодической системе элементов Менделеева металл занимает 82 место. Обозначают свинец сокращённым знаком Pb (лат. Plumbum).
Свинец
Исторические сведения
Химический элемент известен людям с древних времён. Одним из первых методов добычи металлов, освоенных человеком, была выплавка свинца. Первыми археологическими находками, подтверждающими это, были найденные свинцовые бусы времён Чатал-Хююк (современная территория Турции). Изделия датируются 6400 годом до нашей эры.
Самая древняя свинцовая фигурка девушки в длинной одежде была выкопана в Египте. Её относят к временам первой династии фараонов (3000 лет до н.э.).
Трубы из свинца составляли древнеримский водопровод. В Древнеримской империи ежегодно выплавляли до 80 тысяч тонн этого металла. На Руси с древних времён свинец использовали как кровельное покрытие соборов и церквей.
Невысокая температура плавления свинца с незапамятных времён сделала доступным получение металла и изготовление из него изделий любой формы.
Обратите внимание! Индустриальная революция с 1840 года в течение 20 лет подняла объём ежегодной выплавки свинца в мире со 100 до 250 тысяч тонн в год.
Происхождение названия
Латинское название металла Plumbum произошло от английского выражения plumber (водопроводчик), что показывает связь со свинцовым водопроводом Древнего Рима. Среди славянских народов бытуют такие названия, как оливо, олёво и волава. В Прибалтийских странах наименование металла более похоже на русское название – свинс и свинас.
Среди славянских народов бытуют такие названия, как оливо, олёво и волава. В Прибалтийских странах наименование металла более похоже на русское название – свинс и свинас.
Нахождение в природе
В чистом виде плюмбум обычно не обнаруживается. Его находят в более чем 100 разных минералах в виде интерметаллических агломератов. Свинец присутствует в урановых и ториевых жилах. Большие скопления свинцово-цинковых руд обнаружены и разрабатываются в Забайкалье, Приморском районе. В разных залежах свинец добывают на Урале, в Норильске.
Самое крупное месторождение с большим содержанием свинца находится в урановых рудах Кохистанской Ладахской дуги (северный Пакистан).
Ископаемый свинец
Получение
Сырьём для извлечения свинца служат породы, включающие геленит. Процесс выплавки тяжёлого металла состоит из нескольких фаз. Из первоначального сырья способом флотации выделяют концентрат с содержанием от 40 до 70 процентов плюмбума. Далее производители идут разными путями.
Одним из способов превращения продукта в веркблей (черновой свинец) является плавка методом регенерации. Другой способ заключается в том, что восстановление металла из оксида происходит плавкой сырья в ватержакетном калорифере.
Полученный веркблей с содержанием 90% свинца очищают от меди. Затем щелочным рафинированием убирают мышьяк и сурьму. Потом выделяют серебро и цинк. Воздействием магния и кальция исключают висмут. В итоге получают свинец чистотой 99,8%.
Производство мирового объёма свинца по итогам исследования международных организаций за 2005 год
| Страна производитель | Объём, килотонн |
|---|---|
| Страны Европы | 2220 |
| КНР | 1430 |
| Российская федерация | 1120 |
| Ю. Корея | 650 |
| Казахстан | 570 |
| Украина | 410 |
Технологические свойства и характеристики
Характеристики металла можно представить перечнем:
- Плотность свинца и его масса;
- Температура плавки свинца;
- Механические свойства;
- Сопротивление коррозии.
Плотность свинца и его масса
Плотность металла составляет 11342 кг/м3. Это значит, что метрический куб свинца весит 11,342 тн. Большой удельный вес позволяет его использовать в виде полезных грузов в различных устройствах.
Температура плавки свинца
Расплавленный металл в чистом виде имеет температуру около 400 градусов. В этом состоянии свинец обладает свойствами текучести жидкости. Литейные качества позволяют заливать свинец в жидком состоянии в формы сложной конфигурации.
Заливка формы свинцом
Металл закипает при нагреве до 1750 градусов. Во время кипения возникают летучие испарения в виде свинцовой пыли, паров оксидов, которые могут нанести тяжёлое отравление человеческому организму.
Механические свойства
Химический элемент обладает мягкостью и пластичностью, что позволяет холодной прокаткой достичь состояния тонкой фольги. Холодная деформация не влияет на изменение механических свойств.
Сопротивление коррозии
Химическая инертность элемента приближена к показателю благородных металлов. В воздушной среде плюмбум практически не подвергается коррозии. Быстро образующаяся оксидная плёнка на поверхности свинца ставит непреодолимый барьер на пути коррозионных процессов.
Агрессивной средой для свинца являются сероводород, ангидрит угля и серная кислота. Под их воздействием металл активно разрушается.
Области применения свинцовых сплавов
Свинцовые соединения разделяют на высоколегированные и низколегированные сплавы. Первые формируются за счёт добавления большого количества химических элементов, обеспечивающих высокую прочность, стойкость к истиранию и низкую усадку при более низкой температуре плавления.
Низколегированные соединения свинца получаются в результате небольших включений из таких веществ, как олово, сурьма, медь и кадмий. Этим добиваются повышенной стойкости сплава к коррозионным процессам в условиях загрязнённой атмосферы, неорганической кислотной среды.
Сплавы применяют в кислотных и щелочных аккумуляторах, в качестве оболочек как мощных, так и кабелей низкого напряжения. Соединения сурьмы или меди со свинцом используют для производства трубопроводов, листовой облицовки различных устройств и защитных матов от радиационного поражения.
Домашние и промышленные способы
Без оловянно-свинцовых припоев (ПОС) невозможно существование такой отрасли, как радиотехника. Многие промышленные изделия имеют в своём составе покрытия из ПОС.
Оловянно-свинцовые припои
Промышленность поставляет на рынок припойный продукт:
- литые чушки;
- проволока;
- фольгированная лента;
- припойные трубочки с флюсом;
- порошок или паста.
Сплавы с содержанием 90% олова и 10% свинца применяют для пайки изделий, которые потом подвергаются гальваническому покрытию из золота или серебра. Температура плавления чистого олова – 2310 С. Поэтому припой расплавится при нагреве 2200 С.
Трубчатый припой с флюсом
Оловянно-свинцовый ПОС с преобладанием в своём составе олова (61%) имеет более низкую температуру плавления – 191%. ПОС 61 используют для покрытия контактных групп в различных приборах, также им обрабатывают тонкую проволоку для обмоток якорей электродвигателей и катушек трансформаторов.
Важно! Учитывая, при какой температуре плавится олово, регулируют % содержание свинца в сплаве. Этим добиваются комфортного температурного режима, при котором оловянно-свинцовый припой быстро переходит в жидкое состояние.
ПОС 30 плавится при 256 градусах. Соединения обладают меньшей прочностью, чем средства с более высоким содержанием олова.
10 процентный припой далёк от температурного порога, при котором происходит плавление олова. Поэтому ПОС 10 применяют как прочный материал для лужения больших металлических поверхностей.
Приготовление расплава и заливка
В промышленных условиях расплав готовят в специальных тиглях, которые помещают в электропечи (оборудование, оснащённое электронной измерительной аппаратурой, поддерживающее нужный режим плавки).
В радиотехническом производстве используют специальные нагревательные ванны, в которых готовят припой для печатных плат радиосхем.
В мастерских и дома припой плавят жалом паяльника. Для приготовления большого объёма расплавленного металла его помещают в медный сосуд на электроплите. Сплав в виде лома загружают в плавильную ванну постепенно, по мере расплавления очередного слоя металла.
Рыболовные лаки
Заядлые рыбаки дома отливают рыболовные грузила и блесны, вливая в глиняные формы расплавленное олово. Блесны затем покрывают водостойкими лаками.
Интересно. Рыболовный лак используют для защиты от появления оксидов на различных статуэтках и других изделиях.
Рыболовный лак
Методы избавления от оксида
Во время нахождения на воздухе свинцовые изделия покрываются оксидной плёнкой. Это результат ионного взаимодействия атомов кислорода и свинца. Оксид становится не только защитой от агрессивной среды, но и барьером на пути электрического тока.
Важно! Механическая чистка не принесёт желаемого результата. Плёнка восстановится довольно быстро. Избавиться от оксидов могут помочь подсолнечное масло, графитовая смазка или лак.
В домашних условиях изделие помещают в сосуд с подсолнечным маслом минут на пять. После чего его извлекают из сосуда и дают просохнуть.
В промышленных условиях пользуются графитовой смазкой. Обработанная средством свинцовая поверхность долгое время сохраняет блестящий вид.
Техника безопасности
При работе с расплавленным металлом надо соблюдать особую осторожность. Помимо того, что жидкий свинец может нанести ожоги на кожу, он прожжёт также одежду и напольное покрытие, а также вызовет пожар.
Если вода попадёт в кипящий сплав, брызги металла разлетятся во все стороны. Поэтому работник должен быть экипирован защитной одеждой, маской, перчатками, специальными очками и головным убором. Обязательно рядом должны находиться аптечка и огнетушитель.
Видео
1. Температура плавления олова 232 °С. При какой температуре оно отвердевает? Как изменяется его внутренняя энергия при переходе в твердое состояние?
Вариант 1 Изменение агрегатных состояний вещества
1. Температура плавления олова 232 °С. При какой температуре оно отвердевает? Как изменяется его внутренняя энергия при переходе в твердое состояние?
а) При любой температуре; увеличивается.
б) При 232 °С; уменьшается.
в) При температуре плавления; увеличивается.
2. Температура в электропечи достигает 1500 °С. Какое из веществ — медь, стать, железо — можно в ней расплавить?
а) Медь. б) Сталь. в) Железо.
3. Кусок льда нагрели и расплавили. График этого процесса представлен на рисунке. Определите по нему, сколько минут плавился лед, какому процессу соответствует участок АВ графика.
а) 6 минут; нагреванию льда 0 °С.
б) 4 мин; нагреванию льда до температуры плавления.
в) 4 мин; плавлению льда.
4. На рисунке изображены графики изменения температуры веществ со временем. Какой из них соответствует процессу отвердевания вещества?
а) № 1.
б) № 2.
в) № 3.
5. Сколько энергии необходимо для превращения в жидкость 3 кг парафина при температуре его плавления?
а) 7,5 · 105 Дж. б) 4,5 · 105 Дж. в) 0,5 · 105 Дж.
6. Кусок льда массой 500 г находится при температуре —20 °С. Какое количество теплоты нужно ему сообщить, чтобы он полностью расплавился?
а) 1,95 · 105 Дж. б) 0,25 · 105 Дж. в) 1,75 · 105 Дж.
7. При какой температуре жидкость не испаряется?
а) При отрицательной температуре.
б) При той, при которой вещество отвердевает.
в) Жидкость испаряется при любой температуре.
8. Каково условие, при котором наступает динамическое равновесие между паром и жидкостью?
а) Число покидающих жидкость молекул должно стать равным числу молекул, возвращающихся в нее из пара.
б) Неизменность количества жидкости и пара.
в) Прекращение испарения жидкости.
Вариант 2 Изменение агрегатных состояний вещества
Известно, что олово находится при температуре 232 °С. Плавится оно или отвердевает?
а) Частично плавится, частично отвердевает.
б) Если получает энергию, то плавится, если отдает — отвердевает.
в) Плавится, но иногда отвердевает в зависимости от его количества.
Максимальная температура, на которую рассчитана плавильная печь, 3000 °С. Какой металл — железо, вольфрам, алюминий — нельзя в ней расплавить?
а) Железо.
б) Вольфрам.
в) Алюминий.
Какому процессу изменения агрегатного состояния воды соответствует представленный на рисунке график? Какой длительности интервал времени занял этот процесс?
а) Отвердеванию; 5 мин.
б) Охлаждению без изменения агрегатного состояния вещества; 5 мин.
в) Плавлению; 10 мин.
Какой из графиков построен для плавящегося вещества? Какому процессу соответствует график № 2?
а) № 1; нагреванию вещества.
б) № 2; охлаждению вещества.
в) № 3; нагреванию вещества.
Вычислите количество теплоты, необходимое для плавления 5 кг свинца при температуре 327 °С.
а) 0,5 · 104 Дж. в) 2,5 · 105 Дж.
б) 1,25 · 105 Дж. г) 12,5 · 105 Дж.
Сколько энергии нужно для плавления 10 кг меди? Ее температура 585 °С,
а) 4,1 · 106 Дж.
б) 4,6 · 106 Дж.
в) 2,3 · 106 Дж.
г) 41 · 106 Дж.
Как испарение жидкости зависит от площади ее поверхности?
а) Не зависит.
б) Чем больше площадь поверхности, тем испарение интенсивнее.
в) При увеличении площади поверхности испарение замедляется.
Что характерно для состояния динамического равновесия пара и жидкости?
а) Замедление и прекращение испарения жидкости.
б) Увеличения количества пара и его интенсивная конденсация.
в) Испарение жидкости и конденсация пара в равных количествах.
Абсолютная влажность воздуха 25,42 г/м3. Какова в нем плотность водяного пара?
а) 2,54 г/м3 б) 25,42 г/м3 в) 50,84 г/м3
Что показывает точка росы?
а) Температуру, при которой водяной пар, находящийся в воздухе, становится насыщенным.
б) Момент, когда пар воды, содержащийся в воздухе, достигает насыщения
в) Переход при понижении температуры ненасыщенного пара в насыщенный.
При каком процессе — испарении жидкости или конденсации пара — энергия выделяется?
а) При испарении жидкости. в) При том и другом процессе.
б) При конденсации пара.
Какой вид парообразования более интенсивен? Почему?
а) Испарение, потому что у жидкости может быть большая поверхность.
б) Кипение, так как пар образуется во всем объеме жидкости.
в) Их интенсивность нельзя сравнить, поскольку нет нужных данных.
Какие жидкости, из указанных в таблице 5 учебника, закипают при более низкой температуре, чем вода?
а) Эфир и спирт. б) Молоко, эфир, спирт,
в) Водород, кислород, эфир, спирт.
По какой формуле рассчитывают количество теплоты, выделяющееся при конденсации пара?
a) Q = λm. в) Q = cm(t2 – t1).
б ) Q = Lm. г) Q = qm.
Сколько энергии выделяет при конденсации 100 г ртути?
а) 3 · 104 Дж.
б) 3 · 105 Дж.
в) 3 · 106 Дж.
г) 3 · 107 Дж.
Какое количество теплоты потребуется для превращения при кипении в пар 0,5 кг воды, находящейся при температуре 40 °С?
а) 12,34 · 105 Дж.
б) 12,76 · 104 Дж.
в) 12,76 · 105 Дж.
Имеются: чашечка воды, кусочек льда, пробирка с водяным паром. Массы воды во всех состояниях одинаковы. Расположите эти тела в порядке убывания внутренней энергии воды.
а) Пробирка — чашечка — кусочек льда.
б) Чашечка — пробирка — кусочек льда.
в) Кусочек льда — чашечка — пробирка.
Наличие каких основных частей обязательно для любого теплового двигателя?
а) Цилиндра с поршнем, рабочего вала, маховика.
б) Источника газа или пара, вращаемого вала, отвода отработавшего газа (пара).
в) Нагревателя, рабочего тела, холодильника.
9. Плотность
водяного пара в атмосфере при температуре
10 °С равна 8,3 г/м3.
Какова абсолютная влажность воздуха?
а) 83 г/м3 6) 8.3 г/м3 в) Ответить нельзя без дополнительных данных.
10. В каком случае возможно при росте абсолютной влажности воздуха уменьшение его относительной влажности?
а) При очень медленном увеличении абсолютной влажности.
б) В случае понижения температуры воздуха.
в) При повышении температуры воздуха.
11. В каком из названных явлений происходит выделение энергии?
а) На балконе сохнет белье.
б) В комнате запотевают окна.
в) На полу, протертом мокрой тряпкой, уменьшаются пятна влаги.
12. Какой вид парообразования — испарение или кипение — происходит при определенной для каждого вещества температуре?
а) Испарение.
б) Кипение.
в) Оба вида парообразования происходят при любой температуре.
13. В обычных условиях ртуть — жидкость, медь — твердое тело. Температура кипения какого из этих веществ выше? Почему?
а) Ртути, так как это металл.
б) Меди, потому что ее надо сначала превратить в жидкость.
в) Их температуры примерно одинаковы, поскольку оба вещества — металлы.
14. По какой формуле можно вычислить количество теплоты, расходуемой на кипение жидкости?
a) Q = Lm. б ) Q = λm. в) Q = qm.
15. Какое количество теплоты надо затратить на выкипание 15 кг эфира при температуре 35 °С?
а) 1,4 · 106 Дж. б) 21 · 107 Дж. в) 6 · 106 Дж.
16. Если эфир находится при комнатной температуре (20 °С), то сколько потребуется энергии, чтобы превратить в пар при кипении 200 г этого вещества?
а) 8705 Дж. б) 96450 Дж. в) 87050 Дж.
17. В каком случае на превращение воды одной и той же массы в пар придется затратить больше энергии: когда взят лед при 0 °С или вода при 0 °С, вода при 100 °С?
а) Лед. б) Вода при 0 °С. в) Вода при 100 °С.
18. Какая физическая величина характеризует экономичность теплового двигателя?
а) Произведенная двигателем полезная работа.
б) Масса сжигаемого топлива.
в) Коэффициент полезного действия.
Вариант 3 Изменение агрегатных состояний вещества
Температура плавления олова 232 °С. В каком состоянии оно находится при 230 °С? При 235 °С?
а) Твердом; жидком. б) В обоих случаях в твердом. в) В обоих случаях в жидком.
Нужно расплавить кусочки олова, свинца и цинка. Если в распоряжении есть для этого только нагреватель, максимальная температура которого 350 °С, то какой металл расплавить не удастся?
а) Олово. б) Свинец. в) Цинк.
Одинакового размера шарообразные капли эфира, одеколона и ртути находятся на стеклянной пластине в равных условиях. Какая из капель испарится быстрее других?
а) Эфира. б) Одеколона. в) Ртути.
На рисунке изображен график изменения температуры олова со временем. Какому процессу соответствует участок АВ графика? Участок ВС?
а) АВ — плавлению; ВС—отвердеванию.
б) АВ — отвердеванию; ВС — охлаждению.
в) АВ — плавлению; ВС — охлаждению.
Какой из графиков, соответствующих отвердеванию разных веществ, построен для воды?
а) № 1.
б) № 2.
в) № 3.
Определите количество теплоты, выделенное ртутью массой 4 кг при отвердевании.
а) 0,03 · 105 Дж. 6) 0,24 · 105 Дж. в) 0,48 · 105 Дж.
Сколько энергии нужно затратить, чтобы перевести в жидкое состояние 25 кг железа, температура которого 539 °С?
а) 182,5 · 105 Дж. б) 67,5 · 105 Дж. в) 11,5 · 105 Дж.
Плотность водяного пара в атмосфере 19,7 г/м3. Чему равна в этом случае абсолютная влажность воздуха?
а) 39,4 г/м3. б) 19,7 г/м3 в) 9,85 г/м3.
Что показывает относительная влажность воздуха?
а) На сколько в процентом отношении абсолютная влажность воздуха далека от насыщенного водяного пара в атмосфере.
б) Какой процент составляет плотность водяного пара в атмосфере от возможной плотности насыщенного пара в ней.
в) Выраженное в процентах отношение абсолютной влажности воздуха к плотности насыщенного пара при температуре воздуха.
Вариант 4 Изменение агрегатных состояний вещества
В каком состоянии находится олово при температуре 232 °С?
а) В жидком. б) В твердом.
в) Для ответа нужно знать, получает или отдает энергию олово при этой температуре.
Какой из металлов — олово, свинец, цинк — не удастся расплавить на электроплитке, нагревающей тела до 420 °С?
а) Олово. б) Свинец. в) Цинк.
Определите по графику, изображенному на рисунке, в каком состоянии находился свинец в первые 2 мин наблюдения за его температурой. Сколько времени длился его переход в другое (какое?) состояние?
а) В жидком; 8 мин шло отвердевание.
б) В твердом; 10 мин он плавился.
в) В жидком; через 15 мин он отвердел.
На каком из графиков плавления веществ не отражен процесс нагревания полученной жидкости?
а) № 1.
б) № 2.
в) № 3.
Какое количество теплоты потребуется для того, чтобы расплавить 6 кг чугуна, взятого при температуре 200 °С? (Удельную теплоту плавления чугуна принять равной )
а) 3,84 · 105 Дж. 6) 38,4 · 105 Дж. в) 12,48 · 105 Дж.
Какие молекулы — находящиеся внутри жидкости или на ее поверхности — участвуют в процессе испарения?
а) Расположенные на поверхности жидкости.
б) Находящиеся внутри нее.
в) И те, и другие молекулы.
Чем отличается ненасыщенный пар жидкости от насыщенного?
а) Разными условиями образования.
б) Частотой возникновения.
в) Отсутствием динамического равновесия между паром и жидкостью.
г
Если абсолютная влажность воздуха равна 95,6 г/м3, то какова плотность водяного пара, находящегося в атмосфере?
а) 95,6 4 г/м3. 6) 91,2 г/м3 в) 47,8 г/м3
Увеличится или уменьшится относительная влажность воздуха, если при той же абсолютной влажности температура понизится?
а) Уменьшится. 6) Увеличится. в) Не изменится.
Какое из названных явлений сопровождается поглощением энергии?
а) Конденсация пара на крышке кастрюли с горячей водой.
б) Образование вечером тумана на лугу возле речки.
в) Высыхание вымытой тарелки.
Для какого процесса — испарения или кипения жидкости — необходим внешний источник энергии?
а) Для испарения.
б) Для кипения.
в) Ни для какого: расходуется внутренняя энергия жидкости.
Чтобы закипела медь, нужно довести ее температуру до 2567 °С, а температура кипения свинца 1740 °С, железа 2750 °С. У какого из этих металлов силы притяжения его молекул друг к другу наименьшие?
а) У меди. б) У свинца. в) У железа.
Если известно затраченное на испарение жидкости количество теплоты Q то какой формулой следует воспользоваться для нахождения массы образовавшегося пара?
a) m = Q/L. б ) m = Q/λ. в) m = Q/q.
В тазу находилось 4 кг воды. Через несколько дней она испарилась. Сколько энергии получила на это вода от окружающей среды?
а) 9,2 · 106 Дж. 6) 9,2· 107 Дж.
в) Ответить нельзя, так как не указана температура.
Сконденсировалось 400 г паров эфира и полученная жидкость остыла до комнатной температуры (20 °С). Какое при этом выделилось количество теплоты?
а) 1,7 · 106 Дж. 6) 1,8 · 105 Дж. в) 1,7· 105 Дж.
Как известно, «обратный» нагреванию процесс — охлаждение, «обратный» плавлению — отвердевание. Какой «обратен» кипению?
а) Испарение. б) Конденсация. в) Таяние.
Какой тип теплового двигателя особенно широко применяется в современной технике?
а) Турбина. б) ДВС. в) Реактивный.
Почему КПД теплового двигателя в принципе не может быть равен 100% (всегда меньше)?
а) Потому что неизбежны потери энерг ии в результате теплопередачи.
б) Потому что существует трение в движущихся частях двигателя.
в) Потому что часть энергии передается холодильнику.
В сосуды с водой одинаковой температуры поставлены бутыли с квасом, из которых левая обернута марлей. В какой из них квас остынет лучше?
а) № 1.
б) № 2.
в) Одинаково.
Какой вид парообразования жидкости — испарение или кипение — происходит при постоянной температуре?
а) Испарение.
б) Кипение.
в) Кипение только в закрытом сосуде.
При комнатной температуре (20 °С) железо — твердое тело, кислород — газ, эфир — жидкость. Какое из этих веществ должно обладать самой низкой температурой кипения? (Проверьте свой ответ по таблице 5 учебника.)
а) Железо.
б) Кислород.
в) Эфир.
Какое условие необходимо выполнить, чтобы вычислить количество теплоты, расходуемое на кипение вещества, по формуле Q = Lm?
а) Вещество должно находиться в жидком состоянии.
б) Вещество должно быть нагрето до высокой температуры.
в) Вещество должно находиться при температуре кипения.
Вычислите затраты энергии, произведенные для того, чтобы испарить 3 кг воды.
а) 6.9 · 106 Дж. 6) 6,9 · 107 Дж. в) 6,9 · 108 Дж.
Какое количество теплоты выделится при конденсации водяного пара массой 1,5 кг и остывании полученной воды до 30 °С?
а) 38,9 · 106 Дж. б) 36,3 · 105 Дж. в) 38,9 · 105 Дж.
Почему пар, имеющий температуру 100 °С, обжигает кожу сильнее, чем кипяток?
а) Потому что пар лучше, чем кипяток, контактирует с кожей.
б) Потому что пар, конденсируясь, выделяет энергию, которая усиливает его тепловое действие.
в) Потому что струя пара обладает большей скоростью, чем струя кипятка.
Определите КПД паровой турбины, если при совершении полезной работы, равной 1,408 ·10 Дж, на получение пара было затрачено 100 кг природного газа.
а) 45%. 6) 35%. в) 32%.
Какое значение КПД теплового двигателя маловероятно, а какое — ошибочно: 20%, 40%, 80%, 100%?
а) 80% — маловероятно, 100% — ошибочно.
б)40% — маловероятно, 100% — ошибочно.
в) 80% — маловероятно, 20% — ошибочно.
Вход в личный кабинетКонтекстная рекламаУЗИП серии ETHERNET Для защиты оборудования, использующего интерфейс Ethernet. От гроз, электростатических разрядов и др.
Щитовое оборудование CHINT Официальный представитель производителя CHINT.
Силовые автоматические выключатели CHINT Такое нельзя пропустить! Смотрите запись от 1 февраля 2021 г. Неожиданные новинки, сенсационное партнерство.
Корпус RS52 — решение для Вас! Цените своё время и беспокоитесь о безопасности при установке электрооборудования? Вам нужен RS52 ТМ «Узола»!
Face Temp Многофункциональный терминал для распознавания лица и измерения температуры. Доставка. | Страница «/upload/file/sprav/master1.htm» не найдена. | Поиск по сайтуКонтекстная рекламаЛестничные лотки LESTA IEK® Металлические кабельные лотки высотой: 55, 80, 100, 150 мм. Высокая нагрузка и стойкость к коррозии. Надежная прокладка кабельной трассы.
Автоматические выключатели CHINT Широкий ассортимент электрооборудования и низковольтной аппаратуры удобно приобрести в интернет магазине официального представителя.
Автоматические выкл. ВА88 MASTER IEK Рабочее напряжение до 690 В. Служат для защиты электрических сетей от КЗ, перегрузки, снижений напряжения. Компактные размеры.
H07RN-F медный кабель от производителя Кабели по международному стандарту. Напрямую с завода, доставка по всей России, комплексные заказы.
Надёжное электрощитовое оборудование! Широкий ассортимент, доступные цены и высокое качество. Добро пожаловать на страницы каталога ГК «Узола»!
Свежий номерРассылкаПодпишитесь на нашу бесплатную рассылку! */ ]]]]>]]> |
Как расплавить алюминиевые банки и фольгу в домашних условиях
Вы можете расплавить алюминий дома, чтобы использовать его в научных или художественных проектах. (Маркос Андре)Алюминиевые банки и фольгу легко расплавить, чтобы переработать чистый металл. Алюминий полезен, потому что он легкий, безопасный для еды и кожи, податливый и устойчивый к коррозии. Вылейте расплавленный алюминий в формы, чтобы сделать посуду, украшения, скульптуры или украшения.
Точка плавления алюминия
Утилизация банок и фольги — это просто, но это проект только для взрослых, потому что вам нужна высокая температура.Температура плавления алюминия составляет 660,32 ° C или 1220,58 ° F. Это намного выше, чем тепло, выделяемое духовкой или грилем (вот почему алюминий отлично подходит для кухонной посуды), но ниже, чем температура плавления железа (1535 ° C или 2795 ° F) или нержавеющей стали (около 1500 ° C или 2750 ° F). Чтобы достичь точки плавления алюминия, вам понадобится горелка для бутана (1430 ° C или 2610 ° F), пропановая горелка (1995 ° C или 3623 ° F) или печь для обжига.
Материалы для плавки алюминия
- Алюминиевые банки или фольга
- Горелка для бутана или пропана или электрическая печь
- Чугунная сковорода или стальная чаша
- Термостойкие перчатки
- Металлические щипцы
- Формы для расплавленного алюминия
Банки не нужно чистить перед плавлением, если они не покрыты грязью или песком.Органические материалы, такие как остатки соды или пластиковое покрытие, сгорают в процессе плавления.
Как расплавить алюминий
- Раздавите банки и смять фольгу, чтобы как можно больше в вашей миске или сковороде. Ожидайте, что на каждые 40 банок будет приходиться около одного фунта алюминия.
- Безопасность прежде всего! Наденьте защитные очки и термостойкие перчатки. Соберите длинные волосы назад и наденьте длинные брюки и обувь с закрытыми носками.
- Если вы используете печь, нагрейте ее до 1220 ° F или немного выше (стараясь оставаться ниже точки плавления стали или железа, в зависимости от того, что вы используете).Поместите алюминиевый контейнер в печь. Он плавится почти сразу после достижения точки плавления, но подождите не менее 30 секунд, чтобы весь алюминий расплавился. В теплозащитных перчатках осторожно извлеките емкость из печи с помощью щипцов.
- Если вы используете фонарик, поместите алюминиевый контейнер на жаропрочную поверхность. Нагрейте алюминий, стараясь не повредить емкость. Это особенно важно, если вы используете пропановую горелку, потому что пропан может гореть при температуре, достаточной для плавления железа и стали!
- После того, как у вас будет расплавленный алюминий, вылейте его в форму (поищите творческие идеи на YouTube).Вы можете поместить форму, полную алюминия, в ведро с холодной водой, но будьте осторожны, потому что тепло будет производить много пара. В противном случае дайте форме остыть и затвердеть самостоятельно. Для затвердевания металла потребуется около 15 минут.
- Возможно, в вашем контейнере остались остатки алюминия. Вы можете выбить его из контейнера, постучав им о твердую поверхность. Другой вариант — освободить его, изменив температуру контейнера (либо нагревая, либо охлаждая его). Это работает, потому что алюминий и контейнер имеют разные значения коэффициента расширения.
Переработка алюминия
Около 36% алюминия в США производится из переработанного металла, в то время как Бразилия лидирует в мире по переработке алюминия, повторно используя 98,2% металла. Переработка требует 5% энергии, необходимой для очистки элемента от его руды.
Ссылки
- Greenwood, Norman N .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- Моррис, Дж. (2005). «Сравнительные LCA для рециркуляции обочины по сравнению с захоронением или сжиганием с рекуперацией энергии». Международный журнал оценки жизненного цикла , 10 (4), 273–284.
- Оскамп, С. (1995). «Сохранение и переработка ресурсов: поведение и политика». Журнал социальных проблем . 51 (4): 157–177. DOI: 10.1111 / j.1540-4560.1995.tb01353.x
- Шлезингер, Марк (2006). Переработка алюминия . CRC Press. ISBN 978-0-8493-9662-5.
Сравнение температур плавления припоя, олова и свинца | Эксперимент
Электрический припой представляет собой сплав олова с одним или несколькими другими металлами.Припои на основе олова и свинца были широко доступны, но теперь в производстве используются припои, не содержащие свинца, и становится все труднее получить припои на основе свинца.
В этом эксперименте ученики нагревают образцы олова, свинца и припоя олово-свинец, чтобы сравнить их точки плавления, наблюдая, что металлический сплав имеет гораздо более низкую температуру плавления, чем любой из чистых металлов. Это показывает, насколько с таким сплавом удобнее и безопаснее работать при пайке.
Эксперимент удобно проводить группами по два человека и займет около 30 минут.
Оборудование
Аппарат
- Защита глаз
- Горелка Бунзена
- Штатив
- Термостойкий мат
- Треугольник Пипекле
- Крышка тигля
Химическая промышленность
- Олово мелкое
- Свинец (ТОКСИЧНЫЙ, ОПАСНЫЙ ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫ), мелкий кусок
- Припой без флюса, мелкий кусок
Примечания по охране труда, технике безопасности и технике
- Прочтите наше стандартное руководство по охране труда и технике безопасности.
- Всегда используйте защитные очки. Будьте очень осторожны, чтобы избежать контакта с расплавленными каплями металла. Обеспечьте хорошую вентиляцию. Студентам-астматикам может быть рекомендовано работать в вытяжном шкафу.
- Олово, Sn (s) — см. CLEAPSS Hazcard HC102A.
- Свинец, Pb (s), (ТОКСИЧНЫЙ, ОПАСНЫЙ ДЛЯ ОКРУЖАЮЩЕЙ СРЕДЫ) — см. CLEAPSS Hazcard HC056.
- Припой без флюса — важно, чтобы припой не содержал флюса. Пары, образующиеся при использовании припоя, содержащего флюс на канифольной основе, могут раздражать дыхательную систему и в некоторых случаях вызывать сенсибилизацию.
Процедура
Показать в полноэкранном режиме- Поместите небольшой кусок олова, свинца и припоя на крышку перевернутого тигля. Убедитесь, что вы знаете, какая шишка какая!
- Установите крышку тигля на глиняный треугольник на штативе. Поместите зажженную конфорку Бунзена на термостойкий коврик и осторожно нагрейте крышку.
- Посмотрите на три куска, чтобы увидеть порядок их плавления.
- Когда все три расплавятся, выключите горелку Бунзена и дайте всему остыть.
- Обратите внимание на порядок, в котором комки снова затвердевают.
Учебные заметки
Напомните учащимся об опасностях контакта с горячим расплавленным металлом.
Хорошая вентиляция лаборатории важна, особенно если проводится большое количество экспериментов. Астматикам следует предложить проводить свои эксперименты с использованием вытяжного шкафа.
Общая проблема этого эксперимента заключается в том, что ученики забывают, какая шишка какая.
Точки плавления олова и свинца составляют 232 ° C и 328 ° C соответственно, в то время как припой плавится при более низкой температуре, чем любой из них. (Бессвинцовый припой имеет тенденцию плавиться при температуре около 220 ° C.) Таким образом, порядок плавления следующий: припой, олово и свинец, а порядок затвердевания — противоположный.
Металлические сплавы классифицируются как твердые растворы и обычно получают путем смешивания расплавленных металлов в соответствующем соотношении.
Если это соответствует уровню способностей, учащихся следует попросить сравнить обычный твердожидкостный раствор с раствором сплава.
Дополнительная информация
Это ресурс из проекта «Практическая химия», разработанного Фондом Наффилда и Королевским химическим обществом. Этот сборник из более чем 200 практических занятий демонстрирует широкий спектр химических концепций и процессов. Каждое упражнение содержит исчерпывающую информацию для учителей и технических специалистов, включая полные технические заметки и пошаговые инструкции. Практическая химия сопровождает практическую физику и практическую биологию.
© Фонд Наффилда и Королевское химическое общество
Проверено на здоровье и безопасность, 2016
Олово — точка плавления — точка кипения
Олово — точка плавления и температура кипения
Температура плавления олова 231,93 ° C .
Точка кипения олова 2602 ° C .
Обратите внимание, что эти точки связаны со стандартным атмосферным давлением.
Точка кипения — насыщение
В термодинамике термин насыщение определяет состояние, при котором смесь пара и жидкости может существовать вместе при заданных температуре и давлении.Температура, при которой начинает происходить испарение (кипение) для данного давления, называется температурой насыщения или точкой кипения . Давление, при котором начинается испарение (кипение) для данной температуры, называется давлением насыщения. Если рассматривать температуру обратного перехода от пара к жидкости, ее называют точкой конденсации.
Точка плавления — насыщение
В термодинамике точка плавления определяет состояние, при котором твердое тело и жидкость могут находиться в равновесии.Добавление тепла превратит твердое вещество в жидкость без изменения температуры. Температура плавления вещества зависит от давления и обычно указывается при стандартном давлении. Когда рассматривается как температура обратного перехода от жидкости к твердому телу, она упоминается как точка замерзания или точка кристаллизации.
Олово — Свойства
| Элемент | Олово |
|---|---|
| Атомный номер | 50 |
| Символ | Sn |
| Категория элемента | Бедный металл |
| Фаза в STP | цельный |
| Атомная масса [а.е.м.] | 118.71 |
| Плотность при стандартной температуре [г / см3] | 7,31 |
| Электронная конфигурация | [Кр] 4д10 5с2 5п2 |
| Возможные состояния окисления | +2,4 |
| Сродство к электрону [кДж / моль] | 107,3 |
| Электроотрицательность [шкала Полинга] | 1,96 |
| Энергия первой ионизации [эВ] | 7,3438 |
| Год открытия | неизвестно |
| Первооткрыватель | неизвестно |
| Тепловые свойства | |
| Температура плавления [шкала Цельсия] | 231.93 |
| Точка кипения [шкала Цельсия] | 2602 |
| Теплопроводность [Вт / м · К] | 67 |
| Удельная теплоемкость [Дж / г К] | 0,227 |
| Теплота плавления [кДж / моль] | 7.029 |
| Теплота испарения [кДж / моль] | 295,8 |
–
–
–
Припой из легкоплавкого и низкотемпературного сплава
Эти сплавы часто называют «легкоплавкими», потому что они легко плавятся при относительно низкой температуре по сравнению с большинством припоев.Эти сплавы состоят из двух или более следующих элементов: висмута, олова, свинца, кадмия и индия.
Каждый из этих ингредиентов используется для придания сплаву определенных характеристик и свойств. Сплавы могут быть выбраны в пропорциях для получения бинарных третичных сплавов, которые плавятся значительно ниже их легирующих элементов. Они либо эвтектические, что означает, что они плавятся при одной температуре (как чистый металл), либо неэвтектические, что означает, что у них есть диапазон плавления. Этот диапазон определяется как ликвидус — температура, выше которой они полностью жидкие, и солидус — температура, ниже которой они полностью твердые.Температуры между ними определены как «пастообразный диапазон».
Характеристики этих сплавов включают: низкое давление пара, хорошую теплопроводность, простоту обращения, высокую текучесть жидкости, возможность повторного использования и контролируемые термические размерные свойства. С помощью этого последнего элемента можно изготавливать сплав с минимальной усадкой при затвердевании. В отличие от большинства металлов, чистый висмут расширяется на 3,3% объема при переходе от жидкого состояния к твердому. Это расширение используется в сплавах, содержащих висмут, для компенсации усадки при затвердевании.Сплавы, содержащие более 55% висмута, расширяются, а сплавы с менее 48% сжимаются при затвердевании. Между сплавами наблюдается небольшое изменение объема. Изменение объема из-за охлаждения представляет собой простую линейную усадку, но некоторые сплавы показывают изменения в структуре сплава, которые позволяют отливкам из этих сплавов иметь размеры, такие же или большие, чем размеры формы, в которую они были отлиты.
Некоторые из этих изменений размеров могут продолжаться в течение 1000 часов после затвердевания.Большинство этих сплавов перестают расти через 24 часа.
Применение легкоплавких сплавов
| Устройства безопасности | Спринклеры пожарные, Заглушки котлов, автоматические противопожарные двери и т. Д. |
| Литейный цех | Изготовление лекал, пробного литья, плавких стержней и т. Д. |
| Радиационная защита | Постоянные формы для защиты отливок. |
| Склеивание и герметизация | Припайка к стеклу и термочувствительным устройствам. Предотвращает коробление тонкостенной трубы на больших радиусах изгиба. |
| Гибка труб | Предотвращает коробление тонкостенной трубы при резких радиусах изгиба. |
| Электроформование | Для изготовления одноразовых оправок сложной формы. |
Низкотемпературные сплавы или плавкие вставки широко используются во многих отраслях промышленности.Благодаря своим уникальным характеристикам, они находят все больше применений для этих сплавов в электронных сборках.
Низкотемпературные сплавы содержат два или более из следующих элементов: висмут, олово, свинец, серебро, кадмий и / или индий.
Конкретные характеристики этих сплавов включают низкое давление пара, хорошую теплопроводность, легкость оплавления, высокую текучесть жидкости и контролируемые размерные свойства.
Легкоплавкие сплавы
| Составляющие — вес в процентах | Точки плавления | |||||||||
| Сплав | Висмут | Вести | Банка | Кадмий | Индий | Серебро | Солидус | Ликвидус | ||
| Обозначение | Би | Pb | Sn | CD | В | Ag | ° F | ° C | ° F | ° C |
| 117 | 44.7 | 22,6 | 8,3 | 5,3 | 19,1 | 0 | 117 | 47 | 117 | 47 |
| 136 | 49 | 18 | 12 | 0 | 21 год | 0 | 136 | 58 | 136 | 58 |
| 158 | 50 | 26.7 | 13,3 | 10 | 0 | 0 | 158 | 70 | 158 | 70 |
| 158–190 | 42.5 | 37,2 | 11,3 | 9 | 0 | 0 | 158 | 70 | 190 | 88 |
| 174 | 57 | 0 | 17 | 0 | 26 год | 0 | 174 | 79 | 174 | 79 |
| 203 | 52.5 | 32 | 15.5 | 0 | 0 | 0 | 203 | 95 | 203 | 95 |
| 255 | 55.5 | 44,5 | 0 | 0 | 0 | 0 | 255 | 124 | 255 | 124 |
| 281 | 58 | 0 | 42 | 0 | 0 | 0 | 281 | 138 | 281 | 138 |
| 281-338 | 40 | 0 | 60 | 0 | 0 | 0 | 281 | 138 | 338 | 170 |
| 291-325 | 14 | 43 год | 43 год | 0 | 0 | 0 | 291 | 144 | 325 | 163 |
| 244 | 0 | 0 | 48 | 0 | 52 | 0 | 244 | 118 | 244 | 118 |
| 296 | 0 | 0 | 0 | 0 | 97 | 3 | 296 | 147 | 296 | 147 |
| 293 | 0 | 30.5 | 51,2 | 18,3 | 0 | 0 | 293 | 145 | 293 | 145 |
| 300-302 | 0 | 15 | 0 | 0 | 80 | 5 | 300 | 149 | 302 | 150 |
| 307-323 | 0 | 18 | 70 | 0 | 12 | 0 | 307 | 153 | 323 | 162 |
| 320-345 | 0 | 30 | 0 | 0 | 70 | 0 | 320 | 160 | 345 | 174 |
| Весовой процент компонентов | ||||||
| Сплав | висмут | Свинец | Олово | Кадмий | Индий | Серебро |
| Обозначение | Bi | Пб | Sn | Cd | В | Ag |
| 117 | 44.7 | 22,6 | 8,3 | 5,3 | 19,1 | 0 |
| 174 | 57 | 0 | 17 | 0 | 26 | 0 |
| 281 | 58 | 0 | 42 | 0 | 0 | 0 |
| 281-338 | 40 | 0 | 60 | 0 | 0 | 0 |
| 291-325 | 14 | 43 | 43 | 0 | 0 | 0 |
| 244 | 0 | 0 | 48 | 0 | 52 | 0 |
| Точки плавления | |||
| Солидус | Ликвидус | ||
| ° F | ° С | ° F | ° С |
| 117 | 47 | 117 | 47 |
| 174 | 79 | 174 | 79 |
| 281 | 138 | 281 | 138 |
| 281 | 138 | 338 | 170 |
| 291 | 144 | 325 | 163 |
| 244 | 118 | 244 | 118 |
Легкоплавкие оксидные стекла, полученные при температуре плавления 500 ° C
Исследование химического состава стекол на основе фосфата олова
Во-первых, мы исследовали химический состав основного фосфатного стекла, пригодного для плавления при 500 ° C.Существует обычная зависимость между температурой плавления ( T м ) и температурой стеклования ( T г ), то есть T г / T м ~ 2/3 21 . Таким образом, эталонный показатель T г составляет примерно 243 ° C для достижения плавления при 500 ° C. В этом исследовании мы сосредоточились на системе стекла SnO – P 2 O 5 , поскольку сообщалось, что стекла SnO – P 2 O 5 обычно имеют более низкие значения T г ниже 300 ° C. 4, 5, 17, 22,23,24 .Важно поддерживать состояния Sn 2+ во время плавления при 500 ° C, поскольку сообщается, что реакция окисления Sn 2+ начинается примерно при 450 ° C 25 .
В таблице 1 представлены химические составы и значения T g нескольких стекол на основе SnO – P 2 O 5 , полученных при 500 ° C. Кривые дифференциального термического анализа (ДТА) показаны на рис. 1а. Столбики ошибок этих значений T g превышают 5 ° C, что незначительно больше, чем стандартные значения ошибок, оцененные путем экстраполяции кривой DTA.Альтернативный состав ID2 (50SnO – 40P 2 O 5 ) также показан для понимания изменения T г с добавлением либо 10 мол.% SnO (для ID3), либо 10 мол. % от K 2 O (для ID4). Это говорит о том, что полученные стекла являются термодинамически метастабильными переходными состояниями, в которых концентрация групп ОН 17 или формирование сетки несколько отличается. Поскольку базовый химический состав аналогичен, ожидается, что стекло с более высокой T г будет демонстрировать более высокую химическую стойкость.Иногда мы наблюдали коричневатую окраску приготовленного стекла в стекле 60SnO – 40P 2 O 5 , хотя все исходные химические вещества не содержали углеродных частиц. Поскольку в образце коричневатого цвета (рис. S1) не наблюдаются заметные дифракционные пики, ожидается, что в процессе плавления могут образоваться небольшие количества нанокристаллитов Sn. На рис. 1б показаны спектры оптического поглощения 50SnO – 50P 2 O 5 (ID1), 55.6SnO – 44.4P 2 O 5 (ID2), 60SnO – 40P 2 O 5 ( ID3) и 10K 2 O – 50SnO – 40P 2 O 5 (ID4).На вставке — расширенные спектры в области края оптического поглощения. Если мы оценим край оптического поглощения из экстраполяции коэффициента поглощения, как показано пунктирной линией на рисунке, зависимость от состава может быть выяснена. Было обнаружено, что эти края оптического поглощения были расположены ниже 330 нм и что края оптического поглощения смещались в синий цвет с уменьшением значений T g , как показано на фиг. 1c. Для стекла, легированного SnO, полученного обычным методом закалки в расплаве, край оптического поглощения из-за катиона Sn 2+ смещается в красную сторону с увеличением доли SnO 26 .Однако такой сдвиг края в зависимости от доли SnO в данном случае не наблюдается. Принимая во внимание T g , ожидается, что концентрация группы ОН влияет на синее смещение края оптического поглощения. Это предположение подтверждается спектрами поглощения в инфракрасной (ИК) области. Коэффициенты поглощения этих стекол в ИК-области увеличиваются с уменьшением значений T g , тем самым предполагая, что более высокая концентрация OH вызывает большее снижение T g .Полосы поглощения при 1570 нм и 2135 нм относятся к обертону растяжения P – OH и комбинации растяжения – изгиба мод P – OH, соответственно 27, 28 . На рисунке 1d показан коэффициент поглощения пика 2135 нм как функция T g . Примечательно, что поверхность стекла 50SnO – 50P 2 O 5 с самой высокой концентрацией ОН быстро повреждалась при погружении в воду при комнатной температуре (КТ). Однако, если доля SnO превышает 60 мол.%, Для стекол SnO – P 2 O 5 потребуется температура плавления выше 500 ° C, и они иногда проявляют непрозрачность или коричневатую окраску.Стекло ID1 по водостойкости было худшим, а ID4 — лучшим среди этих стекол. Из этих спектров мы пришли к выводу, что ID4 (10K 2 O – 50SnO – 40P 2 O 5 ) был лучшим кандидатом как с легкоплавкими свойствами, так и с химической стойкостью среди этих композиций. Поскольку pH воды снизился (кислый) после испытания этих стекол на растворение, мы можем сделать вывод, что существует обычный механизм реакции гидролиза между водой и фосфатными цепями 18 .
Таблица 1 Химический состав и значения температуры стеклования ( T г ) стекол на основе SnO – P 2 O 5 . Рис. 1Тепловые и оптические свойства стекла на основе SnO – P 2 O 5 : ( a ) Кривые ДТА для SnO – P 2 O 5 стекол на основе , перечисленных в таблице 1. ( b ) Спектры оптического поглощения 50SnO – 50P 2 O 5 (ID1), 55.6SnO – 44.4P 2 O 5 (ID2), 60SnO – 40P 2 O 5 (ID3) и 10K 2 O – 50SnO-40P 2 O 5 (ID4) стекла плавили при 500 ° C в течение 30 мин. На вставке показаны расширенные спектры в области края оптического поглощения. Пунктирной линией показана линия экстраполяции ID1 для края оптического поглощения. ( c ) Взаимосвязь края оптического поглощения и T g этих очков. ( d ) Соотношение между коэффициентом поглощения при приблизительно 2135 нм и T г .
Мы предположили, что водостойкость стекол K 2 O – SnO – P 2 O 5 может зависеть от структурных изменений в области P 2 O 5 . Для изучения структурных изменений на основе химического состава были измерены спектры ядерного магнитного резонанса (ЯМР) 31 P вращения под магическим углом (MAS). На рис. 2а показаны спектры MAS ЯМР 31 P стекол на основе SnO – P 2 O 5 , которые перечислены в таблице 2.Различные фосфатные звенья Q i в спектрах ЯМР 31 P можно идентифицировать по химическому сдвигу, которому приписывается число мостиковых атомов кислорода 11, 31,32,33 . Пики Q 2 , Q 1 и Q 0 в стеклах на основе олова-фосфата расположены при -33 ppm, -19 ppm и -9 ppm соответственно 34 . Из спектров ЯМР видно, что димерная структура Q 1 , химический сдвиг которой составляет примерно -19 м.д., является основной фосфатной единицей в этих стеклах.Рассчитанные доли Q n единиц показаны в Таблице S1. Во всех образцах наблюдалось небольшое количество звена Q 0 . Ранее предполагалось, что блоки Q 0 и Q 1 , которые являются блоками с высокой степенью делокализации электронов, влияют на химическую (водную) стойкость по сравнению с блоком Q 2 . Иными словами, если доля таких сильно делокализованных электронов единиц велика, стекло будет демонстрировать отличную водостойкость 33 .Однако, вопреки нашим ожиданиям, заметной разницы между этими очками не было. Кроме того, хотя доли (Q 0 + Q 1 ) превышают 80% во всех системах, эти стекла обладают низкой водостойкостью. Таким образом, мы предполагаем, что остаточные группы ОН влияют на водостойкость этих стекол из-за низкой температуры плавления.
Рисунок 2Структурный анализ стекол на основе SnO – P 2 O 5 , плавленных при 500 ° C в течение 1 ч.( a ) 31 P MAS ЯМР-спектры стекол на основе SnO – P 2 O 5 . Пунктирными линиями обозначены компоненты Q 0 , Q 1 и Q 2 после пика деконволюции. ( b ) Sn L 2 -краевые XANES-спектры стекол на основе SnO – P 2 O 5 и SnO. ( c ) XANES-спектры Sn K-края стекол на основе SnO – P 2 O 5 . ( d ) FT EXAFS Sn K-кромка XAFS.Область k для FT составляет от 3,4 до 12 Å -1 .
Таблица 2 Химический состав и потеря массы стекол KSP после испытания на погружение при 50 ° C в течение 72 часов. Однако стекло KSP, легированное 1.0La 2 O 3 , не было получено из-за сильного образования пузырьков во время термообработки при 500 ° C.Поскольку это приготовление проводили в условиях окружающего давления или пониженного давления при 500 ° C, что было сравнимо с обычной температурой для окисления Sn 2+ , предполагалось, что большинство разновидностей олова были двухвалентными 25 .Поскольку Sn 2+ более предпочтителен для легкоплавкости по сравнению с Sn 4+ , важно экспериментальное подтверждение 29 . Чтобы подтвердить валентное состояние олова, мы измерили спектры ближней структуры рентгеновского поглощения Sn L-края (XANES) в соответствии с предыдущей статьей 29 . На рис. 2b показана кромка Sn L 2 стекол ID2 и ID4 вместе с кромкой SnO. По сравнению с эталоном (SnO) очевидно, что примерно все виды Sn являются двухвалентными, и локальное координационное состояние SnO не меняется кардинально при добавлении K 2 O.Поскольку также предполагалось, что на связность SnO будет влиять химический состав, мы также измерили спектры тонкой структуры поглощения рентгеновских лучей на K-крае Sn (XAFS). На рис. 2с показаны спектры XAFS Sn K-края стекол ID2 и ID4 с SnO в качестве эталона. Поскольку формы спектров XANES аналогичны, результат согласуется с оценкой валентности по краю L 2 . На рисунке 2d показано преобразование Фурье (FT) расширенной области XAFS (EXAFS) Sn K-edge XAFS.FT выполняли с областью k от 3,4 до 12 Å -1 . Добавление K 2 O изменяет структуру SnO, т.е. расстояние Sn – O увеличивается, а координационное число увеличивается за счет добавления K 2 O. Довольно странно, что расстояние Sn – O для стекол K 2 O-замещенных SnO – P 2 O 5 ближе к SnO, чем у SnO-богатых SnO – P 2 O 5 стекло. Сообщалось, что SnO имеет тетрагональную элементарную ячейку со структурой глета 30 .Однако предполагается, что связь P = O звена P 2 O 5 в структуре SnO – P 2 O 5 может увеличивать межатомное расстояние Sn 2+ из-за отталкивания. электронов. Следовательно, ожидается, что катионы калия будут располагаться рядом с фосфатными цепями для предпочтительной компенсации заряда, а остаточные катионы Sn 2+ будут существовать в более высоком координационном состоянии, аналогичном структуре SnO. Поскольку спектры ЯМР 31 P и краевые XANES-спектры Sn L 2 подобны, изменение координации катиона Sn при добавлении K 2 O является одной из причин повышения водостойкости.По результатам исследования состава было выбрано стекло 10K 2 O – 50SnO – 40P 2 O 5 , которое далее обозначается как стекло KSP и имеет наименьшую концентрацию ОН и наибольшую T г среди этих стекол, как состав стекла на основе фосфата олова.
Повышение водостойкости стекол на основе КСП
Хотя мы выбираем стекло КСП в качестве основного основного состава, его свойство водостойкости является недостаточным.Следовательно, требуется дополнительная конструкция материала при температуре плавления 500 ° C. Поведение фосфатных стекол при растворении часто обсуждается в зависимости от природы поверхности стекла и скорости гидролиза P – O – P. Естественно, что состав и структура стекол влияют на поведение при растворении. Оксиды щелочных металлов и фосфатные звенья Q 2 и Q 3 увеличивают скорость их растворения, тогда как катионы с высокой напряженностью поля, такие как Al 2 O 3 и Fe 2 O 3 , снижают скорости растворения.Иногда сообщалось, что смешивание оксидов щелочных металлов, т.е. смешанный щелочной эффект оксидных стекол , , улучшает водостойкость стекол 35, 36 . Недавно Онодера и др. . предположил, что коррелированное парное расположение Na и K было внутренней причиной смешанного щелочного эффекта. На основании предыдущих отчетов было приготовлено несколько стекол, содержащих два оксида щелочных металлов. На рис. 3а представлена фотография стекол x Li 2 O — (10 — x ) KSP, полученных при 500 ° C.Прозрачность уменьшается с увеличением концентрации Li 2 O, и, в частности, стекло без O K 2 непрозрачно, что непригодно для оптических применений (см. Рис. S2). Аналогичный результат был также подтвержден в системе Na 2 O-замещенных x Na 2 O — (10 — x ) KSP (рис. 3b). В Na-замещенной системе стекло КСП также показало лучшую прозрачность среди них. Поведение кристаллизации оценивается путем получения рентгенограмм.На рисунке 3c показаны дифрактограммы стекол KSP, 10Na 2 O-SP и 10Na 2 O-SP вместе с диаграммами Объединенного комитета по порошковым дифракционным стандартам (JCPDS) Sn (№ 00-004-0673), SnO. (№ 01-072-1012) и Sn 2 P 2 O 7 (№ 00-056-0358). В этих стеклах не наблюдалось заметного выделения кристаллитов. Следовательно, предполагается, что 500 ° C слишком низка для того, чтобы расплавить гомогенное стекло и проявить смешанный щелочной эффект, и во время плавления происходит только фазовое разделение.Хотя причина, по которой введение K 2 O дает лучший результат среди оксидов щелочных металлов, остается неясной, предполагается, что катионный радиус K 2 O является подходящим для прозрачности и поведения с низкой температурой плавления.
Рисунок 3Прозрачность щелочно-замещенных стекол КСП. ( a ) Фотографии x Li 2 O — (10 — x ) KSP и ( b) x Na 2 O- (10- x ) стекла KSP, расплавленные при 500 ° C в течение 10 мин.Фракции замещения: 0, 5 и 10. ( c ) Рентгенограммы KSP, 10Na 2 O-SP и 10Na 2 O-SP стекол вместе с JCPDS-диаграммами Sn (№ 00-004- 0673), SnO (№ 01-072-1012) и Sn 2 P 2 O 7 (№ 00-056-0358).
Для повышения водостойкости легкоплавкого стекла KSP мы попытались добавить четвертый компонент. В таблице 2 показаны химический состав и потеря веса стекол KSP после испытания погружением в воду при 50 ° C в течение 72 часов.Данные в таблице 2 показывают, что концентрация добавки кажется менее эффективной по сравнению с элементами. Среди нескольких оксидов металлов мы обнаружили, что La 2 O 3 может эффективно улучшить водостойкость материалов. Об улучшении водостойкости за счет добавления La 2 O 3 сообщалось в нескольких системах стекла, полученных методом закалки в расплаве 37, 38 . В настоящей стеклянной системе также подтверждается улучшенная водостойкость благодаря добавлению La 2 O 3 , даже при температуре плавления 500 ° C, что намного ниже, чем обычная температура плавления.Также следует отметить, что добавление La 2 O 3 не вызывает ухудшения прозрачности стекла KSP. Мы предполагаем, что катионы La соединяются с фосфатными звеньями, чтобы предотвратить разделение фаз.
Физические свойства стекла KSP, легированного La
2 O 3Предыдущие данные показывают, что стекло KSP (LKSP), легированное 0,5La 2 3 , является многообещающим кандидатом для неорганических низко- плавильные стаканы. В течение трех лет мы подтвердили, что стекло ЛКСП стабильно в условиях окружающей среды (25 ° C, влажность ~ 60%), несмотря на значительное количество K 2 O, поскольку La 2 O 3 и SnO предотвратить реакцию гидролиза.Поэтому мы исследовали структуру и физические свойства стекла ЛКСП. На рисунке 4 представлено сравнение очков KSP и LKSP. Наблюдается увеличение T g при добавлении La 2 O 3 , как показано на рис. 4а, и одновременно с этим в спектрах оптического поглощения видно уменьшение концентрации ОН (рис. 4b). . Следовательно, уменьшение количества ОН-групп за счет добавления La 2 O 3 является одной из причин увеличения T g .Эффект добавления La 2 O 3 также наблюдается на краю оптического поглощения. Хотя молярная доля SnO несколько снижается при добавлении La 2 O 3 , край поглощения смещается в красную область, как показано на вставке к фиг. 4b. Связь между T g и этими абсорбционными свойствами была также подтверждена в образце, легированном La, как показано на фиг. 4c. Примечательно, что фракции Q n в спектрах MAS ЯМР 31 P незначительно изменены добавлением La 2 O 3 (рис.4d), а доля Q 2 увеличивается при добавлении La 2 O 3 (Таблица S1). В случае железосодержащего стекла предлагается добавлять катионы Fe, связанные с фосфатными цепями, для улучшения химической стойкости 39, 40 . По результатам соотношения Q 2 ожидается, что катионы La выполняют ту же роль, что и предыдущий отчет о фосфатной сети 39 . Поскольку у Sn L 2 -ребня XANES заметной разницы не наблюдается (рис.4e) и спектров XAFS K-края Sn (рис. 4f), предполагается, что катионы La в основном взаимодействуют с фосфатными звеньями, уменьшая концентрацию ОН при нагревании до 500 ° C, тем самым улучшая водостойкость стекла LKSP.
Рисунок 4Влияние добавки La 2 O 3 на стекла KSP. ( a) Кривые ДТА стекла КСП и стекла КСП (ЛКСП), легированного La 2 O 3 . ( b ) Спектры оптического поглощения стекол КСП и ЛКСП. На вставке показаны расширенные спектры поглощения в области края поглощения.( c ) Край оптического поглощения и коэффициент поглощения около 2135 нм как функция T g . ( d ) 31 P MAS ЯМР-спектры стекол КСП и ЛКСП. ( e ) XANES-спектры Sn K-края стекол KSP и LKSP вместе с SnO. ( f ) FT EXAFS SnO K-edge XAFS-спектры стекол KSP и LKSP вместе с SnO.
На рисунке S3 показана кривая вязкости стекла LKSP. Экспериментальные данные могут быть подогнаны с помощью уравнения Фогеля – Фулчера – Таммана (VFT) 41,42,43 .По кривой вязкости мы можем определить несколько тепловых параметров, которые перечислены в таблице 3. В ней также показаны коэффициент теплового расширения и упругие параметры. Из термических параметров можно понять, что полученное стекло может проявлять легкоплавкие свойства, T г сравнимо с обычным легкоплавким стеклом 2,3,4,5,6,7, 8,9,10 . T г при 235 ° C близко к ожидаемому значению T г (243 ° C), основанному на соотношении: T г / T м ~ 2 / 3 21 .Исходя из хрупкости стеклообразующей жидкости, определенной Новиковым и соавт. 44 , отношение продольной и поперечной скорости звука v L / v T составляет приблизительно 1,76, что указывает на то, что стекло скорее прочное, чем хрупкое. Ожидается, что адаптация поверхности с помощью метода нанопечати может быть адаптирована к этому стеклу при температуре ниже 400 ° C, что является преимуществом не только для снижения температуры, но и для возможности применения других типов форм для поверхностной нанопечати на поверхности.Тем не менее, показатель преломления стекла LKSP составляет 1,65 нм при длине волны 633 нм, что выше, чем у обычных стекол, что дает еще одно преимущество этого легкоплавкого неорганического стекла.
Таблица 3 Тепловые и упругие свойства стекла ЛКСП.Примечательно, что стекло KLSP трудно приготовить обычным плавлением с использованием платиновых тиглей. Как показано на рис. S4, значительные повреждения поверхности Pt тигля были обнаружены после плавления при 800 ° C в атмосфере Ar. Следовательно, легкоплавкий процесс при 500 ° C с использованием водного H 3 PO 4 имеет дополнительное преимущество, заключающееся в предотвращении повреждения тиглей из-за сильной реакции восстановления.
Как упоминалось во введении, мы предполагаем, что аналог легкоплавкого неорганического стекла — это ЭП. Здесь мы сравниваем термостойкость и светостойкость стекла LKSP со стойкостью обычных EP и поликарбонатов (ПК). На рис. 5а показаны спектры пропускания стекла KSP, легированного La 2 O 3 , а также ПК после ускоренного испытания на долговечность. Для сравнения толщины ПК и стекла были нормированы на 1 мм. Для проверки свойств были проведены два ускоренных испытания: (1) ультрафиолетовое (УФ) воздействие при комнатной температуре в течение 700 часов и (2) термообработка при 200 ° C в течение 1000 часов в окружающей атмосфере.Прозрачность неорганического стекла осталась неизменной после обоих испытаний на долговечность, в то время как после обоих испытаний наблюдалось значительное ухудшение прозрачности ПК. На рис. 5б показаны фотографии ПК до и после испытаний на долговечность УФ-облучения и термообработки. Коэффициент пропускания ПК резко ухудшается после обоих испытаний на долговечность. И наоборот, прозрачность стекла не изменилась после обоих ускоренных испытаний на долговечность. Приведенные здесь результаты демонстрируют, что настоящее неорганическое стекло можно использовать в некоторых областях применения EP.В последнее время неорганические стекла были заменены органическими смолами или EP из-за их плотности, стоимости изготовления и температуры приготовления. Однако с точки зрения термической стойкости и стойкости к сильному свету существуют преимущества использования неорганических стекол. Уменьшая температуру приготовления, мы подчеркнули, что теперь открыты несколько окон применения для неорганических стекол.
Рисунок 5Пропускание стекла ЛКСП при ускоренном испытании на долговечность по сравнению с поликарбонатами (ПК).( a ) Спектры пропускания стекла ЛКСП и ПК после УФ-облучения и термообработки при 200 ° C в течение 1000 ч. ( b ) Фотографии ПК до и после испытаний на долговечность. Значительное ухудшение пропускания наблюдается в ПК, в то время как в стекле LKSP изменений не наблюдается.
В итоге мы изготовили легкоплавкое фосфатное стекло с температурой плавления 500 ° C. Подбирая химический состав и исходные материалы, можно получить бесцветные прозрачные стекла.Температура T g ниже 250 ° C, что является большим преимуществом для плавления и формовки при низких температурах. Хотя водостойкость иногда представляет собой главную проблему для легкоплавкого фосфатного стекла, это свойство можно улучшить с помощью состава и процесса приготовления. Поскольку это легкоплавкое стекло устойчиво к тепловым воздействиям и сильному освещению, оно считается новым кандидатом в бесцветное твердое вещество, которое может частично функционировать как заменитель обычных EP.
Фазовые диаграммы жидкость-твердое тело: олово и свинец
На этой странице объясняется взаимосвязь между кривыми охлаждения для жидких смесей олова и свинца и полученной фазовой диаграммой. Он также предлагает простое введение в идею эвтектической смеси.
Кривые охлаждения для чистых веществ
Предположим, у вас есть немного чистого расплавленного свинца, и вы даете ему остыть, пока он полностью не затвердеет, по мере того как вы наносите график зависимости температуры свинца от времени. Вы получите типичную кривую охлаждения для чистого вещества.
На протяжении всего эксперимента тепло теряется в окружающую среду, но температура не падает вообще, пока свинец замерзает. Это связано с тем, что в процессе замораживания выделяется тепло с той же скоростью, с какой оно теряется в окружающую среду. Энергия высвобождается при образовании новых связей — в данном случае сильных металлических связей в твердом свинце. Если вы повторите этот процесс для чистого жидкого олова, форма графика будет точно такой же, за исключением того, что точка замерзания теперь будет при 232 ° C (график для этого находится ниже на странице.)
Кривые охлаждения оловянно-свинцовых смесей
Если добавить в свинец олова, форма кривой охлаждения изменится. На следующем графике показано, что произойдет, если вы охладите жидкую смесь, содержащую около 67% свинца и 33% олова по массе.
Есть на что посмотреть:
- Обратите внимание, что при нормальной температуре замерзания свинца ничего не происходит. Добавление в него олова снижает температуру замерзания.
- Замерзание этой смеси начинается при температуре около 250 ° C.Вы начнете получать твердый свинец, но не олово. В этот момент скорость охлаждения замедляется — кривая становится менее крутой.
- Однако график еще не идет горизонтально. Хотя при превращении свинца в твердое тело выделяется энергия, с оловом ничего подобного не происходит. Это означает, что выделяется недостаточно энергии для поддержания постоянной температуры.
- Температура перестает падать при 183 ° C. Сейчас мерзнут и олово, и свинец. Как только все застынет, температура продолжает падать.
Изменение пропорций олова и свинца
Если в смеси было меньше олова, общая форма кривой остается почти такой же, но точка, в которой свинец сначала начинает замерзать, изменяется. Чем меньше олова, тем меньше падение температуры замерзания свинца. Для смеси, содержащей всего 20% олова, температура замерзания свинца составляет около 275 ° C. Вот где график внезапно стал бы менее крутым. НО . . . график будет горизонтальным (показывающий замерзание олова и свинца) при точно такой же температуре: 183 ° C.
По мере увеличения доли олова первые признаки твердого свинца появляются при все более низких температурах, но окончательное замерзание всей смеси все же происходит при 183 ° C. Это продолжается до тех пор, пока вы не добавите достаточно олова, чтобы смесь содержала 62% олова и 38% свинца. В этот момент график изменится.
Эта конкретная смесь свинца и олова имеет кривую охлаждения, которая больше похожа на кривую чистого вещества, чем на смесь. Есть только одна горизонтальная часть графика, где все замирает.Однако это все еще смесь (не раствор). Если вы посмотрите в микроскоп на твердое вещество, образовавшееся после замораживания, вы увидите отдельные кристаллы олова и свинца.
Эта конкретная смесь известна как эвтектическая смесь . Слово «эвтектика» происходит от греческого и означает «легко плавится». Эвтектическая смесь имеет самую низкую температуру плавления (которая, конечно, такая же, как температура замерзания) из всех смесей свинца и олова. Температура, при которой эвтектическая смесь замерзает или плавится, известна как температура эвтектики.
Что произойдет, если в смеси будет более 62% олова?
Вы можете проследить это точно таким же образом, представив, что вы начинаете с чистого олова, а затем добавляете к нему свинец. Кривая охлаждения чистого жидкого олова выглядит так:
Это похоже на кривую охлаждения чистого свинца, за исключением того, что температура замерзания олова ниже. Если вы добавите небольшое количество свинца в олово, так что у вас будет примерно 80% олова и 20% свинца, вы получите такую кривую:
Обратите внимание на пониженную температуру замерзания олова.Обратите внимание, что окончательное замораживание всей смеси снова происходит при 183 ° C. По мере увеличения количества свинца (или уменьшения количества олова — то же самое!) До 62% олова и 38% свинца вы снова получите эвтектическую смесь с кривой, которую мы уже рассмотрели.
Фазовая диаграмма
Построение фазовой диаграммы
Вы начинаете с данных, полученных из кривых охлаждения. Вы строите график температуры, при которой начинается первое замерзание, в зависимости от соотношения олова и свинца в смеси.Единственное, что необычно, это то, что вы рисуете температурную шкалу на каждом конце диаграммы, а не только с левой стороны.
Обратите внимание, что в левой и правой частях кривых указаны точки замерзания (точки плавления) чистого свинца и олова.
Чтобы закончить фазовую диаграмму, все, что вам нужно сделать, это провести одну горизонтальную линию поперек при эвтектической температуре. Затем вы помечаете каждую область диаграммы тем, что вы найдете в различных условиях.
Использование фазовой диаграммы
Предположим, у вас есть смесь 67% свинца и 33% олова. Это смесь из первой кривой охлаждения, построенной выше. Предположим, он находится при температуре 300 ° C. Это соответствует набору условий в области фазовой диаграммы, обозначенной как расплавленное олово и свинец.
А теперь подумайте, что произойдет, если вы охладите эту смесь. В конце концов температура упадет до точки, где она пересекает линию в следующую область диаграммы.В этот момент смесь начнет выделять твердый свинец — другими словами, свинец (но не олово) начнет замерзать. Это происходит при температуре около 250 ° C.
Теперь нужно тщательно обдумать следующий фрагмент, потому что есть два разных способа взглянуть на него. Если вас научили делать это одним способом, придерживайтесь этого — иначе вы рискуете сильно запутаться!
Задумываясь об изменении состава жидкости
При замерзании первого свинца состав оставшейся жидкости изменяется.Очевидно, он становится пропорционально богаче оловом. Это немного снижает точку замерзания свинца, и поэтому следующий кусок свинца замерзает при немного более низкой температуре, оставляя жидкость еще более богатой оловом.
Этот процесс продолжается. Жидкость становится все богаче и богаче оловом, а температура, необходимая для замораживания следующей партии свинца, продолжает падать. Набор условий температуры и состава жидкости по существу движется вниз по кривой — пока не достигнет точки эвтектики.
После достижения точки эвтектики, если температура продолжает падать, вы, очевидно, просто попадаете в область смеси твердого свинца и твердого олова — другими словами, вся оставшаяся жидкость замерзает.
Размышляя о составе системы в целом
Мы видели, что по мере того, как жидкость постепенно замерзает, ее состав меняется. Но если вы посмотрите на систему в целом, очевидно, что пропорции свинца и олова остаются неизменными — вы ничего не убираете и ничего не добавляете.Все, что происходит, — это то, что все меняется от жидкостей к твердым телам. Итак, предположим, что мы продолжаем охлаждение за пределами температуры, при которой появляется первый твердый свинец и температура падает до точки, показанной на следующей диаграмме — точки, четко расположенной в области «твердый свинец и расплавленная смесь».
Что бы вы увидели в смеси? Чтобы выяснить это, вы проводите горизонтальную связку через эту точку, а затем смотрите на ее концы.
На левом конце у вас 100% преимущество.Это твердый свинец, который замерз из смеси. В правом конце у вас есть состав жидкой смеси. Теперь он намного богаче оловом, чем вся система, потому что, очевидно, выделилось изрядное количество твердого свинца. По мере того, как температура продолжает падать, состав жидкой смеси (как показано на правом конце соединительной линии) будет приближаться к эвтектической смеси.
Он наконец достигнет эвтектического состава, когда температура упадет до температуры эвтектики — и тогда вся партия замерзнет.Очевидно, что при температуре ниже температуры эвтектики вы находитесь в области твердого свинца и твердого олова. Если вы охладите жидкую смесь в правой части фазовой диаграммы (справа от эвтектической смеси), все будет работать точно так же, за исключением того, что вместо твердого свинца образуется твердое олово. Если вы уже поняли, что произошло раньше, понять, что происходит, совсем не сложно.
Наконец. . . что произойдет, если вы охладите жидкую смесь, имеющую именно эвтектический состав? Он просто остается жидкой смесью, пока температура не упадет настолько, что все затвердеет.Вы никогда не попадете в неудобные участки фазовой диаграммы.
Смеси оловянно-свинцовые в качестве припоя
Традиционно в качестве припоя использовались смеси олова и свинца, но их использование постепенно прекращается из-за проблем со здоровьем, связанных со свинцом. Это особенно актуально, когда припой используется для соединения водопроводных труб, в которых вода используется для питья. Новые бессвинцовые припои были разработаны в качестве более безопасной замены.
Типичные старомодные припои включают:
- 60% олова и 40% свинца.Это близко к эвтектическому составу (62% олова и 38% свинца), что дает низкую температуру плавления. Он также будет плавиться и чисто замерзать в очень ограниченном диапазоне температур. Это полезно для электромонтажных работ.
- 50% олова и 50% свинца. Это будет плавиться и замерзать в более широком диапазоне температур. Когда он расплавится, он начнет замерзать при температуре около 220 ° C и, наконец, затвердеть при температуре эвтектики 183 ° C. Это означает, что он остается работоспособным в течение полезного количества времени. Это полезно, если он используется для сантехнических соединений.

