| Табл. 2. Значения температурного коэффициента линейного расширения меди при различных температурах | |||||
| t, К | α х 10 6 , К -1 | t, К | α х 10 6 , К -1 | t, К | α х 10 6 , К -1 |
| 200 | 15,2 | 450 | 17,6 | 900 | 20,9 |
| 220 | 15,6 | 500 | 17,9 | 950 | 21,4 |
| 240 | 15,9 | 550 | 18,3 | 1000 | 21,8 |
| 260 | 16,2 | 600 | 18,7 | 1050 | 22,3 |
| 280 | 16,5 | 700 | 19,4 | 1100 | 22,8 |
| 300 | 16,7 | 750 | 19,7 | 1150 | 23,3 |
| 350 | 17,0 | 800 | 20,1 | 1200 | 23,8 |
| 400 | 17,3 | 850 | 20,5 | 1250 | 24,4 |
Теплопроводность меди λ существенно снижают примеси и легирующие элементы (рис. 4).
4).
Рис. 4. Влияние содержания элементов на теплопроводность меди
Теплопроводность меди разных марок при 20°С составляет:
Марка λ , Вт(м * К)
П овышение температуры меди приводит к уменьшению ее теплопроводности (табл. 3. ).
| Табл. 3. Значения теплопроводности λ меди при различных температурах | |||||||||
| t, К | λ, Вт/(м*К) | t, К | λ, Вт/(м*К) | t, К | λ, Вт/(м*К) | t, К | λ, Вт/(м*К) | t, К | λ, Вт/(м*К) |
| 100 | 500 | 350 | 393 | 600 | 382 | 850 | 376 | 1100 | 349 |
| 150 | 435 | 400 | 391 | 650 | 379 | 900 | 364 | 1150 | 345 |
| 200 | 414 | 450 | 383 | 700 | 376 | 950 | 360 | 1200 | 342 |
| 250 | 403 | 500 | 387 | 750 | 372 | 1000 | 356 | 1250 | 338 |
| 300 | 398 | 550 | 385 | 800 | 370 | 1050 | 353 | 1300 | 334 |
Влияние температу ры на физические свойства меди на примере М0 показано в табл. 4.
4.
| Таблица   =>> v
| История открытия:Латинское название меди Cuprum произошло от названия острова Кипр, где уже в III в. до н. э. существовали медные рудники и производилась выплавка меди. Слова медь и медный встречаются в древнейших русских литературных памятниках. Русское слово «медь» производят от греческого слова, означающего рудник, копь. Нахождение в природе, получение:Медь встречается в природе как в соединениях, так и в самородном виде. Промышленное значение имеют халькопирит CuFeS2, также известный как медный колчедан, халькозин Cu2S и борнит Cu5FeS4. Вместе с ними встречаются и другие минералы меди: ковеллин CuS, куприт Cu2O, азурит Cu3(CO Такую черновую медь окончательно очищают электролизом, где изготовленные из нее аноды растворяются, на катоде оседает чистая медь, а примеси оседают на дне в виде осадка, шлама. В состав шлама могут входить такие ценные элементы, как Au, Ag, Se, Te, поэтому его подвергают дальнейшей переработке. Физические свойства:Чистая медь — тягучий вязкий металл светло-розового цвета, легко прокатываемый в тонкие листы. Плотность 8,92 г/см3, температура плавления 1083,4°C, температура кипения 2567°C. Химические свойства: В химическом отношении медь является малоактивным металлом. Однако с галогенами она реагирует уже при комнатной температуре, например, с влажным хлором образует хлорид CuCl2. При нагревании медь взаимодействует и с серой, образуя сульфид Cu2S.
В сухой атмосфере медь практически не изменяется. Во влажном воздухе на поверхности меди в присутствии углекислого газа образуется «патина» — зеленоватая пленка состава Cu(OH)2·CuCO3, содержащая также сернистые соединения меди. Важнейшие соединения: Оксид меди(I) — Cu2O, имеет красновато-коричневую окраску. Ионы меди(I) в водном растворе неустойчивы и легко подвергаются диспропорционированию:
2Cu+(водн.) Cu2+(водн.) + Cu(тв.) Соли меди(II) — образуют кристаллогидраты синего и сине-зелёного цвета, растворы солей меди(II) в большинстве случаев имеют кислую реакцию в следствие гидролиза. Сульфат меди(II), CuSO4 — белый порошок, при гидратации даёт синие кристаллы медного купороса CuSO4*5H2O, используется как фунгицид. Применение: — В электротехнике — катализатор полимеризации ацетилена — Для производства медно-окисных гальванических элементов и батарей. — Широко используются сплавы с использованием меди: латунь — сплав меди с цинком, бронза — сплав меди с оловом, мельхиор — сплав меди и никеля, и другие.  Они применяются для чеканки разменной монеты, в судостроении, в ювелирном деле. Они применяются для чеканки разменной монеты, в судостроении, в ювелирном деле. — Оксиды меди используются для получения оксида иттрия бария меди YBa2Cu3O7-x, который является основой для получения высокотемпературных сверхпроводников. Медь является необходимым элементом для всех высших растений и животных, входя в состав многих ферментов. В крови головоногих и некоторых брюхоногих моллюсков медь выполняет ту же роль, что и железо в крови человека. В организме взрослого человека содержится до 80 мг меди и для восполнения потерь необходимо поступление меди в количестве 0,9 мг в день. При недостатке меди в организме снижается активность ферментных систем и замедляется белковый обмен и нарушается рост костных тканей.
Однако содержание меди в питьевой воде не должно превышать 1 мг/л, многие соединения меди обладают токсичными свойствами. Жерновникова А., Третьякова М. Источники: Википедия: http://ru.  wikipedia.org/wiki/Cu, wikipedia.org/wiki/Cu,Н.А.Фигуровский «Открытие элементов и происхождение их названий». Москва, Наука, 1970. (на сайте ХФ МГУ http://www.chem.msu.su/rus/history/element/Cu.html) |
Оксид меди и серебра поможет отыскать взрывчатку и наркотики — Наука
Ученым из из Института катализа имени Г. К. Борескова Сибирского отделения РАН совместно с Лабораторией рентгеновской дифрактометрии Новосибирского государственного университета удалось получить смешанный оксид меди и серебра. Свойства нового композита настолько специфичны, что обещают ему широкое применение в производстве самых разных продуктов — от пластиковых бутылок до взрывчатки. Об этом сообщает сайт Сибирского отделения РАН.
Одна из наиболее важных отраслей, где применяются смешанные оксиды, — это каталитическая химия. Разные металлы различным образом создают соединения, содержащие кислород (оксиды). Если в одном соединении кислород связан сразу двумя металлами, его свойства резко отличаются, от тех, что можно наблюдать в обычных оксидах металлов (той же ржавчине). Например, такой кислород может значительно активнее реагировать с внешними соединениями, то есть быть куда более эффективным катализатором, в том числе при низких температурах.
Например, такой кислород может значительно активнее реагировать с внешними соединениями, то есть быть куда более эффективным катализатором, в том числе при низких температурах.
Чем ниже температура того или иного массового технологического процесса, тем меньше затраты энергии на его поддержание. Например, на такой реакции, как окисление этилена, основано получение этиленгликоля, полиэтиленгликолей (из них делают антифризы, тормозные жидкости, моющие средства). Чем ниже температура и чем быстрее идут такие реакции, тем дешевле и конкурентоспособнее конечные продукты. А в их числе даже косметика, парфюмерия, ПЭТ-бутылки и ряд взрывчаток.
На первом этапе ученые изучили каталитические свойства обычного оксида CuO в его наноразмерном состоянии. Выяснилось, что в зависимости от размера «зерна» CuO каталитический эффект оксида меди заметно разнится. Крупные кристаллы хорошо окисляли только при температуре 150—200 градусов Цельсия, а наноразмерные частицы — уже при комнатной температуре. Более детальное исследование показало, что в наноразмерном оксиде меди соотношение атомов соответствовало формуле не CuO, а уже Cu4O3, благодаря чему кислород имел аномально высокую реакционную способность.
Более детальное исследование показало, что в наноразмерном оксиде меди соотношение атомов соответствовало формуле не CuO, а уже Cu4O3, благодаря чему кислород имел аномально высокую реакционную способность.
Далее химики ввели в оксид второй металл — серебро, заменив им одновалентную медь. Так был получен смешанный оксид серебра и меди Ag2Cu2O3. Его каталитические свойства оказались еще лучше, чем у медного, сравнимыми с современными катализаторами окислительного типа на базе палладия, платины или золота. Однако и серебро, и тем более медь намного дешевле этих благородных металлов.
Попутно выяснилось, что если нагревать Ag2Cu2O3, то выделяются наночастицы серебра размерами 5—15 нанометров. Причем происходило это только вдоль определенных направлений в кристалле. Из этого следует, что на основе таких двойных оксидов можно создавать ориентированные металл-оксидные наноструктуры и нанокомпозиты.
В теории нанокомпозит на основе смешанного оксида должен демонстрировать эффект гигантского комбинационного рассеяния света на адсорбированных молекулах. За счет этого спектральный сигнал может усиливаться в миллион и более раз. Данный эффект был бы весьма полезен при создании высокочувствительных аналитических методов поиска ничтожно малых концентраций разнообразных веществ — например, взрывчатки и наркотиков в аэропортах.
определите свойства вещества:Медь — Железо -Резина -Пластмасса — Золото — помогите,
На воздухе медь приобретает ярко желтоватый красный оттенок за счёт образования оксидной пленки тонкие же пластинки при просвечивании зеленовато голубого цвета. В чистом виде имеет достаточно мягкое тягучая и легко прокатывается и вытягивается. Высокую электропроводность меди можно назвать главным свойством определяющими и преимущественное использование. Также медь обладает очень высокой теплопроводностью. Медь обладает высоким значением плотности температура . Медь хорошо поддается обработке.
3резина можно рассматривать как сшитую коллоидную систему в которой каучук составляет дисперсионную среду наполнители дисперсную фазу. Важнейшие свойства резины высокая эластичность то есть способность к большим обратимым деформациям в широком интервале температур
4пластмасса не подвергаются коррозии они стойкие против действия растворов слабых кислот и щелочей А некоторые пластмассы например из полиэтилена полистирола стойки к воздействию даже концентрированных растворов кислот солей и щелочей Их используют при строительстве предприятий химической промышленности и канализационных сетей для изоляции емкости пластмассовые Как правильно являются плохими проводниками тепла . пластмасса хорошо окрашивается в любые цвета и долго сохраняет цвет. ценным свойством пластмасс является легкость их обработки возможность придания им разнообразной даже Самой сложной формы и различными способами
польза и вред. Как ухаживать за медной посудой.
Медная посуда: польза и вред. Как ухаживать за медной посудой. Многие кулинары-любители мечтают раскрыть секреты знаменитых поваров. Но бывает, что необыкновенный вкус приготовленного блюда зависит не столько от правильно подобранных составляющих и всевозможных специй, сколько от полезных качеств используемой посуды. На кухне дорогого ресторана, где работают профессионалы, и у опытной хозяйки всегда найдется медная посуда. Польза и вред, оказываемые ею на здоровье человека, обязательно должны учитываться перед приобретением этих предметов кухонной утвари. Достоинства медной посуды Наиболее важной характеристикой медной посуды следует считать ее высокую теплопроводность, которая в 10 раз выше, чем у стальной или алюминиевой емкости. Это способствует равномерному распределению тепла по всей поверхности, что значительно ускоряет процесс приготовления пищи, не снижая ее вкусовые качества. Считается, что особенно вкусное варенье или пикантный соус получаются, если готовятся именно в медной посуде. За счет снижения времени на термическую обработку пищи ее полезные вещества сохраняются. Легкий вес и долговечность также являются неоспоримыми достоинствами, которыми обладает медная посуда. Польза и вред, которые может принести медь здоровью человека, заслуживают отдельного внимания. Полезные свойства медной посуды На протяжении многих веков используется людьми медная посуда. Свойства, недостатки, и как ухаживать за кастрюлями и сковородками, выполненными из меди, — все это известно с давних пор. Одним из самых главных полезных свойств медной посуды следует назвать ее антибактериальное действие. Медь способна бороться с целым рядом грибков и бактерий, не допуская их попадания в пищу. В старину в медных емкостях хранили воду с целью ее обеззараживания. Американские ученые экспериментальным путем доказали, что медь успешно справляется со штаммами сальмонеллы, а также кишечной палочки. Пища, которая готовится в медной посуде, обеззараживается, предотвращая появление заболеваний желудочно-кишечного тракта. Недаром издавна медь применялась в народной медицине для лечения многих заболеваний: при интоксикации организма, судорогах, язвах, геморрое и т. д. Вред медной посуды Кроме положительных свойств, которыми обладает медь, ученые обнаружили и ряд отрицательных факторов, которые могут нанести вред здоровью или негативно повлиять на качество приготовляемых в такой посуде продуктов: Аскорбиновая кислота, которая содержится во фруктах и ягодах, под агрессивным воздействием меди разрушается. При хранении продуктов в медной посуде происходит потеря витаминов и окисление полиненасыщенных жирных кислот, что может способствовать возникновению онкозаболеваний. Вред посуды особенно серьезен, если она находится во влажной среде. Повышенная влажность вызывает окисление меди, это проявляется в виде зеленого налета. При взаимодействии с пищевыми кислотами во время нагревания вырабатываются особо вредные для организма вещества. Поэтому при появлении на посуде такого налета необходимо его тщательно удалить, протерев поверхность поваренной солью, смоченной в уксусе. Покрытие медной посуды С продуктами, обладающими повышенной кислотностью, медная посуда взаимодействует отрицательно. Для того чтобы предотвратить окисление и сделать приготовление пищи безопасным, изнутри медную емкость покрывают обычно специальными сплавами олова, железа или никеля. Когда такое покрытие протирается — посуду следует менять. При приготовлении пищи в медной посуде лучше всего пользоваться деревянной лопаточкой, чтобы не поцарапать внутреннюю поверхность. Уход за посудой из меди Медная посуда нуждается в более бережном уходе по сравнению с какой-либо другой. Ее необходимо периодически тщательно полировать, чтобы избежать налета, соблюдать условия хранения — такая посуда не терпит высокой влажности. Это для меди враг номер один. Не рекомендуется мыть медные предметы в посудомоечной машине, т. к. использование при этом сильных моющих средств может повредить их, значительно сократив срок службы. По этой же причине не стоит применять для чистки моющие средства, содержащие отбеливатель. Для мытья нужно использовать мягкую тряпочку или губку без абразивного слоя, чтобы не повредить защитный слой на внутренней поверхности.
В НИТУ «МИСиС» синтезировали препарат на основе наночастиц меди для длительной противовирусной обработки
Ученые кафедры физической химии НИТУ «МИСиС», основываясь на собственных многолетних исследованиях свойств наночастиц металлов, а также разработках американских и британских коллег, опубликованных в открытых источниках, синтезировали первую партию противовирусного препарата для обработки индивидуальных средств защиты и различных поверхностей на основе меди.
Препарат представляет собой спиртозоль — суспензию наночастиц меди размером от 1 до 3 нанометров в растворе антисептика цетилпиридиния хлорида в этиловом спирте. При дезинфекционной обработке при влажном воздухе медь на поверхности материала превращается в положительно заряженный ион гидроксида меди, что обеспечивает необходимую защиту обработанных предметов от вирусов и других патогенов.
О противовирусных и противомикробных свойствах меди человечеству известно несколько тысяч лет. Медь за счет перехода в водной среде в ионную форму значительно превосходит другие металлы по своим антибактериальным и противовирусным свойствам, в том числе серебро, которое широко известно этими характеристиками.
Современные исследования ученых доказывают — медь, действительно, активно уничтожает микробы и вирусы. В частности, ученые Саутгемптонского университета (Великобритания), проводившие изучение антивирусных свойств меди, констатируют, что частицы вируса — вирионы — буквально взрываются, попадая на медную поверхность.
По заказу Американской ассоциации производителей меди они провели серию исследований, которые продемонстрировали дезинфицирующие свойства меди и медных сплавов. Ученые экспериментировали и с родственником COVID-19 — коронавирусом 229E, открытым в 2015 году. В своих экспериментах профессор Билл Кивилл брал полированные медные пластины, обрабатывал их спиртом и ацетоном, затем наносил на поверхность патогены.
Пластины экспонировались в течение определенного времени — от нескольких минут до нескольких дней. После этого их исследовали двумя способами: одни помещали в емкость с водой и стеклянными бусинами, которые омывали их и соскребали с них образцы, другие изучали под микроскопом. Ни в одном из случаев следы вирусов и других патогенов обнаружены не были. Медь, действительно, самоочищалась.
«Это свойство объясняется тем, что медь очень легко переходит из атомарного состояния в ионное, — поясняет доцент кафедры физической химии НИТУ „МИСиС“ Георгий Фролов. — Положительно заряженные ионы гидроксида меди являются „мягким“ электрофильным реагентом, который вступает в химическое взаимодействие с серосодержащими структурами вируса, а также меняет рН-среды в кислую сторону. Таким образом разрушается оболочка любого микроорганизма, в том числе и вириона. Ионы гидроксида металла как бы „расстреливают“ вирус. Однако в высокой концентрации они опасны так же и для клеток организма, могут вызывать раздражение кожных покровов. Поэтому наиболее целесообразно использовать препараты на основе ионов меди и ее соединений в качестве сильного внешнего дезинфектора совместно с антисептиком цетилпиридиния хлоридом».
Основываясь на этих данных и многолетнем опыте работы с коллоидными растворами наночастиц металлов, Георгий Фролов совместно с коллегами синтезировал первую экспериментальную партию дезинфицирующего спиртозоля на основе нанодисперсных частиц меди и антисептика цетилпиридиния хлорида.
«Молекулы цетилпиридиния хлорида, четвертичные аммониевые ПАВ (поверхностно активные вещества) в составе спиртозоля, являясь сильнейшим электрофильным агентом, разрушают оболочку вируса и других патогенных микроорганизмов. Высокая поверхностная энергия частиц меди, приводит к высокой адгезии (слипанию) вирусов и их агрегации, — добавляет Фролов. — Наноформуляция, в которой находится медь, обеспечивает длительное воздействие на обработанных поверхностях даже после высыхания спиртовой основы».
Проведенные на базе лаборатории НИТУ «МИСиС» исследования продемонстрировали, что обработанные медным спиртозолем поверхности сохраняются защищенными более длительное время, чем обработанные обычными спиртами за счет действия наночастиц меди. Биоцидный эффект па поверхности материала зависит от концентрации наночастиц меди и попадающих вирусных частиц и патогенов, однако принципиальное отличие от обычных антисептиков очевидно.
В настоящее время препарат уже применяется в качестве дезинфектора в одной из московских стоматологических клиник.
Свойства меди
Чистая медь по электрической проводимости занимает следующее место после серебра, обладающего из всех известных проводников наивысшей проводимостью. Высокая проводимость и стойкость к атмосферной коррозии в сочетании с высокой пластичностью делают медь основным материалом для проводов.
На воздухе медные провода окисляются медленно, покрываясь тонким слоем окиси СuО, препятствующим дальнейшему окислению меди. Коррозию меди вызывают сернистый газ SО2, сероводород h3S, аммиак Nh4, окись азота NО, пары азотной кислоты и некоторые другие реактивы.
Проводниковую медь получают из слитков путем гальванической очистки ее в электролитических ваннах. Примеси, даже в ничтожных количествах, резко снижают электропроводность меди (рис. 8-1), делая ее малопригодной для проводников тока, поэтому в качестве электротехнической меди применяются лишь две ее марки (М0 и M1) по ГОСТ 859-66, химический состав которых приведен в табл. 8-1.
В табл. 8-1 не указана бескислородная медь марки М00 (99,99% Си), свободная от содержания кислорода и окислов меди, отличающаяся от меди марок М0 и M1 меньшим количеством примесей и существенно более высокой пластичностью, позволяющей ее волочение в тончайшие проволоки. По проводимости медь М00 не отличается от меди М0 и M1. Медь повышенной чистоты широко используется в электровакуумной технике.
Примеси Bi и Рb в больших количествах, чем указано в табл. 8-1, делают невозможным горячую прокатку меди. Сера не вызывает горячеломкость меди, но повышает ее хрупкость на холоде. Примеси в небольших количествах Ni, Ag, Zn и Sn не ухудшают технологических свойств, повышая механическую прочность и термическую стойкость меди.
Кислород как примесь в малых дозах, не затрудняя заметно прокатку, несколько повышает проводимость меди, так как находящиеся в меди другие примеси в результате окисления выводятся из твердого раствора, где они наиболее сильно влияют на снижение проводимости металла.
Повышенное содержание кислорода снижает проводимость и делает медь хрупкой в холодном состоянии, поэтому в электротехнических марках меди присутствие кислорода ограничивается (табл. 8-1). Медь, содержащая кислород, подвержена также водородной болезни. В восстановительной атмосфере закись меди восстанавливается до металла. Во время реакций, идущих с образованием водяных паров, в меди появляются микротрещины.
Медный провод | AMERICAN ELEMENTS ®
РАЗДЕЛ 1. ИДЕНТИФИКАЦИЯ
Название продукта: Copper Wire
Номер продукта: Все применимые коды продуктов American Elements, например CU-M-02-W , CU-M-03-W , CU-M-04-W , CU-M-05-W , CU-M-06-W
Номер CAS: 7440-50-8
Соответствующие установленные области применения вещества: Научные исследования и разработки
Информация о поставщике:
American Elements
10884 Weyburn Ave.
Лос-Анджелес, Калифорния
Тел .: +1 310-208-0551
Факс: +1 310-208-0351
Телефон экстренной связи:
Внутренний номер, Северная Америка: +1 800-424-9300
Международный: +1 703-527-3887
РАЗДЕЛ 2. ИДЕНТИФИКАЦИЯ ОПАСНОСТИ
Классификация вещества или смеси
Классификация в соответствии с Регламентом (ЕС) № 1272/2008
Вещество не классифицируется как опасное для здоровья или окружающей среды в соответствии с правила CLP.
Классификация в соответствии с Директивой 67/548 / EEC или Директивой 1999/45 / EC
N / A
Информация об особых опасностях для человека и окружающей среды:
Нет данных
Опасности, не классифицируемые иным образом
Нет данных
Элементы маркировки
Маркировка в соответствии с в соответствии с Регламентом (ЕС) № 1272/2008
Н / Д
Пиктограммы опасностей
Н / Д
Сигнальное слово
Н / Д
Краткая характеристика опасности
Н / Д
Классификация WHMIS
Не контролируется
Система классификации
Рейтинги HMIS (шкала 0- 4)
(Система идентификации опасных материалов)
Здоровье (острые эффекты) = 0
Воспламеняемость = 0
Физическая опасность = 0
Другие опасности
Результаты оценки PBT и vPvB
PBT: Нет данных
vPvB: Нет
РАЗДЕЛ 3.СОСТАВ / ИНФОРМАЦИЯ ОБ ИНГРЕДИЕНТАХ
Вещества
Номер CAS / Название вещества:
7440-50-8 Медь
Идентификационный номер (а):
Номер ЕС: 231-159-6
РАЗДЕЛ 4. ПЕРВАЯ ПОМОЩЬ
Описание мер первой помощи
Общие сведения
Никаких специальных мер не требуется.
При вдыхании:
В случае жалоб обратиться за медицинской помощью.
При попадании на кожу:
Обычно продукт не раздражает кожу.
При попадании в глаза:
Промыть открытый глаз под проточной водой в течение нескольких минут.Если симптомы не исчезнут, обратитесь к врачу.
При проглатывании:
Если симптомы не исчезнут, обратиться к врачу.
Информация для врача
Наиболее важные симптомы и воздействия, как острые, так и замедленные
Данные отсутствуют
Указание на необходимость немедленной медицинской помощи и специального лечения
Нет данных
РАЗДЕЛ 5. МЕРЫ ПОЖАРОТУШЕНИЯ
Средства пожаротушения
Подходящие средства пожаротушения
Специальный порошок для металлических огней. Не используйте воду.
Средства пожаротушения непригодны из соображений безопасности
Вода
Особые опасности, исходящие от вещества или смеси
При пожаре могут образоваться следующие вещества:
Оксиды меди
Рекомендации для пожарных
Защитное снаряжение:
Никаких специальных мер не требуется .
РАЗДЕЛ 6. МЕРЫ ПРИ СЛУЧАЙНОМ ВЫБРОСЕ
Меры личной безопасности, защитное снаряжение и порядок действий в чрезвычайной ситуации
Не требуется.
Меры по защите окружающей среды:
Не допускайте попадания материала в окружающую среду без официального разрешения.
Не допускать попадания продукта в канализацию, канализацию или другие водоемы.
Не допускайте попадания материала в землю или почву.
Методы и материалы для локализации и очистки:
Подобрать механически.
Предотвращение вторичных опасностей:
Никаких специальных мер не требуется.
Ссылка на другие разделы.
См. Раздел 7 для получения информации о безопасном обращении.
См. Раздел 8 для получения информации о средствах индивидуальной защиты.
См. Раздел 13 для получения информации об утилизации.
РАЗДЕЛ 7. ОБРАЩЕНИЕ И ХРАНЕНИЕ
Обращение
Меры предосторожности для безопасного обращения
Хранить контейнер плотно закрытым.
Хранить в сухом прохладном месте в плотно закрытой таре.
Информация о защите от взрывов и пожаров:
Никаких специальных мер не требуется.
Условия безопасного хранения с учетом несовместимости
Требования, предъявляемые к складским помещениям и таре:
Особых требований нет.
Информация о хранении в одном общем хранилище:
Нет данных
Дополнительная информация об условиях хранения:
Хранить тару плотно закрытой.
Хранить в прохладном, сухом месте в хорошо закрытой таре.
Особое конечное использование
Нет данных
РАЗДЕЛ 8. КОНТРОЛЬ ВОЗДЕЙСТВИЯ / ЛИЧНАЯ ЗАЩИТА
Дополнительная информация о конструкции технических систем:
Нет дополнительных данных; см. раздел 7.
Параметры контроля
Компоненты с предельными значениями, требующие контроля на рабочем месте: 7440-50-8 Медь (100,0%)
PEL (США) Долгосрочное значение: 1 * 0,1 ** мг / м 3 как Cu * пыль и туман ** дым
REL (США) Долгосрочное значение: 1 * 0.1 ** мг / м 3 как Cu * пыль и туман ** дым
TLV (США) Долгосрочное значение: 1 * 0,2 ** мг / м 3 * пыль и туман; ** дым; как Cu
EL (Канада) Долгосрочное значение: 1 * 0,2 ** мг / м 3 * пыль и туман; ** дым
EV (Канада) Долгосрочное значение: 0,2 * 1 ** мг / м 3 как медь, * дым; ** пыль и туман
Дополнительная информация: Нет данных
Контроль воздействия
Средства индивидуальной защиты
Следуйте типичные защитные и гигиенические методы работы с химическими веществами.
Поддерживайте эргономичную рабочую среду.
Дыхательное оборудование: Не требуется.
Защита рук: Не требуется.
Время проницаемости материала перчаток (в минутах)
Нет данных
Защита глаз: Защитные очки
Защита тела: Защитная рабочая одежда.
РАЗДЕЛ 9. ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА
Информация об основных физических и химических свойствах
Внешний вид:
Форма: Твердое вещество в различных формах
Цвет: Медного цвета
Запах: Без запаха
Порог запаха: Нет данных.
pH: нет данных
Точка плавления / интервал плавления: 1083 ° C (1981 ° F)
Точка кипения / интервал кипения: 2562 ° C (4644 ° F)
Температура сублимации / начало: данные отсутствуют
Воспламеняемость (твердое, газ): Нет данных.
Температура возгорания: данные отсутствуют
Температура разложения: данные отсутствуют
Самовоспламенение: данные отсутствуют.
Взрывоопасность: данные отсутствуют.
Пределы взрываемости:
Нижний: данные отсутствуют
Верхние: данные отсутствуют
Давление пара при 20 ° C (68 ° F): 0 гПа
Плотность при 20 ° C (68 ° F): 8.94 г / см 3 (74,604 фунта / галлон)
Относительная плотность: данные отсутствуют.
Плотность пара: Нет данных
Скорость испарения: Нет данных
Растворимость в воде (H 2 O): Нерастворимый
Коэффициент распределения (н-октанол / вода): данные отсутствуют.
Вязкость:
Динамическая: Нет данных
Кинематическая: Нет
Другая информация
Нет данных
РАЗДЕЛ 10. СТАБИЛЬНОСТЬ И РЕАКЦИОННАЯ СПОСОБНОСТЬ
Реакционная способность
Нет данных
Химическая стабильность
Стабилен при рекомендуемых условиях хранения
Термическое разложение / условия, которых следует избегать:
При использовании и хранении в соответствии со спецификациями разложения не происходит.
Возможность опасных реакций
Нет известных опасных реакций
Условия, которых следует избегать
Данные отсутствуют
Несовместимые материалы:
Данные отсутствуют
Опасные продукты разложения:
Оксиды меди
РАЗДЕЛ 11. ТОКСИКОЛОГИЧЕСКАЯ ИНФОРМАЦИЯ
Информация о токсикологическом воздействии
Острый токсичность:
Реестр токсического действия химических веществ (RTECS) содержит данные об острой токсичности этого вещества.
Значения LD / LC50, относящиеся к классификации:
LD50 при пероральном приеме> 5000 мг / кг (мышь)
Раздражение или разъедание кожи: Без раздражающего действия.
Раздражение или разъедание глаз: Без раздражающего действия.
Сенсибилизация: Сенсибилизирующие эффекты неизвестны.
Мутагенность зародышевых клеток: Эффекты неизвестны.
Канцерогенность:
EPA-D: Канцерогенность для человека не классифицируется: неадекватные доказательства канцерогенности для человека и животных или данные отсутствуют.
Реестр токсических эффектов химических веществ (RTECS) содержит данные о онкогенных, канцерогенных и / или опухолевых заболеваниях для этого вещества.
Репродуктивная токсичность:
Реестр токсических эффектов химических веществ (RTECS) содержит репродуктивные данные для этого вещества.
Специфическая системная токсичность, поражающая отдельные органы-мишени — многократное воздействие: Эффекты неизвестны.
Специфическая системная токсичность, поражающая отдельные органы-мишени — однократное воздействие: Эффекты неизвестны.
Опасность при вдыхании: Эффекты неизвестны.
От подострой до хронической токсичности: Эффекты неизвестны.
Дополнительная токсикологическая информация:
Насколько нам известно, острая и хроническая токсичность этого вещества полностью не изучена.
Канцерогенные категории
OSHA-Ca (Управление по охране труда)
Вещество не перечислено.
РАЗДЕЛ 12. ЭКОЛОГИЧЕСКАЯ ИНФОРМАЦИЯ
Токсичность
Водная токсичность:
Нет данных
Стойкость и разлагаемость
Нет данных
Потенциал биоаккумуляции
Нет данных
Мобильность в почве
Нет данных
Дополнительная экологическая информация:
Нет допускать попадание материала в окружающую среду без официальных разрешений.
Не допускайте попадания неразбавленного продукта или больших количеств в грунтовые воды, водоемы или канализацию.
Избегать попадания в окружающую среду.
Результаты оценки PBT и vPvB
PBT: N / A
vPvB: N / A
Другие побочные эффекты
Нет данных
РАЗДЕЛ 13. УТИЛИЗАЦИЯ
Методы обработки отходов
Рекомендация
Для обеспечения надлежащей утилизации см. Официальные правила .
Неочищенная тара:
Рекомендация:
Утилизация должна производиться в соответствии с официальными предписаниями.
РАЗДЕЛ 14. ИНФОРМАЦИЯ ПО ТРАНСПОРТИРОВКЕ
Номер ООН
DOT, ADN, IMDG, IATA
НЕТ
Собственное транспортное наименование ООН
DOT, ADN, IMDG, IATA
НЕТ
Класс (ы) опасности при транспортировке
DOT, ADR, ADN, IMDG, IATA
Class
N / A
Группа упаковки
DOT, IMDG, IATA
N / A
Экологические опасности:
Морской загрязнитель (IMDG):
Да (PP)
Да (P)
Особые меры предосторожности для пользователя
Н / Д
Транспортировка навалом в соответствии с Приложением II MARPOL73 / 78 и Кодексом IBC
Н / Д
Транспортировка / Дополнительная информация:
DOT
Морской загрязнитель (DOT):
№
РАЗДЕЛ 15 .НОРМАТИВНАЯ ИНФОРМАЦИЯ
Нормативы / законодательные акты по безопасности, охране здоровья и окружающей среды, относящиеся к веществу или смеси
Национальные правила
Все компоненты этого продукта перечислены в Реестре химических веществ Закона о контроле за токсичными веществами Агентства по охране окружающей среды США.
Все компоненты этого продукта занесены в Канадский список веществ, предназначенных для домашнего использования (DSL).
SARA Раздел 313 (списки конкретных токсичных химикатов)
7440-50-8 Медь
Предложение штата Калифорния 65
Предложение 65 — Химические вещества, вызывающие рак
Вещество не указано в списке.
Prop 65 — Токсичность для развития
Вещество не указано.
Предложение 65 — Токсичность для развития, женщины
Вещество не указано.
Предложение 65 — Токсичность для развития, мужчины
Вещество не указано.
Информация об ограничении использования:
Для использования только технически квалифицированными специалистами.
Другие постановления, ограничения и запретительные постановления
Вещество, вызывающее особую озабоченность (SVHC) в соответствии с Регламентом REACH (EC) № 1907/2006.
Вещества нет в списке.
Необходимо соблюдать условия ограничений согласно Статье 67 и Приложению XVII Регламента (ЕС) № 1907/2006 (REACH) для производства, размещения на рынке и использования.
Вещества нет в списке.
Приложение XIV Правил REACH (требуется разрешение на использование)
Вещество не указано.
REACH — Предварительно зарегистрированные вещества
Вещество внесено в список.
Оценка химической безопасности:
Оценка химической безопасности не проводилась
РАЗДЕЛ 16.ПРОЧАЯ ИНФОРМАЦИЯ
Паспорт безопасности в соответствии с Регламентом (ЕС) № 1907/2006 (REACH). Вышеприведенная информация считается правильной, но не претендует на исчерпывающий характер и должна использоваться только в качестве руководства. Информация в этом документе основана на текущем уровне наших знаний и применима к продукту с учетом соответствующих мер безопасности. Это не является гарантией свойств продукта. American Elements не несет ответственности за любой ущерб, возникший в результате обращения или контакта с вышеуказанным продуктом.Дополнительные условия продажи см. На обратной стороне счета-фактуры или упаковочного листа. АВТОРСКИЕ ПРАВА 1997-2021 AMERICAN ELEMENTS. ЛИЦЕНЗИОННЫМ ДАННЫМ РАЗРЕШЕНО ИЗГОТОВЛЕНИЕ НЕОГРАНИЧЕННЫХ КОПИИ БУМАГИ ТОЛЬКО ДЛЯ ВНУТРЕННЕГО ИСПОЛЬЗОВАНИЯ.
Медная фольга | AMERICAN ELEMENTS ®
РАЗДЕЛ 1. ИДЕНТИФИКАЦИЯ
Название продукта: Copper Foil
Номер продукта: Все применимые коды продуктов American Elements, например CU-M-02-F , CU-M-025-F , CU-M-03-F , CU-M-035-F , CU-M-04-F , CU-M-05-F , CU-M-06-F
Номер CAS: 7440-50-8
Соответствующие установленные области применения вещества: Научные исследования и разработки
Информация о поставщике:
American Elements
10884 Weyburn Ave.
Лос-Анджелес, Калифорния
Тел .: +1 310-208-0551
Факс: +1 310-208-0351
Телефон экстренной связи:
Внутренний номер, Северная Америка: +1 800-424-9300
Международный: +1 703-527-3887
РАЗДЕЛ 2. ИДЕНТИФИКАЦИЯ ОПАСНОСТИ
Классификация вещества или смеси
Классификация в соответствии с Регламентом (ЕС) № 1272/2008
Вещество не классифицируется как опасное для здоровья или окружающей среды в соответствии с правила CLP.
Классификация в соответствии с Директивой 67/548 / EEC или Директивой 1999/45 / EC
N / A
Информация об особых опасностях для человека и окружающей среды:
Нет данных
Опасности, не классифицируемые иным образом
Нет данных
Элементы маркировки
Маркировка в соответствии с в соответствии с Регламентом (ЕС) № 1272/2008
Н / Д
Пиктограммы опасностей
Н / Д
Сигнальное слово
Н / Д
Краткая характеристика опасности
Н / Д
Классификация WHMIS
Не контролируется
Система классификации
Рейтинги HMIS (шкала 0- 4)
(Система идентификации опасных материалов)
Здоровье (острые эффекты) = 0
Воспламеняемость = 0
Физическая опасность = 0
Другие опасности
Результаты оценки PBT и vPvB
PBT: Нет данных
vPvB: Нет
РАЗДЕЛ 3.СОСТАВ / ИНФОРМАЦИЯ ОБ ИНГРЕДИЕНТАХ
Вещества
Номер CAS / Название вещества:
7440-50-8 Медь
Идентификационный номер (а):
Номер ЕС: 231-159-6
РАЗДЕЛ 4. ПЕРВАЯ ПОМОЩЬ
Описание мер первой помощи
Общие сведения
Никаких специальных мер не требуется.
При вдыхании:
В случае жалоб обратиться за медицинской помощью.
При попадании на кожу:
Обычно продукт не раздражает кожу.
При попадании в глаза:
Промыть открытый глаз под проточной водой в течение нескольких минут.Если симптомы не исчезнут, обратитесь к врачу.
При проглатывании:
Если симптомы не исчезнут, обратиться к врачу.
Информация для врача
Наиболее важные симптомы и воздействия, как острые, так и замедленные
Данные отсутствуют
Указание на необходимость немедленной медицинской помощи и специального лечения
Нет данных
РАЗДЕЛ 5. МЕРЫ ПОЖАРОТУШЕНИЯ
Средства пожаротушения
Подходящие средства пожаротушения
Специальный порошок для металлических огней. Не используйте воду.
Средства пожаротушения непригодны из соображений безопасности
Вода
Особые опасности, исходящие от вещества или смеси
При пожаре могут образоваться следующие вещества:
Оксиды меди
Рекомендации для пожарных
Защитное снаряжение:
Никаких специальных мер не требуется .
РАЗДЕЛ 6. МЕРЫ ПРИ СЛУЧАЙНОМ ВЫБРОСЕ
Меры личной безопасности, защитное снаряжение и порядок действий в чрезвычайной ситуации
Не требуется.
Меры по защите окружающей среды:
Не допускайте попадания материала в окружающую среду без официального разрешения.
Не допускать попадания продукта в канализацию, канализацию или другие водоемы.
Не допускайте попадания материала в землю или почву.
Методы и материалы для локализации и очистки:
Подобрать механически.
Предотвращение вторичных опасностей:
Никаких специальных мер не требуется.
Ссылка на другие разделы.
См. Раздел 7 для получения информации о безопасном обращении.
См. Раздел 8 для получения информации о средствах индивидуальной защиты.
См. Раздел 13 для получения информации об утилизации.
РАЗДЕЛ 7. ОБРАЩЕНИЕ И ХРАНЕНИЕ
Обращение
Меры предосторожности для безопасного обращения
Хранить контейнер плотно закрытым.
Хранить в сухом прохладном месте в плотно закрытой таре.
Информация о защите от взрывов и пожаров:
Никаких специальных мер не требуется.
Условия безопасного хранения с учетом несовместимости
Требования, предъявляемые к складским помещениям и таре:
Особых требований нет.
Информация о хранении в одном общем хранилище:
Нет данных
Дополнительная информация об условиях хранения:
Хранить тару плотно закрытой.
Хранить в прохладном, сухом месте в хорошо закрытой таре.
Особое конечное использование
Нет данных
РАЗДЕЛ 8. КОНТРОЛЬ ВОЗДЕЙСТВИЯ / ЛИЧНАЯ ЗАЩИТА
Дополнительная информация о конструкции технических систем:
Нет дополнительных данных; см. раздел 7.
Параметры контроля
Компоненты с предельными значениями, требующие контроля на рабочем месте: 7440-50-8 Медь (100,0%)
PEL (США) Долгосрочное значение: 1 * 0,1 ** мг / м 3 как Cu * пыль и туман ** дым
REL (США) Долгосрочное значение: 1 * 0.1 ** мг / м 3 как Cu * пыль и туман ** дым
TLV (США) Долгосрочное значение: 1 * 0,2 ** мг / м 3 * пыль и туман; ** дым; как Cu
EL (Канада) Долгосрочное значение: 1 * 0,2 ** мг / м 3 * пыль и туман; ** дым
EV (Канада) Долгосрочное значение: 0,2 * 1 ** мг / м 3 как медь, * дым; ** пыль и туман
Дополнительная информация: Нет данных
Контроль воздействия
Средства индивидуальной защиты
Следуйте типичные защитные и гигиенические методы работы с химическими веществами.
Поддерживайте эргономичную рабочую среду.
Дыхательное оборудование: Не требуется.
Защита рук: Не требуется.
Время проницаемости материала перчаток (в минутах)
Нет данных
Защита глаз: Защитные очки
Защита тела: Защитная рабочая одежда.
РАЗДЕЛ 9. ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА
Информация об основных физических и химических свойствах
Внешний вид:
Форма: Твердое вещество в различных формах
Цвет: Медного цвета
Запах: Без запаха
Порог запаха: Нет данных.
pH: нет данных
Точка плавления / интервал плавления: 1083 ° C (1981 ° F)
Точка кипения / интервал кипения: 2562 ° C (4644 ° F)
Температура сублимации / начало: данные отсутствуют
Воспламеняемость (твердое, газ): Нет данных.
Температура возгорания: данные отсутствуют
Температура разложения: данные отсутствуют
Самовоспламенение: данные отсутствуют.
Взрывоопасность: данные отсутствуют.
Пределы взрываемости:
Нижний: данные отсутствуют
Верхние: данные отсутствуют
Давление пара при 20 ° C (68 ° F): 0 гПа
Плотность при 20 ° C (68 ° F): 8.94 г / см 3 (74,604 фунта / галлон)
Относительная плотность: данные отсутствуют.
Плотность пара: Нет данных
Скорость испарения: Нет данных
Растворимость в воде (H 2 O): Нерастворимый
Коэффициент распределения (н-октанол / вода): данные отсутствуют.
Вязкость:
Динамическая: Нет данных
Кинематическая: Нет
Другая информация
Нет данных
РАЗДЕЛ 10. СТАБИЛЬНОСТЬ И РЕАКЦИОННАЯ СПОСОБНОСТЬ
Реакционная способность
Нет данных
Химическая стабильность
Стабилен при рекомендуемых условиях хранения
Термическое разложение / условия, которых следует избегать:
При использовании и хранении в соответствии со спецификациями разложения не происходит.
Возможность опасных реакций
Нет известных опасных реакций
Условия, которых следует избегать
Данные отсутствуют
Несовместимые материалы:
Данные отсутствуют
Опасные продукты разложения:
Оксиды меди
РАЗДЕЛ 11. ТОКСИКОЛОГИЧЕСКАЯ ИНФОРМАЦИЯ
Информация о токсикологическом воздействии
Острый токсичность:
Реестр токсического действия химических веществ (RTECS) содержит данные об острой токсичности этого вещества.
Значения LD / LC50, относящиеся к классификации:
LD50 при пероральном приеме> 5000 мг / кг (мышь)
Раздражение или разъедание кожи: Без раздражающего действия.
Раздражение или разъедание глаз: Без раздражающего действия.
Сенсибилизация: Сенсибилизирующие эффекты неизвестны.
Мутагенность зародышевых клеток: Эффекты неизвестны.
Канцерогенность:
EPA-D: Канцерогенность для человека не классифицируется: неадекватные доказательства канцерогенности для человека и животных или данные отсутствуют.
Реестр токсических эффектов химических веществ (RTECS) содержит данные о онкогенных, канцерогенных и / или опухолевых заболеваниях для этого вещества.
Репродуктивная токсичность:
Реестр токсических эффектов химических веществ (RTECS) содержит репродуктивные данные для этого вещества.
Специфическая системная токсичность, поражающая отдельные органы-мишени — многократное воздействие: Эффекты неизвестны.
Специфическая системная токсичность, поражающая отдельные органы-мишени — однократное воздействие: Эффекты неизвестны.
Опасность при вдыхании: Эффекты неизвестны.
От подострой до хронической токсичности: Эффекты неизвестны.
Дополнительная токсикологическая информация:
Насколько нам известно, острая и хроническая токсичность этого вещества полностью не изучена.
Канцерогенные категории
OSHA-Ca (Управление по охране труда)
Вещество не перечислено.
РАЗДЕЛ 12. ЭКОЛОГИЧЕСКАЯ ИНФОРМАЦИЯ
Токсичность
Водная токсичность:
Нет данных
Стойкость и разлагаемость
Нет данных
Потенциал биоаккумуляции
Нет данных
Мобильность в почве
Нет данных
Дополнительная экологическая информация:
Нет допускать попадание материала в окружающую среду без официальных разрешений.
Не допускайте попадания неразбавленного продукта или больших количеств в грунтовые воды, водоемы или канализацию.
Избегать попадания в окружающую среду.
Результаты оценки PBT и vPvB
PBT: N / A
vPvB: N / A
Другие побочные эффекты
Нет данных
РАЗДЕЛ 13. УТИЛИЗАЦИЯ
Методы обработки отходов
Рекомендация
Для обеспечения надлежащей утилизации см. Официальные правила .
Неочищенная тара:
Рекомендация:
Утилизация должна производиться в соответствии с официальными предписаниями.
РАЗДЕЛ 14. ИНФОРМАЦИЯ ПО ТРАНСПОРТИРОВКЕ
Номер ООН
DOT, ADN, IMDG, IATA
НЕТ
Собственное транспортное наименование ООН
DOT, ADN, IMDG, IATA
НЕТ
Класс (ы) опасности при транспортировке
DOT, ADR, ADN, IMDG, IATA
Class
N / A
Группа упаковки
DOT, IMDG, IATA
N / A
Экологические опасности:
Морской загрязнитель (IMDG):
Да (PP)
Да (P)
Особые меры предосторожности для пользователя
Н / Д
Транспортировка навалом в соответствии с Приложением II MARPOL73 / 78 и Кодексом IBC
Н / Д
Транспортировка / Дополнительная информация:
DOT
Морской загрязнитель (DOT):
№
РАЗДЕЛ 15 .НОРМАТИВНАЯ ИНФОРМАЦИЯ
Нормативы / законодательные акты по безопасности, охране здоровья и окружающей среды, относящиеся к веществу или смеси
Национальные правила
Все компоненты этого продукта перечислены в Реестре химических веществ Закона о контроле за токсичными веществами Агентства по охране окружающей среды США.
Все компоненты этого продукта занесены в Канадский список веществ, предназначенных для домашнего использования (DSL).
SARA Раздел 313 (списки конкретных токсичных химикатов)
7440-50-8 Медь
Предложение штата Калифорния 65
Предложение 65 — Химические вещества, вызывающие рак
Вещество не указано в списке.
Prop 65 — Токсичность для развития
Вещество не указано.
Предложение 65 — Токсичность для развития, женщины
Вещество не указано.
Предложение 65 — Токсичность для развития, мужчины
Вещество не указано.
Информация об ограничении использования:
Для использования только технически квалифицированными специалистами.
Другие постановления, ограничения и запретительные постановления
Вещество, вызывающее особую озабоченность (SVHC) в соответствии с Регламентом REACH (EC) № 1907/2006.
Вещества нет в списке.
Необходимо соблюдать условия ограничений согласно Статье 67 и Приложению XVII Регламента (ЕС) № 1907/2006 (REACH) для производства, размещения на рынке и использования.
Вещества нет в списке.
Приложение XIV Правил REACH (требуется разрешение на использование)
Вещество не указано.
REACH — Предварительно зарегистрированные вещества
Вещество внесено в список.
Оценка химической безопасности:
Оценка химической безопасности не проводилась
РАЗДЕЛ 16.ПРОЧАЯ ИНФОРМАЦИЯ
Паспорт безопасности в соответствии с Регламентом (ЕС) № 1907/2006 (REACH). Вышеприведенная информация считается правильной, но не претендует на исчерпывающий характер и должна использоваться только в качестве руководства. Информация в этом документе основана на текущем уровне наших знаний и применима к продукту с учетом соответствующих мер безопасности. Это не является гарантией свойств продукта. American Elements не несет ответственности за любой ущерб, возникший в результате обращения или контакта с вышеуказанным продуктом.Дополнительные условия продажи см. На обратной стороне счета-фактуры или упаковочного листа. АВТОРСКИЕ ПРАВА 1997-2021 AMERICAN ELEMENTS. ЛИЦЕНЗИОННЫМ ДАННЫМ РАЗРЕШЕНО ИЗГОТОВЛЕНИЕ НЕОГРАНИЧЕННЫХ КОПИИ БУМАГИ ТОЛЬКО ДЛЯ ВНУТРЕННЕГО ИСПОЛЬЗОВАНИЯ.
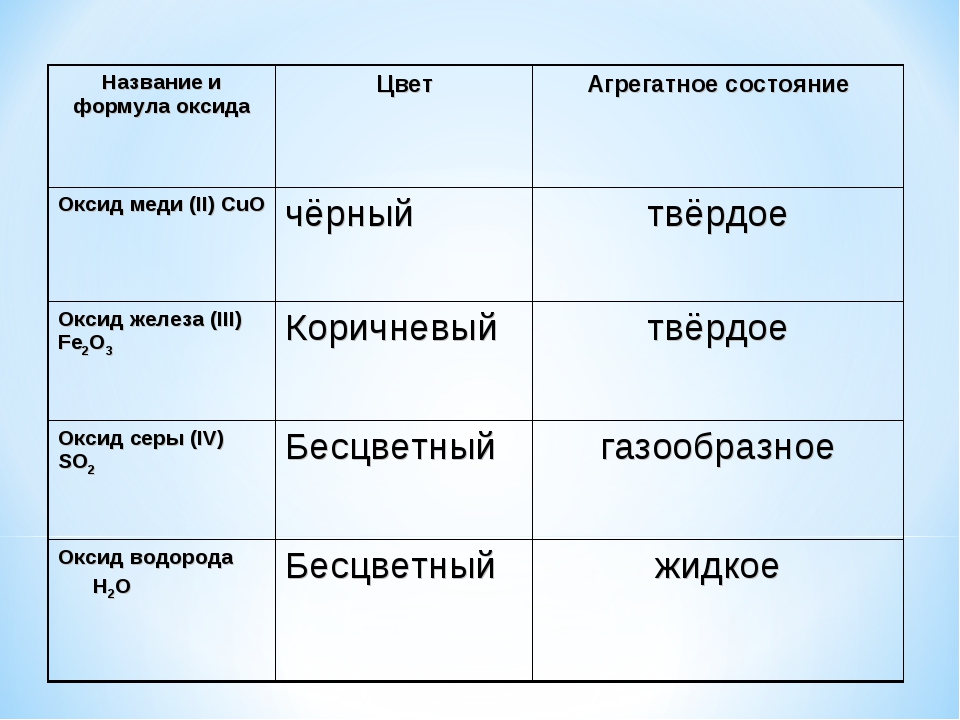
3.5: Различия в физических и химических свойствах веществ
Цели обучения
Для отделения физических свойств от химических.
Все вещества обладают физическими и химическими свойствами. Физические свойства — это характеристики, которые ученые могут измерить без изменения состава исследуемого образца, такие как масса, цвет и объем (объем пространства, занимаемого образцом).Химические свойства описывают характерную способность вещества реагировать с образованием новых веществ; они включают его воспламеняемость и подверженность коррозии. Все образцы чистого вещества имеют одинаковые химические и физические свойства. Например, чистая медь всегда представляет собой красновато-коричневое твердое вещество (физическое свойство) и всегда растворяется в разбавленной азотной кислоте с образованием синего раствора и коричневого газа (химическое свойство).
Физическая собственность
A физическое свойство — это характеристика вещества, которую можно наблюдать или измерять без изменения идентичности вещества.Серебро — блестящий металл, который очень хорошо проводит электричество. Его можно формовать в тонкие листы, это свойство называется пластичностью. Соль тусклая и хрупкая, она проводит электричество, когда растворяется в воде, что довольно легко. Физические свойства вещества включают цвет, твердость, пластичность, растворимость, электропроводность, плотность, точки плавления и кипения.
Цвет элементов не сильно меняется от одного элемента к другому. Подавляющее большинство элементов бесцветны, серебристые или серые.У некоторых элементов действительно есть отличительные цвета: сера и хлор желтые, медь (конечно) медный цвет, а элементарный бром красный. Однако плотность может быть очень полезным параметром для идентификации элемента. Из материалов, которые существуют в твердом виде при комнатной температуре, йод имеет очень низкую плотность по сравнению с цинком, хромом и оловом. Золото имеет очень высокую плотность, как и платина. Например, чистая вода имеет плотность 0,998 г / см 3 при 25 ° C. Средние плотности некоторых распространенных веществ указаны в Таблице \ (\ PageIndex {1} \).Обратите внимание, что у кукурузного масла отношение массы к объему ниже, чем у воды. Это означает, что при добавлении в воду кукурузное масло будет «плавать».
| Вещество | Плотность при 25 ° C (г / см3) |
|---|---|
| кровь | 1.035 |
| телесный жир | 0,918 |
| цельное молоко | 1.030 |
| кукурузное масло | 0,922 |
| майонез | 0,910 |
| мед | 1,420 |
Твердость помогает определить, как можно использовать элемент (особенно металл). Многие элементы довольно мягкие (например, серебро и золото), в то время как другие (например, титан, вольфрам и хром) намного тверже. Углерод — интересный пример твердости.В графите («грифель» в карандашах) углерод очень мягкий, в то время как углерод в алмазе примерно в семь раз тверже.
Рисунок \ (\ PageIndex {1} \): карандаш (слева) и бриллиантовое кольцо (справа). Оба являются формой углерода, но обладают очень разными физическими свойствами.Точки плавления и кипения — это своего рода уникальные идентификаторы, особенно соединений. Помимо предоставления некоторого представления об идентичности соединения, может быть получена важная информация о чистоте материала.
Химические свойства
Химические свойства вещества описывают его способность претерпевать некоторые химические изменения или реакции в силу своего состава. Присутствующие элементы, электроны и связи придают материи потенциал для химических изменений. Довольно сложно определить химическое свойство без слова «изменение». В конце концов, изучив химию в течение некоторого времени, вы сможете взглянуть на формулу соединения и указать некоторые химические свойства.Например, водород может воспламениться и взорваться при правильных условиях — это химическое свойство. Металлы в целом обладают химическим свойством реагировать с кислотой. Цинк реагирует с соляной кислотой с образованием газообразного водорода — это химическое свойство.
Рисунок \ (\ PageIndex {2} \): сильная ржавчина на звеньях цепи возле моста Золотые Ворота в Сан-Франциско; он постоянно подвергался воздействию влаги и солевых брызг, что приводило к разрушению поверхности, растрескиванию и отслаиванию металла.(CC BY-SA 3.0; Марлит).Химическое свойство железа — это его способность соединяться с кислородом с образованием оксида железа, химического названия ржавчины (Рисунок \ (\ PageIndex {2} \)). Более общий термин для обозначения ржавчины и других подобных процессов — коррозия. Другие термины, которые обычно используются при описании химических изменений, — это горение, гниение, взрыв, разложение и брожение. Химические свойства очень полезны для идентификации веществ. Однако, в отличие от физических свойств, химические свойства можно наблюдать только тогда, когда вещество находится в процессе преобразования в другое вещество.
| Физическая собственность | Химическая собственность |
|---|---|
| Металлический галлий плавится при температуре 30 o C. | Железо металлическое ржавчина. |
| Ртуть — очень плотная жидкость. | Зеленый банан при созревании становится желтым. |
| Золото блестит. | Горит сухой кусок бумаги. |
Пример \ (\ PageIndex {1} \)
Что из перечисленного является химическим свойством железа?
- Железо корродирует во влажном воздухе
- Плотность = 7,874 г / см 3
- В чистом виде железо мягкое.
- Железо плавится при 1808 К.
Решение
«Железо разъедает во влажном воздухе» — единственное химическое свойство железа из списка.
Упражнение \ (\ PageIndex {1A} \)
Что из перечисленного является физическим свойством материи?
- коррозионная активность
- pH (кислотность)
- плотность
- воспламеняемость
- Ответ
- c
Упражнение \ (\ PageIndex {1B} \)
Что из перечисленного является химическим свойством?
- воспламеняемость
- точка плавления
- точка кипения
- плотность
- Ответ
- a
Резюме
Физическое свойство — это характеристика вещества, которую можно наблюдать или измерять без изменения идентичности вещества.Физические свойства включают цвет, плотность, твердость, а также точки плавления и кипения. Химическое свойство описывает способность вещества претерпевать определенные химические изменения. Чтобы определить химическое свойство, мы ищем химическое изменение. Химическое изменение всегда производит один или несколько типов материи, которые отличаются от материи, существовавшей до изменения. Образование ржавчины — это химическое изменение, потому что ржавчина — это другой тип вещества, чем железо, кислород и вода, присутствовавшие до образования ржавчины.
Материалы и авторство
Эта страница была создана на основе содержимого следующими участниками и отредактирована (тематически или всесторонне) командой разработчиков LibreTexts в соответствии со стилем, представлением и качеством платформы:
Reade Advanced Materials — медь (Cu), металл и медный порошок
Физические свойства
Порошок, нанопорошок, дробь, стружка, пуля, монокристалл, фольга, диски, мишени для распыления, пластина, сетка, проволока, стержень и трубки.
Медный порошок доступен в следующих сортах:
Высокопрочная медь
Медь с восстановленным оксидом
Медь, распыленная воздухом
Медь, распыленная водой
Электролитическая медь
Специальная медь
Хлопья меди
Доступен медный порошок, распыляемый воздухом:
- Размер частиц от -10 меш (<1650 мкм) до -325 меш (<45 мкм)
Водно-распыленный медный порошок доступен:
- Размер частиц от -100 меш (<150 мкм) до -325 меш (<45 мкм)
Чтобы узнать больше о размерах других сортов, пожалуйста, свяжитесь с READE.
Химические свойства
а) От 98% до 99,999%
б) Порошок электролитической меди
Типичные приложения
Общие области применения включают, помимо прочего, автомобилестроение, скобяные изделия, строительные материалы, электрические материалы, крепеж, промышленные, морские материалы, боеприпасы, водопровод. Это также обычный ингредиент в соединениях, монетах и проводах.
Описание
Медь — один из важнейших элементов.Это красноватый металл, ковкий и пластичный с ярким металлическим блеском. Медь — хороший проводник тепла и электричества (уступает только серебру по электропроводности). Из-за его пластичности его легко формовать в листы, проволоку и трубки.
Химическое название: Cu
Упаковка
Банки, ведра, бочки, многослойные бумажные мешки, мешки для массовых грузов и контейнеры из ДВП. Для получения дополнительной информации о вариантах упаковки свяжитесь с READE.
Синонимы
Медный порошок, медный порошок, медные хлопья, сферический медный порошок, атомизированный медный порошок, электролитический медный порошок, медный нанопорошок, медный туман, медная металлическая пыль, медная пыль, медные гранулы, медная дробь, медная дробь, медная стружка, медные осадки , Медный металлический порошок, измельченная медь, медный дым, медный порошок OFHC, бронзовый порошок, номер CAS 7440-50-8
Классификация
Медь металлическая, медный порошок и медные гранулы TSCA (SARA Title III) Статус: внесен в список.Для получения дополнительной информации, пожалуйста, позвоните в E.P.A. по телефону +1.202.554.1404
Медь металлическая, медный порошок и медные гранулы Номер CAS: CAS # 7440-50-8
Международная карта химической безопасности CDC / NIOSH — Медный (Cu) порошок: посетите эту внешнюю ссылку
Медь металлическая, медный порошок и медные гранулы Номер ООН: 3089
Сопутствующие товары
Объемные свойства — Свойства материалов — OCR Gateway — GCSE Combined Science Revision — OCR Gateway
Отдельные атомы не обладают физическими свойствами веществ, которые их содержат.Например, атом меди не может проводить электричество, хотя кусок меди может это делать. Объемные свойства — это свойства, обусловленные совместным действием множества атомов, ионов или молекул.
Точки плавления и кипения
Химические связи разрываются или преодолеваются во время плавления и кипения. Чем прочнее эти связи, тем выше температура плавления и кипения.





 Эта особенность главным образом определила применение металлической меди.
Эта особенность главным образом определила применение металлической меди. Данные действительно впечатляют. Температура плавления меди превышает одну тысячу градусов Цельсия! А температура кипения составляет 2570 градусов Цельсия.
Данные действительно впечатляют. Температура плавления меди превышает одну тысячу градусов Цельсия! А температура кипения составляет 2570 градусов Цельсия.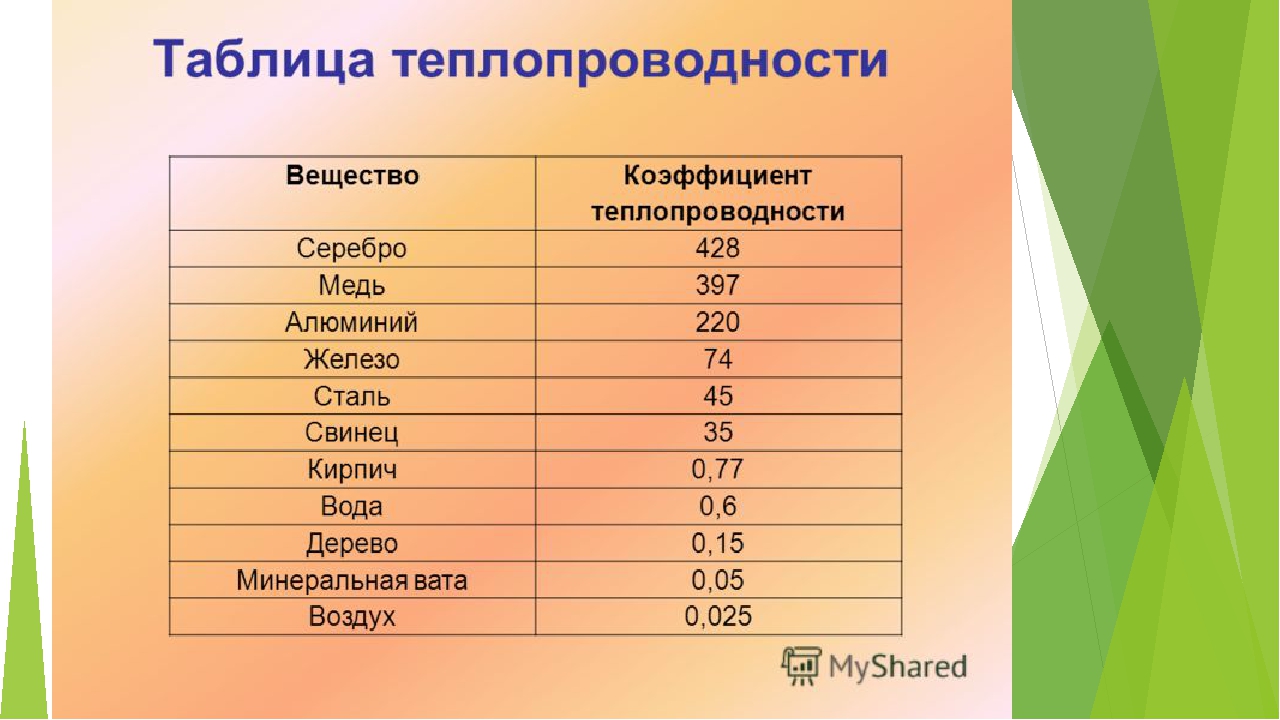 Кроме того, она никак не реагирует при контакте с такими химическими элементами, как:
Кроме того, она никак не реагирует при контакте с такими химическими элементами, как: Бронза по праву может считаться одним из величайших достижений металлургов древности. По сути, бронза — это соединение меди с прочими элементами. В большинстве случаев в роли второго компонента выступает олово. Но вне зависимости от того, какие элементы входят в сплав, основным компонентом всегда является медь. Формула латуни содержит главным образом медь и цинк, но возможны и дополнения к ним в виде других химических элементов.
Бронза по праву может считаться одним из величайших достижений металлургов древности. По сути, бронза — это соединение меди с прочими элементами. В большинстве случаев в роли второго компонента выступает олово. Но вне зависимости от того, какие элементы входят в сплав, основным компонентом всегда является медь. Формула латуни содержит главным образом медь и цинк, но возможны и дополнения к ним в виде других химических элементов. Он является высокоэкологичным материалом. Именно поэтому он используется при строительстве домов. Например, кровельное покрытие, выполненное из металлической меди, благодаря своей высочайшей коррозийной устойчивости обладает сроком службы более сотни лет, не требуя при этом особого ухода и покраски.
Он является высокоэкологичным материалом. Именно поэтому он используется при строительстве домов. Например, кровельное покрытие, выполненное из металлической меди, благодаря своей высочайшей коррозийной устойчивости обладает сроком службы более сотни лет, не требуя при этом особого ухода и покраски. Восполнить дефицит этого вещества можно при помощи специально подобранного питания. Медь содержится во многих продуктах питания, поэтому составить полезный рацион по душе не составит труда. Для примера, одним из продуктов, в составе которых имеется этот элемент, является обычное молоко.
Восполнить дефицит этого вещества можно при помощи специально подобранного питания. Медь содержится во многих продуктах питания, поэтому составить полезный рацион по душе не составит труда. Для примера, одним из продуктов, в составе которых имеется этот элемент, является обычное молоко. Только при выполнении этого условия использование медных кастрюлек не несет угрозы пищевого отравления.
Только при выполнении этого условия использование медных кастрюлек не несет угрозы пищевого отравления. Купить медь можно в комании «КУПРУМ».
Купить медь можно в комании «КУПРУМ». Также медь обладает очень высокой теплопроводностью. Такие примеси как железо, фосфор, олово, сурьма и мышьяк влияют на базовые свойства и уменьшают электропроводность и теплопроводность. По данным показателям медь уступает лишь серебру.
Также медь обладает очень высокой теплопроводностью. Такие примеси как железо, фосфор, олово, сурьма и мышьяк влияют на базовые свойства и уменьшают электропроводность и теплопроводность. По данным показателям медь уступает лишь серебру. С водородом, углеродом и азотом химических реакций нет. На влажном воздухе происходит окисление с образованием карбоната меди (II) – верхнего слоя платины.
С водородом, углеродом и азотом химических реакций нет. На влажном воздухе происходит окисление с образованием карбоната меди (II) – верхнего слоя платины. Метод позволяет получить медный порошкообразный концентрат, который содержит 10-35% меди.
Метод позволяет получить медный порошкообразный концентрат, который содержит 10-35% меди. В конвертере образуется черновая медь, которая содержит 98,4-99,4% меди, железо, серу, а также незначительное количество никеля, олова, серебра и золота.
В конвертере образуется черновая медь, которая содержит 98,4-99,4% меди, железо, серу, а также незначительное количество никеля, олова, серебра и золота. Реже применяются сплавы с неметаллами: фосфором, серой, кислородом. Выделяют две группы медных сплавов: латуни (сплавы с цинком) и бронзы (сплавы с другими элементами).
Реже применяются сплавы с неметаллами: фосфором, серой, кислородом. Выделяют две группы медных сплавов: латуни (сплавы с цинком) и бронзы (сплавы с другими элементами). Во время кипячения в пищу может попасть большое количество меди. Если же посуда внутри покрыта слоем олова, то опасности отравления нет.
Во время кипячения в пищу может попасть большое количество меди. Если же посуда внутри покрыта слоем олова, то опасности отравления нет. Электропроводность меди в твердом состоянии зависит в первую очередь от чистоты металла. Примеси и легирующие элементы уменьшают электропроводность меди (рис. 1 и 2 ) и повышают ее удельное электросопротивление (рис. 3).
Электропроводность меди в твердом состоянии зависит в первую очередь от чистоты металла. Примеси и легирующие элементы уменьшают электропроводность меди (рис. 1 и 2 ) и повышают ее удельное электросопротивление (рис. 3). С повышением температуры удельное электросопротивление меди увеличивается. Например, удельное электросопротивление меди марки M 1 в твердом состоянии при температуре, близкой к температуре плавления, составляет 0,113х10 -6 Ом*м, а в жидком – 0,203х10 -6 Ом м.
С повышением температуры удельное электросопротивление меди увеличивается. Например, удельное электросопротивление меди марки M 1 в твердом состоянии при температуре, близкой к температуре плавления, составляет 0,113х10 -6 Ом*м, а в жидком – 0,203х10 -6 Ом м. 1250К приведены в табл. 2.
1250К приведены в табл. 2.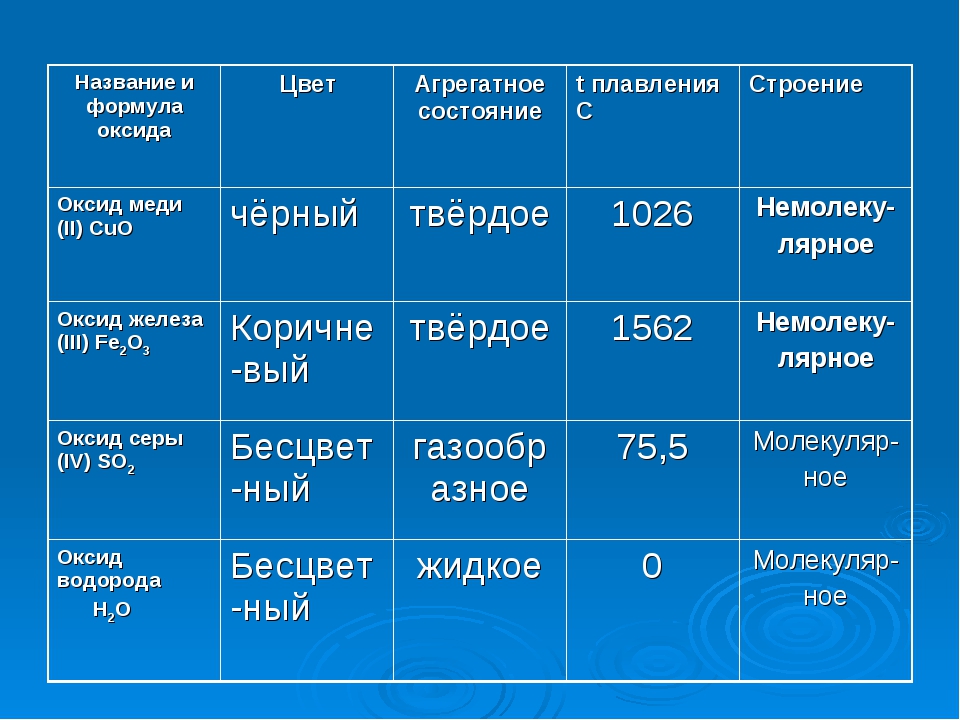 Иногда медь встречается в самородном виде, масса отдельных скоплений может достигать 400 тонн.
Иногда медь встречается в самородном виде, масса отдельных скоплений может достигать 400 тонн.  Медь среди всех других металлов обладает одной из самых высоких теплопроводностей и одним из самых низких электрических сопротивлений (при 20°C удельное сопротивление 1,68·10
Медь среди всех других металлов обладает одной из самых высоких теплопроводностей и одним из самых низких электрических сопротивлений (при 20°C удельное сопротивление 1,68·10 Поэтому соляная и разбавленная серная кислоты на медь не действуют. Однако в присутствии кислорода воздуха медь растворяется в этих кислотах с образованием соответствующих солей:
Поэтому соляная и разбавленная серная кислоты на медь не действуют. Однако в присутствии кислорода воздуха медь растворяется в этих кислотах с образованием соответствующих солей: