масса, температура плавления, удельная теплоемкость
- Редакция
- Реклама на сайте
- Новости
- О проекте
- Контакты
- Главная
- Каменные
- Бутовый камень
- Брусчатка
- Глина
- Гравий
- Галька
- Искусственный керамзитовый гравий
- Природный гравий
- Мрамор
- Искусственный мрамор
- Натуральный мрамор
- Песок
- Cтроительный песок
- Кварцевый песок
- Перлитовый песок
- Карьерный песок
- Речной песок
- Стеновые блоки и камни
- Шлакоблоки
- Арболитовые блоки
- Газобетонные блоки
- Газосиликатные блоки
- Керамзитоблоки
- Керамические блоки
- Полистиролбетонные блоки
- Твинблоки
- Бризолит
- Пескобетонные блоки
- Теплоэффективные блоки
- Опилкобетонные блоки
- Щебень
- Гравийный щебень
- Щебень известняковый
- Вторичный и мраморный
- Декоративный цветной и черный
- Вяжущие
- Неорганические
- Цементы
- Строительный цемент
- Портландцемент
- Расширяющиеся цементы
- Цемент глиноземистый
- Цементы огнеупорные и кислотоупорные
- Белый и цветной цемент
- Водостойкие цементы
- Известь
- Гипс
- Доломит
- Магнезит
- Жидкое стекло
- Известняк
- Цементы
- Органические
- Рубероид
- Пергамин
- Изол
- Бризол
- Гидроизол
- Толь
- Битум
- Битумные мастики
- Асфальт
- Неорганические
- Лесные
- Древесина
- Общие сведения
- Способы обработки
- Породы
- Древесные плиты
- ДСП
- ДВП
- МДФ
- ОСБ
- Необработанные лесоматериалы
- Пиломатериалы
- Фанера
- Древесина
- Керамические
- Кирпич
- Красный
- Силикатный
- Клинкерный
- Керамогранит
- Плитка
- Кафель
- Клинкерная
- Метлахская
- Майолика
- Мозаика
- Терракота
- Трубы
- Черепица
- Битумная
- Композитная
- Керамическая
- Цементно-песчаная
- Металлочерепица
- Кирпич
- Металлические
- Метизы
- Анкеры
- Гвозди
- Саморезы
- Шурупы
- Дюбель
- Виды металлов
- Цветные
- Латунь
- Алюминий
- Бронза
- Медь
- Олово
- Цинк
- Свинец
- Никель
- Титан
- Хром
- Чёрные
- Железо
- Чугун
- Вспомогательные вещества
- Цветные
- Метизы
- Бетон
- Арболит
- Асфальтобетон
- Газобетон
- Железобетон
- Керамзитобетон
- Полимербетон
- Пенобетон
- Цементобетон
- Гидротехнический
Добыча титановых руд: способы, переработка и применение
Титановые руды – это природные минералы, содержащие в своём составе титан (в скобках указано максимальное процентное содержание):
- рутил, модификациями которого являются анатаз и брукит (свыше 99%),
- лейкоксен (более 97%),
- ильменит (почти 93%),
- перовксит (до 57,8%),
- лопарит (доходит до 41%),
- сфен (почти 41%).

Титан – девятый в списке самых распространённых элементов земной коры, его присутствие обнаружено в 70 минералах, но наиболее интересными в плане переработки являются перечисленные выше.
Способы добычи
Более половины титана добывают из россыпей. Добыча в песчаных месторождениях не представляет никакой сложности. Процесс достаточно прост и не требует дробления и измельчения, осуществляется он драгами, земснарядами, экскаваторами, скреперами и другими гидравлическими устройствами.
Карьерный
Иное дело, когда руды залегают жилами на небольшой глубине. В зависимости от твёрдости вскрышных пород, приходится прибегать к их удалению с помощью землеройных механизмов или посредством проведения предварительных буровзрывных работ. После чего, вынутую руду забирают и подвергают дроблению и измельчению для дальнейшей переработки.
Шахтный
Шахтный способ применим при разработке коренных месторождений. Это наиболее затратный и трудоёмкий способ, требующий строительства целого комплекса сложных подземных сооружений, затраты на который окупаются получением целого набора полезных ископаемых, находящихся в составе титаносодержащих руд.
Методы обогащения
Так как процентное содержание диоксида титана (основного минерала титановых руд) изменчиво в зависимости от месторождения, то извлечённую породу подвергают обогащению, подразделяемому на две стадии: отделение пустой массы и выделение индивидуальных минералов.
Мокрое и сухое разделение по удельному весу
Благодаря различной плотности титаносодержащей породы и массы, не обладающей этим природным минералом, становится возможным их разделение в водной или воздушной среде под воздействием физических сил, созданных внутри специальных технических агрегатов. Это – так называемые гравитационные методы обогащения добытого материала.
Флотация
Способность разнообразных материалов удерживаться или не удерживаться на границе сред, пребывающих обычно в жидком и газообразном состоянии, нашла широкое применение в обогащении титановых руд.
В зависимости от первоначального минерала, используют свои специфические свойства химические вещества – образователи флотационной среды. Так, для ильменита в качестве таких сред выступают собиратели в виде жирных кислот. Рутил хорошо флотируется олеиновой кислотой или сульфированными производными углеводородов. Перовскит перед флотацией жирными кислотами необходимо обработать серной кислотой. Существует множество методов и технологий флотации, кроме того, они варьируются в зависимости от месторождений.
Так, для ильменита в качестве таких сред выступают собиратели в виде жирных кислот. Рутил хорошо флотируется олеиновой кислотой или сульфированными производными углеводородов. Перовскит перед флотацией жирными кислотами необходимо обработать серной кислотой. Существует множество методов и технологий флотации, кроме того, они варьируются в зависимости от месторождений.
В последнее время широкое распространение в качестве флотационного материала получило талловое масло. Впрочем, переработчики руководствуются соображениями стоимости, доступности, минимума токсичности, при выборе материала для флотации.
Магнитная и электрическая сепарация
Отличие магнитных и электрических свойств титана от других минералов положено в основу соответствующих сепараций – технологий отделения нужного материала от пустой породы под воздействием электрических и магнитных полей в специальных аппаратах. В их список входят: сепараторы, железоотделители, намагничиватели и размагничиватели.
Металлургический метод
Завершающей стадией получения титанового шлака является плавка концентрата в виде прессованных брикетов в электродуговых печах при температуре 1500-17000 C. Образующиеся в результате металлургического метода отливки содержат до 80% титана.
Промышленное применение
С момента своего открытия в конце XVIII века, титан был оценён специалистами как металл, обладающий лёгкостью, прочностью, жаростойкостью, устойчивостью к коррозии и при этом хорошо поддающийся механической обработке.
Технический титан и его сплавы широко используется в целом ряде отраслей народного хозяйства:
- Химическая индустрия не может обходиться без титановых изделий, обладающих высокой стойкостью к агрессивному воздействию. Это – специальная арматура, ёмкости, трубы, части машин и механизмов, активно используемых в этой отрасли.

- Транспорт активно применяет этот материал, в качестве альтернативы другим металлам, благодаря его низкому удельному весу. Что существенно снижает затраты при перемещении грузов в более лёгких и компактных вагонах и поездах. Используется титан и в автомобилестроении для изготовления витых пружин и систем отвода уходящих газов.
- Незаменим этот материал и в области военной техники. Броня и трубы, глушители и теплообменники, пропеллеры и турбины, являющиеся важными элементами самоходных орудий, танков, самолётов, военно-морских судов и подводных лодок, не обходятся без использования этого минерала.
Химически чистый титан отличается очень высокой жаропрочностью и устойчивостью к механическим воздействиям. Учитывая его лёгкий вес, металл нашёл своё применение в авиации, ракетостроении, космонавтике; при изготовлении электровакуумных приборов и криогенной техники.
Отдельно можно упомянуть медицинские, спортивные и декоративные направления использования этого уникального по своим свойствам материала. Медицинские инструменты и протезы, спортивные снаряды и амуниция, разнообразные декоративно-художественные изделия, известные скульптуры – всё это вместе объединяет между собой такой удивительный материал, как титан.
Медицинские инструменты и протезы, спортивные снаряды и амуниция, разнообразные декоративно-художественные изделия, известные скульптуры – всё это вместе объединяет между собой такой удивительный материал, как титан.
Месторождения в России и мире
Территория России обладает порядка 20-ью месторождениями титановых руд, расположенными в 9-и металлогенических провинциях, крупнейшими из которых являются:
- Оклемо-Становская,
- Тиманская,
- Уральская.
Также значительными запасами обладают месторождения магматического происхождения Баладекского, Джугджурского, Коларского массивов и находящееся в Амурской области месторождение Большой Сейм. Древние морские россыпи, богатые титановыми рудами размещены на Русской плите и в Сибири. Значительные запасы имеются и на территории Карелии.
За рубежом крупные месторождения докембрийского периода обнаружены в США (Тегавус), Канаде (Лейк-Тио), Норвегии (Тельнес). Запасы ильменита присутствуют на территории Канады, Норвегии, Индии, ЮАР; рутила – в ЮАР, Индии и Австралии. Также титановыми рудами в значительном количестве обладают Бразилия, Мексика и Китай.
Также титановыми рудами в значительном количестве обладают Бразилия, Мексика и Китай.
Мировые запасы
Подтверждённые мировые запасы диоксида титана составляют:
- Китай – 232,9 млн. тонн.
- Украина – 184 млн. тонн.
- Россия – 177 млн. тонн.
- Бразилия – 123 млн. тонн.
- Индия – 100 млн. тонн.
- Норвегия – 57 млн. тонн.
- Канада – 51,4 млн. тонн.
- ЮАР – 34,1 млн. тонн.
- Австралия – 21,4 млн. тонн.
- Остальные страны – 59,1 млн. тонн.
Если оценивать в процентном отношении залежи титановых руд, то ситуация будет несколько иная:
- Китай – 38%.
- Россия – 17%
- Австралия – 10%.
- Бразилия – 6%.
- Норвегия – 4%.
- Индия – 4%.
- Канада – 3%.
- Украина – 1%.
- Другие страны – 17%.
Различия объясняются разнообразием месторождений и трудностью объективной оценки точного количества залежей этого минерала.
Страны, добывающие титановые руды
По состоянию на 2018 год ситуация на рынке титана выглядит следующим образом:
- Крупнейшими добывающими странами являются Китай, Австралия, Индия, ЮАР.

- Ведущие производители по переработке руды и выплавке титана выглядят следующим образом: США, Россия, Япония, Китай.
Хотя, ещё в 2005-2006 годах 70% мирового производства ильменитового концентрата обеспечивали Австралия, Норвегия и Украина. А 90% рутилового концентрата выпускали в Австралии, ЮАР и на Украине.
Ситуация с течением времени меняется коренным образом: Китай наращивает как добычу, так и переработку совместно с окончательным производством столь ценного продукта, каким является титан для промышленности.
А другие страны пользуются тем, что доля сырья в окончательной стоимости произведённого продукта (титана) составляет лишь 5%, активно закупают исходные материалы по всему миру, не затрудняя себя разработкой новых месторождений. И на то есть свои объективные причины. Гораздо проще и дешевле заниматься освоением прибрежных морских россыпей, как это делают Австралия, Индия (штаты Керала и Мадрас), США (полуостров Флорида), ЮАР (месторождение прибрежных песков Ричардс-Бей), чем заниматься освоением подземных месторождений, подчас не обещающих высокое содержание нужных полезных ископаемых.
Применение титана — Знаешь как
Титан, известный в соединениях с 1791 г., впервые был получен в элементарном состоянии Хантером (1910 г.), но долгое время считался малопригодным для обработки из-за хрупкости. В пятидесятых годах после достаточной очистки он неожиданно оказался пластичным и сразу завоевал признание как материал, легко обр а б атыв аемый давлением. Непременное общее требование при этом — содержание не более 0,15% кислорода и 0,054 азота. Различные свойства сплавов в большой мере зависят от полиморфной модификации — гексагональной (а) или кубической (Р) структуры металла. В отсутствие примесей одна переходит в другую при температуре 882° С; легирующие добавки смещают этот переход, ускоряют либо замедляют.
В самолетостроении и ракетной технике весьма ценится удельная прочность материалов, отнесенная к плотности. В этом сплавы на основе титана, легированные алюминием,, хромом, ванадием, молибденом и оловом, почти не имеют соперников. Некоторые, также употребляемые в авиации сплавы алюминия и магния, снижают механические характеристики уже при 150° С, а титановые — сохраняют их до 430° С. Теперь легированный титан все чаще используют для изготовления фюзеляжей, частей двигателей реактивных самолетов и других ответственных деталей, для широкого применения он пока еще дорог.
Некоторые, также употребляемые в авиации сплавы алюминия и магния, снижают механические характеристики уже при 150° С, а титановые — сохраняют их до 430° С. Теперь легированный титан все чаще используют для изготовления фюзеляжей, частей двигателей реактивных самолетов и других ответственных деталей, для широкого применения он пока еще дорог.
В ракетостроении из сплавов титана делают баллоны для хранения сжатого водорода, корпусы ракет и детали двигателей.
Транспорт—автомобильный, железнодорожный и водный,, все шире пользуется титановыми сплавами, особенно необходимыми для обшивки подводных лодок.
В химическом машиностроении используют титан как противокоррозионный легкий материал для теплообменников, центрифуг, автоклавов, насосов и защиты аппаратуры от агрессивных сред.
В черной металлургии ферротитан — сплав железа с 18— 25% титана, получаемый электроплавкой рудного сырья, служит раскислителем и легирующей добавкой в марганцовистые, хромистые, хромомолибденовые и хромоникелевые стали.
В сплавы с цветными металлами, преимущественно с медью и алюминием добавляют лигатуры: купротитан (90% Сu и 10% Ті), а в алюминиевые бронзы алютит (40% Аl и до 40% Ті).
Карбид TiC вместе с WC входит в керметы, из которых делают детали газовых и реактивных двигателей.
Чистым пластичным титаном пользуются в малых количествах, преимущественно в электронике и электротехнике. Он идет на изготовление деталей радиоламп, рентгеновских трубок, а в порошке служит геттером — поглотителем остатка газов после их откачки.
Двуокись титана ТіО2— белый тонкий порошок, необходима для изготовления эмалей, глазурей и красок с высокой кроющей способностью, к тому же стойких против коррозии. Титановые белила служат для окраски корпусов кораблей, машин, станков, противокоррозионной защиты строительных конструкций и иных подобных целей. В виде порошка ТiO2 добавляют в резину, бумагу, глазури, эмали и используют как диэлектрик в электротехнике и радиоэлектронике. При современной годовой выплавке металла за рубежом около 25000 т двуокиси титана вырабатывают до 1,5 млн. т.
т.
Статья на тему Применение титана
металл. Свойства титана. Применение титана. Марки и химический состав титана
Вечный, загадочный, космический, материал будущего — все эти и многие другие эпитеты присваиваются в различных источниках титану. История открытия этого металла не была тривиальной: одновременно над выделением элемента в чистом виде трудились несколько ученых. Процесс изучения физических, химических свойств и определение областей его применения не закончен на сегодняшний день. Титан — металл будущего, место его в жизни человека еще окончательно не определено, что дает современным исследователям огромный простор для творчества и научных изысканий.
Характеристика
Химический элемент титан (Titanium) обозначается в периодической таблице Д. И. Менделеева символом Ti. Располагается в побочной подгруппе IV группы четвертого периода и имеет порядковый номер 22. Простое вещество титан – металл бело-серебристого цвета, легкий и прочный. Электронная конфигурация атома имеет следующую структуру: +22)2 )8 )10 )2, 1S22S22P63S23P63d24S2. Соответственно, титан имеет несколько возможных степеней окисления: 2, 3, 4, в наиболее устойчивых соединениях он четырехвалентен.
Электронная конфигурация атома имеет следующую структуру: +22)2 )8 )10 )2, 1S22S22P63S23P63d24S2. Соответственно, титан имеет несколько возможных степеней окисления: 2, 3, 4, в наиболее устойчивых соединениях он четырехвалентен.
Титан — сплав или металл?
Этот вопрос интересует многих. В 1910 году американский химик Хантер получил впервые чистый титан. Металл содержал всего 1 % примесей, но при этом его количество оказалось ничтожно мало и не давало возможности дальнейшего исследования его свойств. Пластичность полученного вещества достигалась толькопод воздействием высоких температур, при нормальных условиях (комнатной температуре) образец был слишком хрупок. Фактически этот элемент не заинтересовал ученых, так как перспективы его использования казались слишком неопределенными. Сложность получения и исследования еще больше снизили потенциал его применения. Только в 1925 году ученые-химики из Нидерландов И. де Бур и А. Ван-Аркел получили металл титан, свойства которого привлекли внимание инженеров и конструкторов всего мира. История исследования этого элемента начинается с 1790 года, именно в это время параллельно, независимо друг от друга, двое ученых открывают титан как химический элемент. Каждый из них получает соединение (оксид) вещества, не сумев выделить металл в чистом виде. Первооткрывателем титана считается английский минеролог монах Уильям Грегор. На территории своего прихода, расположенного в юго-западной части Англии, молодой ученый начал изучение черного песка долины Менакэна. Результатом опытов с магнитом стало выделение блестящих крупиц, которые являлись соединением титана. В это же время в Германии химик Мартин Генрих Клапрот выделил новое вещество из минерала рутиле. В 1797 году он же доказал, что открытые параллельно элементы являются аналогичными. Двуокись титана более века являлась загадкой для многих химиков, получить чистый металл оказалось не по силам даже Берцелиусу.
де Бур и А. Ван-Аркел получили металл титан, свойства которого привлекли внимание инженеров и конструкторов всего мира. История исследования этого элемента начинается с 1790 года, именно в это время параллельно, независимо друг от друга, двое ученых открывают титан как химический элемент. Каждый из них получает соединение (оксид) вещества, не сумев выделить металл в чистом виде. Первооткрывателем титана считается английский минеролог монах Уильям Грегор. На территории своего прихода, расположенного в юго-западной части Англии, молодой ученый начал изучение черного песка долины Менакэна. Результатом опытов с магнитом стало выделение блестящих крупиц, которые являлись соединением титана. В это же время в Германии химик Мартин Генрих Клапрот выделил новое вещество из минерала рутиле. В 1797 году он же доказал, что открытые параллельно элементы являются аналогичными. Двуокись титана более века являлась загадкой для многих химиков, получить чистый металл оказалось не по силам даже Берцелиусу. Новейшие технологии XX века значительно ускорили процесс изучения упомянутого элемента и определили начальные направления его использования. При этом сфера применения расширяется постоянно. Ограничить её рамки может только сложность процесса получения такого вещества, как чистый титан. Цена сплавов и металла достаточно высока, поэтому на сегодняшний день он не может вытеснить традиционное железо и алюминий.
Новейшие технологии XX века значительно ускорили процесс изучения упомянутого элемента и определили начальные направления его использования. При этом сфера применения расширяется постоянно. Ограничить её рамки может только сложность процесса получения такого вещества, как чистый титан. Цена сплавов и металла достаточно высока, поэтому на сегодняшний день он не может вытеснить традиционное железо и алюминий.
Происхождение названия
Менакин — первое название титана, которое применялось до 1795 года. Именно так, по территориальной принадлежности, назвал новый элемент У. Грегор. Мартин Клап
Титан в природе (0,6% в Земной коре)
История открытия этого элемента связана с определенными трудностями. В конце 18 века, немецкие ученые получили неизвестный материал, который был назван титаном. Название этого металла связано исключительно со стандартами химического наименования — о его свойствах было известно немного. Подробные исследования физико-химических характеристик титана стали возможны лишь в середине 20 века, когда был получен химически чистый материал для исследований. Тогда же и были установлены его удивительная прочность и ряд других качеств, благодаря которым титан стал одним из самых востребованных металлов в промышленности.
Тогда же и были установлены его удивительная прочность и ряд других качеств, благодаря которым титан стал одним из самых востребованных металлов в промышленности.
Основные характеристики
Является типичным представителем переходных металлов, внешне напоминает очищенное железо или высокоуглеродистую сталь. Очень прочен и, в тоже время, пластичен — при работе с ним возникает опасность налипания титана на поверхность инструментов. Чистый титан на воздухе довольно быстро окисляется с образованием защитной пленки, что обуславливает характерный тусклый блеск этого металла.
Примечательно, что в плане своей геохимии, титан очень схож с алюминием. В чистом виде не встречается, основная природная форма — оксиды, а также соединения кальция, различные соли и руды. Практически всегда содержится в бокситах, что позволяет проводить одновременную добычу титана и алюминия.
Физико-химические свойства
Выделение чистого титана в конце 20 века позволило провести ряд детальных исследований этого необычного металла, что привело к настоящей сенсации.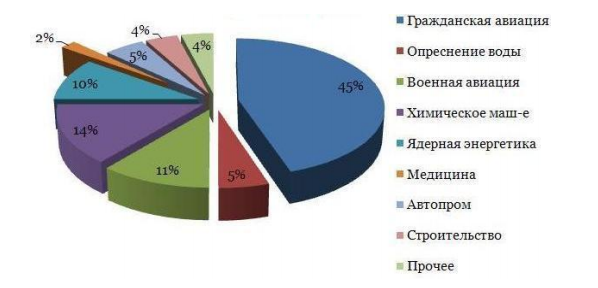 Титан обладал наивысшими показателями прочности среди всех известных тогда элементов, при этом охотно взаимодействовал с большинством реагентов. В настоящий момент физические свойства титана изучены практически досконально:
Титан обладал наивысшими показателями прочности среди всех известных тогда элементов, при этом охотно взаимодействовал с большинством реагентов. В настоящий момент физические свойства титана изучены практически досконально:
- Температура плавления — 1670 0С;
- Средняя плотность — 4,5 г/см3;
- Высокие показатели гибкости и вязкости;
Чистый титан считается довольно хрупким металлом — в нормальных условиях его прочность почти в два раза ниже, чем таковая у никеля или железа. Однако в промышленности в основном используются жаропрочные сплавы на титановой основе, которые в определенных температурных пределах превосходят по прочности и упругости все известные современные металлические соединения.
По своим химическим показателям титан относится к активным переходным металлом. Охотно вступает в реакцию с кислородом с образованием поверхностного слоя из оксида титана. Этим объясняется его коррозионная стойкость, которая характерна для всех неорганических сред. Будучи измельченным в мелкую пыль является огнеопасным веществом, легко воспламеняется с выделением большого количества энергии.
Будучи измельченным в мелкую пыль является огнеопасным веществом, легко воспламеняется с выделением большого количества энергии.
Распространение в природе
Титан является весьма активным элементом, охотно вступает в спонтанные реакции с кислородом и солями. По этой причине, в земной коре химически чистый титан никогда не встречается. Кроме того, природная аллотропная модификация этого элемента четырехвалентна, из-за чего основная форма титана — оксиды, а также соли железа, кальция и алюминия. Добыча ведется совместно с добычей других металлов, основной метод выделения титана — химическая очистка по методу кислотного травления с дальнейшей обработкой и осаждением.
По примерным оценкам, в состав земного грунта входит около 0,6% титана в чистом эквиваленте, что ставит его на десятое место по распространенности. Современные методы добычи титана позволяют использовать его в промышленных масштабах, ежегодные объемы производства оценивается в 5 миллионов тонн.
Сфера промышленного и прикладного применения
Большая часть всего получаемого титана используется для нужд машиностроения, авиационной и судостроительной промышленности. В этом качестве, титан используется наравне с алюминием и железом, что объясняется его чрезвычайно высокими прочностными характеристиками в сочетании с низким весом и плотностью.
Наибольшую известность титан получил в авиационной промышленности, где применяется для изготовления реактивных двигателей, несущих конструкций и деталей обшивки. Кроме того, титан используется во всех сферах, где необходим материал с высокой коррозионной стойкостью и жаропрочностью: химическая промышленность (изготовление емкостей и приборов), производство высокопрочных инструментов.
Что такое титан?
Каждый грамотный и образованный человек должен иметь хотя бы поверхностное представление о различных химических элементах, так как многие из них широко используются в нашей повседневной жизни. Предлагаем рассмотреть, что такое титан, какими свойствами обладает этот химический элемент и где применяется в промышленности.
Предлагаем рассмотреть, что такое титан, какими свойствами обладает этот химический элемент и где применяется в промышленности.
Титан — один из элементов побочной подгруппы четвёртой группы и четвёртого периода в периодической системе Д. И. Менделеева. Его атомный номер 22, а символ обозначения «Ti».
Физические свойства
Титан представляет собой легкий металл, имеющий серебристо-белый цвет. Он относится к числу тугоплавких металлов, так как температура его плавления составляет целых 1660 °C, а точка закипания — 3260 °C . Титан имеет особенность становиться вязким, поэтому в работе с ним используют специальные защитные вещества, препятствующие налипанию этого металла. При обычных температурах титан покрывается защитной плёнкой оксида TiO2. Титановая пыль имеет особенность взрываться, создавая вспышки с температурой 400°C.
Этот металл особенно ценен людьми за его высокую прочность и низкую плотность материала, которые сохраняются даже при высоких температурах. Также титан является плохим проводником электричества и тепла.
Также титан является плохим проводником электричества и тепла.
Химические свойства
- Титан практически не подвержен коррозии, так как на нём образуется защитная оксидная плёнка.
- Устойчив к слабым разбавленным растворам большинства щелочей и кислот.
- Способен реагировать со многими кислотами, даже со слабыми.
- При температуре выше 1200°C может загораться белым пламенем.
- При длительном кипячении оксид титана взаимодействует с серной кислотой.
- Взаимодействует с галогенами при нагревании.
- При контакте с азотом при температуре свыше 400°C образует нитрид.
- При взаимодействии с углеродом образует карбид титана.
Применение в промышленности
В химической промышленности титан используется для создания специализированного оборудования, так как этот металл имеет высокую коррозионную стойкость. Титан широко применяется в нефтяной, пищевой и электрической промышленности, а также в качестве материала для изготовления инструментов для хирургии. Его высокие показатели прочности обусловливают активное применение в авиа- и судостроении. Детали, изготовленные из титана, особо надёжны, так как способны выдержать высокое давление и большие перепады температур.
Его высокие показатели прочности обусловливают активное применение в авиа- и судостроении. Детали, изготовленные из титана, особо надёжны, так как способны выдержать высокое давление и большие перепады температур.
Узнать больше о различных химических элементах вы сможете здесь: Словарь химических терминов.
Титан
Титан и его сплавы имеют очень благоприятное отношение прочности к массе. Они также устойчивы к коррозии, поскольку на их поверхности образуется тонкий, но очень эластичный оксидный слой. Таким образом, они используются там, где важны прочность, легкость и устойчивость к коррозии. Хотя использование титана ограничено его высокой стоимостью, появляются новые процессы, которые, вероятно, значительно снизят затраты, позволяя более широко использовать титан и его сплавы.
Применение титана
Рис. 1 Использование титана.
Почти весь титан используется в сплаве с другими металлами. Среди наиболее важных легирующих металлов — алюминий, ванадий, молибден, марганец, железо, олово, хром и цирконий. Один из наиболее используемых имеет состав из 90% титана, 6% алюминия, 4% ванадия, который часто обозначается как Ti-6AI-4V.
Среди наиболее важных легирующих металлов — алюминий, ванадий, молибден, марганец, железо, олово, хром и цирконий. Один из наиболее используемых имеет состав из 90% титана, 6% алюминия, 4% ванадия, который часто обозначается как Ti-6AI-4V.
Аэрокосмическая промышленность является крупнейшим пользователем титановых сплавов, используя их в основном планере (корпусе) самолетов, а также в различных частях двигателей, шасси и гидравлических трубах (рис. 2).
|
Из-за своей прочности и устойчивости к химическому воздействию металл и сплавы используются там, где другие материалы (даже нержавеющая сталь) могут быстро разрушиться, например, в морской воде. Они используются в судовых винтах и опреснительных установках, а также в реакторах и трубопроводах химических заводов.
Они используются в судовых винтах и опреснительных установках, а также в реакторах и трубопроводах химических заводов.
Ежегодно в мире используется более 1000 тонн титановых сплавов для изготовления хирургических имплантатов, включая детали для замены тазобедренного и коленного суставов (рис. 3). Они также используются в зубных имплантатах в качестве корней заменяющих зубов и для кардиостимуляторов.
|
Недавно некоторые здания были облицованы верхней поверхностью из чистого титана для получения впечатляющего эффекта (рис. 4).
|
Годовое производство титана
| Весь мир | 171 000 тонн |
| Китай | 80 000 тонн |
| Россия | 42 000 тонн |
| Япония | 30 000 тонн |
| Казахстан | 9 000 тонн |
| Украина | 9 000 тонн |
Данные из:
U. S. Geological Survey, Mineral Commodity Summaries, 2016.
S. Geological Survey, Mineral Commodity Summaries, 2016.
Данные по США отсутствуют.
Производство титана
Титан составляет 0,63% земной коры и является четвертым по распространенности структурным металлом после алюминия, железа и магния.
Титановые месторождения, которые можно добывать экономически, находятся по всему миру. Основными рудами являются рутил (TiO 2 ) и ильменит (FeTiO 3 ) в отложениях пляжного песка (Западная Австралия), ильменит-гематит (Канада) и ильменит-магнетит (Украина) в месторождениях твердых пород (рис. 5). .Хотя рутил более редок и дороже, чем ильменит, он используется чаще, поскольку не содержит соединений железа и поэтому может быть более легко переработан. Однако иногда ильменит обрабатывают для удаления железа и получения «синтетического» рутила.
Рис. 5 Складирование концентрата тяжелых минералов, содержащего рутил, ильменит и циркон
, а также другие тяжелые минералы, не представляющие ценности. Затем он будет подвергнут дальнейшей обработке
Затем он будет подвергнут дальнейшей обработке
для отделения рутила перед началом процесса извлечения титана.
С любезного разрешения Iluka Resources.
Процесс Кролла
Большая часть титана производится из руд, содержащих диоксид титана, с использованием длительного четырехступенчатого процесса:
a) хлорирование руды до хлорида титана (IV)
b) очистка хлорида титана (IV)
c) восстановление титана (IV) хлорид до титановой губки
г) обработка титановой губки
(a) Хлорирование руды до хлорида титана (IV)
Диоксид титана термически стабилен и очень устойчив к химическому воздействию.Его нельзя восстановить с помощью углерода, оксида углерода или водорода, а восстановление с помощью более электроположительных металлов является неполным. Однако, если оксид превращается в хлорид титана (IV), путь к титану становится жизнеспособным, так как хлорид легче восстанавливается.
Сухая руда подается в хлоратор вместе с коксом, образуя псевдоожиженный слой. После предварительного нагрева слоя тепла реакции с хлором достаточно для поддержания температуры 1300 K:
После предварительного нагрева слоя тепла реакции с хлором достаточно для поддержания температуры 1300 K:
(b) Очистка хлорида титана (IV)
Неочищенный хлорид титана (IV) очищают перегонкой после химической обработки сероводородом или минеральным маслом для удаления оксихлорида ванадия, VOCl 3 , который кипит при той же температуре, что и хлорид титана (IV).Конечный продукт представляет собой чистый (> 99,9%) хлорид титана (IV), который может быть использован либо для производства титана, либо окислен для получения диоксида титана для пигментов.
Резервуары для хранения должны быть полностью сухими, поскольку продукт подвергается быстрому гидролизу в присутствии воды с образованием плотных белых паров хлористого водорода:
(c) Восстановление хлорида титана (IV) до титановой губки
Хлорид титана (IV) — летучая жидкость. Его нагревают, чтобы получить пар, который подают в реактор из нержавеющей стали, содержащий расплавленный магний (в избытке), предварительно нагретый до примерно 800 К в атмосфере аргона. Экзотермические реакции с образованием хлоридов титана (III) и титана (II) вызывают быстрое повышение температуры примерно до 1100 К. Эти хлориды медленно восстанавливаются, поэтому температуру повышают до 1300 К для завершения процесса восстановления. Тем не менее, это длительный процесс:
Экзотермические реакции с образованием хлоридов титана (III) и титана (II) вызывают быстрое повышение температуры примерно до 1100 К. Эти хлориды медленно восстанавливаются, поэтому температуру повышают до 1300 К для завершения процесса восстановления. Тем не менее, это длительный процесс:
Через 36-50 часов реактор вынимают из печи и дают ему остыть не менее четырех дней.
Непрореагировавший магний и смесь хлорид / титан извлекают, измельчают и выщелачивают разбавленной соляной кислотой для удаления хлорида магния.В альтернативном методе, используемом в Японии, хлорид магния вместе с непрореагировавшим магнием удаляют из титана путем высокотемпературной вакуумной перегонки.
Хлорид магния подвергается электролизу с образованием магния для стадии восстановления, а хлор возвращается на стадию хлорирования руды.
Титан очищают высокотемпературной вакуумной перегонкой. Металл имеет форму пористой гранулы, которую называют губкой. Это может быть обработано на месте или продано
Титан Определение, Факты, Символ, Открытие, Собственность, Использование
Что такое титан
Титан (произношение: ti-TAY-nee-em) — твердый, блестящий, прочный и легкий элемент, классифицируемый как переходный металл и представленный химическим символом Ti [1, 2, 3] . По сравнению с другими ферромагнитными элементами, титан является слабомагнитным металлом, который проявляет свои магнитные характеристики в присутствии внешних магнитных полей [4] .
По сравнению с другими ферромагнитными элементами, титан является слабомагнитным металлом, который проявляет свои магнитные характеристики в присутствии внешних магнитных полей [4] .
Титановый символ
Изотопы
Существует пять стабильных природных изотопов титана, включая Титан-46, Титан-47, Титан-48, Титан-49 и Титан-50, причем Титан-48 имеет наибольшее естественное содержание 73,8% [5] . Титан характеризуется 21 радиоизотопом, из которых наиболее стабильными являются Титан-44, Титан-45, Титан-51 и Титан-52 с периодом полураспада 60 лет, 184.8 минут, 5,76 минуты и 1,7 минуты соответственно [5] .
Где найти титан
Являясь девятым по содержанию элементом земной коры, титан обычно содержится в вулканических породах и их отложениях [1] . Он присутствует в таких минералах, как рутил (диоксид титана), ильменит (оксид титана-железа) и сфен (несиликат кальция-титана), а также в титанате (оксид титана) и некоторых железных рудах [1] .
Его коммерчески извлекают из руды путем восстановления хлорида титана (IV) с использованием натрия или магния [1] .Оксид титана (IV) получают из ильменита с использованием хлора (хлоридный процесс) или серной кислоты (сульфатный процесс) [1] .
В тройку крупнейших производителей титана входят Канада, Австралия и Южная Африка, а в тройку крупнейших держателей запасов титана входят Китай, Австралия и Индия [1] .
Титан
История
Происхождение названия : Название происходит от слова «Титан», которое в греческой мифологии означает «сыновья Богини Земли» [1, 2] .
Кто его открыл : Титан был обнаружен британским минералогом и священнослужителем Уильямом Грегором [1] .
Когда и как было обнаружено
В 1791 году титановый минерал менакканит был обнаружен в Корнуолле Уильямом Грегором [1] . Он изучил его и пришел к выводу, что он состоит из оксида железа и нового металла, о котором он сообщил Королевскому геологическому обществу [1] .
Немецкий химик Мартин Генрих Клапрот в 1795 году проанализировал красную минеральную руду под названием Schörl [1] .Это был оксид неизвестного элемента, который Клапрот назвал титаном [1] . Узнав об открытии Грегора, Клапрот исследовал менакканит и подтвердил, что он состоит из титана [1] .
М.А. Хантер, металлург из Новой Зеландии, в 1910 г. произвел чистый металлический титан из тетрахлорида титана и металлического натрия [1] .
Титановое обозначение | |||
| Атомный номер | 22 [1] | ||
| Номер CAS | 7440-32-6 [1] | ||
| Позиция в таблице Менделеева | Группа | Период | Блок |
| 4 [1] | 4 [1] | d [1] | |
Где находится титан в таблице Менделеева
Свойства и характеристики титана
Общие свойства | ||||||||||||||||
| Относительная атомная масса | 47. 867 [1] 867 [1] | |||||||||||||||
| Атомная масса | 47,867 а.е.м. [1] | |||||||||||||||
| Молярная масса | 47,8670 г / моль [6] | |||||||||||||||
| Молекулярный вес | 47,867 г / моль [7] | |||||||||||||||
Физические свойства | ||||||||||||||||
| Цвет | Серебристо-белый [8] | |||||||||||||||
| Температура плавления / замерзания | 1670 ° C, 3038 ° F [1] | |||||||||||||||
| Температура кипения | 3287 ° C, 5949 ° F [1] | |||||||||||||||
| Плотность | 4.506 г см -3 [1] | |||||||||||||||
| Состояние вещества при комнатной температуре (твердое тело / жидкость / газ) | Цельный [1, 8] | |||||||||||||||
| Твердость | ||||||||||||||||
| — Бринелл | 715 МПа [9] | |||||||||||||||
| — Моос | 6 [9] | |||||||||||||||
| — Виккерс | 970 МПа [9] | |||||||||||||||
| Электропроводность | 2. 5 X 10 6 См / м [9] 5 X 10 6 См / м [9] | |||||||||||||||
| Заряд | +3, +4 [10] | |||||||||||||||
| Теплопроводность | 22 Вт / (м · К) [9] | |||||||||||||||
| Удельная теплоемкость | 524 Дж кг -1 K -1 [1] | |||||||||||||||
| Объемный модуль | Неизвестно [1] | |||||||||||||||
| Модуль сдвига | 43.8 ГПа [1] | |||||||||||||||
| Модуль Юнга | 115,7 ГПа [1] | |||||||||||||||
| Давление пара | ||||||||||||||||
| — Температура (К) | 400 | 600 | 800 | 1000 | 1200 | 1400 | 1600 | 1800 | 2000 | 2200 | 2400 | |||||
| — Давление (Па) | – | – | – | – | 9. 69 Х 10 -9 69 Х 10 -9 | 7,44 Х 10 -6 | 1.06 Х 10 -3 | 0,0493 | 0,978 | 10,6 | 76,9 | |||||
Химические свойства | ||||||||||||||||
| Степени окисления | 4, 3 [1] | |||||||||||||||
| Изотопы | Изотоп | Масса | Численность (%) | Период полураспада | Тип распада | |||||||||||
| 46 Ti | 45.953 | 8,25 | – | – | ||||||||||||
| 47 Ti | 46,952 | 7,44 | – | – | ||||||||||||
| 48 Ti | 47,948 | 73,72 | – | – | ||||||||||||
| 49 Ti | 48,948 | 5,41 | – | – | ||||||||||||
| 50 Ti | 49. 945 945 | 5,18 | – | – | ||||||||||||
Титан Lewis Dot Structure
Атомные данные титана (элемент 22)
| Валентные электроны | 4 [11] | |||||||
| Квантовые числа | ||||||||
| — н. | 3 [12] | |||||||
| — | 2 [12] | |||||||
| — м ℓ | -1 [12] | |||||||
| — м с | +1/2 [12] | |||||||
| Электронная конфигурация (конфигурация благородного газа) | [Ar] 3d 2 4s 2 [1] | |||||||
| Атомная структура | ||||||||
| — Количество электронов | 22 [8] | |||||||
| — Количество нейтронов | 26 [8] | |||||||
| — Количество протонов | 22 [8] | |||||||
| Радиус атома | ||||||||
| — Атомный радиус | 2. 11 Å [1] 11 Å [1] | |||||||
| — Ковалентный радиус | 1,48 Å [1] | |||||||
| Электроотрицательность (шкала Полинга) | 1,54 [1] | |||||||
| Сродство к электрону | 7,622 кДж моль -1 [1] | |||||||
| Энергия ионизации (кДж моль -1 ) | 1-й | 2-я | 3-й | 4-я | 5-я | 6-я | 7-я | 8-я |
| 658.813 | 1309,837 | 2652,546 | 4174.651 | 9581 | 11532,89 | 13585.1 | 16441,1 | |
Титановая электронная конфигурация (модель Бора)
Что такое титан, используемый для
- Титан образует важные сплавы с другими металлами, включая молибден, железо и алюминий, которые используются в ракетах, самолетах и космических кораблях из-за их низкой плотности и устойчивости к высоким температурам [1, 8] .

- Хотя он прочен, как сталь, он имеет гораздо меньшую плотность, из-за чего его обычно используют в ноутбуках, клюшках для гольфа, костылях и велосипедах [1, 8] .
- Поскольку титановые трубы устойчивы к коррозии, они используются в конденсаторах электростанций [1] .
- Обладая превосходной коррозионной стойкостью в морской воде, он широко используется для гребных валов, корпусов кораблей, подводных лодок и в опреснительных установках [1, 8] .
- Титан находит множество хирургических применений, включая его использование при замене тазобедренного сустава и зубных имплантатах [1, 8] .
- Поскольку его пигмент обладает большой укрывистостью, он используется в пластике, художественной краске, краске для дома, эмали и бумаге [1] .
- Он используется в солнечных обсерваториях из-за его превосходных свойств отражения инфракрасного излучения [1] .
- Оксид титана является важным ингредиентом солнцезащитных кремов, используемых для защиты кожи от УФ-излучения [1] .

Токсичность и воздействие на здоровье
Хотя чистый титан считается нетоксичным, воздействие большого количества пыли диоксида титана может быть опасным [1] .Хотя безопасность нано-TiO 2 неясна, исследования показали, что он может повредить функции печени, почек, мозга и легких при вдыхании или приеме в высоких дозах [13] . Он также может быть токсичным для эмбрионов в процессе развития [13] . Неизвестно, что титан играет какую-либо биологическую роль [1] .
Орбитальная диаграмма из титана
Интересные факты
- Каждая магматическая порода (образовавшаяся в результате охлаждения и затвердевания лавы) состоит из титана [3] .
- По данным Boeing, 737 Dreamliner на 15 процентов состоит из титана [3] .
- На спутниковом снимке 2011 года были обнаружены богатые титаном горные породы на поверхности Луны [3] .
- Графическое изображение титана указывает на раннюю вотивную статую, основанную на титанах в греческой мифологии [1] .

Титан Цена
Стоимость чистого титана составляет около 6,61 доллара за грамм [8] .
Список литературы
- http: // www.rsc.org/periodic-table/element/22/titanium
- https://education.jlab.org/itselemental/ele022.html
- https://www.livescience.com/29103-titanium.html
- https://terpconnect.umd.edu/~wbreslyn/magnets/is-titanium-magnets.html
- https://education.jlab.org/itselemental/iso022.html
- https://www.webqc.org/molecular-weight-of-Ti.html
- https://pubchem.ncbi.nlm.nih.gov/compound/titanium
- https://www.chemicool.com/elements/titanium.html
- http://periodictable.com/Elements/022/data.html
- http://www.ochemonline.com/Ions
- http://butane.chem.uiuc.edu/pshapley/GenChem2/Intro/2.html
- http://chemistry-reference.com/q_elements.asp?Symbol=Ti
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5540742/
определение титана и синонимов титана (английский)
| Внешний вид | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| серебристый серо-белый металлик | |||||||||||||||
| Общая недвижимость | |||||||||||||||
| Название, символ, номер | титан, Ti, 22 | ||||||||||||||
| Произношение | / taɪˈteɪniəm / tye- TAY -nee-əm | ||||||||||||||
| Категория элемента | переходный металл | ||||||||||||||
| Группа, период, блок | 4, 4, д | ||||||||||||||
| Стандартный атомный вес | 47. 867 (1) 867 (1) | ||||||||||||||
| Электронная конфигурация | [Ar] 4s 2 3d 2 | ||||||||||||||
| Электронов на оболочку | 2, 8, 10, 2 (Изображение) | ||||||||||||||
| Физические свойства | |||||||||||||||
| Фаза | твердый | ||||||||||||||
| Плотность (около комнатной) | 4,506 г · см −3 | ||||||||||||||
| Плотность жидкости при т.пл. | 4,11 г · см −3 | ||||||||||||||
| Температура плавления | 1941 К, 1668 ° С, 3034 ° F | ||||||||||||||
| Температура кипения | 3560 К, 3287 ° С, 5949 ° F | ||||||||||||||
| Теплота плавления | 14.15 кДж · моль −1 | ||||||||||||||
| Теплота испарения | 425 кДж · моль −1 | ||||||||||||||
| Молярная теплоемкость | 25,060 Дж · моль −1 · K −1 | ||||||||||||||
| Давление пара | |||||||||||||||
| |||||||||||||||
| Атомные свойства | |||||||||||||||
| Степени окисления | 4 , 3, 2, 1 [1] (амфотерный оксид) | ||||||||||||||
| Электроотрицательность | 1. 54 (шкала Полинга) 54 (шкала Полинга) | ||||||||||||||
| Энергии ионизации (подробнее) | 1-й: 658,8 кДж · моль −1 | ||||||||||||||
| 2-я: 1309,8 кДж · моль −1 | |||||||||||||||
| 3-я: 2652,5 кДж · моль −1 | |||||||||||||||
| Атомный радиус | 147 часов | ||||||||||||||
| Ковалентный радиус | 160 ± 20 часов | ||||||||||||||
| Разное | |||||||||||||||
| Кристаллическая структура | гексагональный | ||||||||||||||
| Магнитный заказ | парамагнитный | ||||||||||||||
| Удельное электрическое сопротивление | (20 ° C) 420 нОм · м | ||||||||||||||
| Теплопроводность | 21.9 Вт · м −1 · K −1 | ||||||||||||||
| Тепловое расширение | (25 ° C) 8,6 мкм · м −1 · K −1 | ||||||||||||||
| Скорость звука (тонкий стержень) | (вправо) 5,090 м · с −1 | ||||||||||||||
| Модуль Юнга | 116 ГПа | ||||||||||||||
| Модуль сдвига | 44 ГПа | ||||||||||||||
| Объемный модуль | 110 ГПа | ||||||||||||||
| Коэффициент Пуассона | 0. 32 32 | ||||||||||||||
| Твердость по Моосу | 6,0 | ||||||||||||||
| Твердость по Виккерсу | 970 МПа | ||||||||||||||
| Твердость по Бринеллю | 716 МПа | ||||||||||||||
| Регистрационный номер CAS | 7440-32-6 | ||||||||||||||
| Наиболее стабильные изотопы | |||||||||||||||
| Основная статья: Изотопы титана | |||||||||||||||
| · р | |||||||||||||||
Титан (/ taɪˈteɪniəm / ty- TAY -nee-əm ) представляет собой химический элемент с символом Ti и атомным номером 22.Он имеет низкую плотность и представляет собой прочный, блестящий, устойчивый к коррозии (включая морскую воду, царскую водку и хлор) переходный металл серебристого цвета.
Титан был обнаружен в Корнуолле, Великобритания, Уильямом Грегором в 1791 году и назван Мартином Генрихом Клапротом в честь титанов греческой мифологии. Этот элемент встречается в ряде месторождений полезных ископаемых, в основном рутила и ильменита, которые широко распространены в земной коре и литосфере, и он содержится почти во всех живых существах, скалах, водоемах и почвах. [2] Металл извлекается из основных минеральных руд с помощью процесса Кролла [3] или процесса Хантера. Его наиболее распространенное соединение, диоксид титана, является популярным фотокатализатором и используется при производстве белых пигментов. [4] Другие соединения включают тетрахлорид титана (TiCl 4 ), компонент дымовых завес и катализаторов; и трихлорид титана (TiCl 3 ), который используется в качестве катализатора при производстве полипропилена. [2]
[2] Металл извлекается из основных минеральных руд с помощью процесса Кролла [3] или процесса Хантера. Его наиболее распространенное соединение, диоксид титана, является популярным фотокатализатором и используется при производстве белых пигментов. [4] Другие соединения включают тетрахлорид титана (TiCl 4 ), компонент дымовых завес и катализаторов; и трихлорид титана (TiCl 3 ), который используется в качестве катализатора при производстве полипропилена. [2]
Титан может быть легирован железом, алюминием, ванадием, молибденом, среди других элементов, для производства прочных легких сплавов для аэрокосмической промышленности (реактивные двигатели, ракеты и космические аппараты), военной промышленности, промышленных процессов (химическая и нефтехимическая промышленность, опреснительные установки, целлюлоза). и бумага), автомобилестроение, агропищевая промышленность, медицинские протезы, ортопедические имплантаты, стоматологические и эндодонтические инструменты и файлы, зубные имплантаты, спортивные товары, ювелирные изделия, мобильные телефоны и другие приложения. [2]
[2]
Двумя наиболее полезными свойствами металлической формы являются коррозионная стойкость и самое высокое отношение прочности к весу среди всех металлов. [5] В нелегированном состоянии титан такой же прочный, как и некоторые стали, но на 45% легче. [6] Есть две аллотропные формы [7] и пять встречающихся в природе изотопов этого элемента, от 46 до Ti до 50 Ti, причем 48 Ti является наиболее распространенным (73,8%). [8] Титан по своим химическим и физическим свойствам подобен цирконию, потому что оба они имеют одинаковое количество валентных электронов и находятся в одной группе в периодической таблице.
Характеристики
Физические свойства
Металлический элемент, титан, известен своим высоким отношением прочности к весу. [7] Это прочный металл с низкой плотностью, довольно пластичный (особенно в бескислородной среде), [2] блестящий и металлический белый цвет. [9] Относительно высокая температура плавления (более 1650 ° C или 3000 ° F) делает его полезным в качестве тугоплавкого металла. Он парамагнитен и имеет довольно низкую электрическую и теплопроводность. [2]
[9] Относительно высокая температура плавления (более 1650 ° C или 3000 ° F) делает его полезным в качестве тугоплавкого металла. Он парамагнитен и имеет довольно низкую электрическую и теплопроводность. [2]
Коммерческие марки титана (чистота 99,2%) имеют предел прочности на разрыв около 434 МПа (63000 фунтов на кв. Дюйм), что соответствует таковому у обычных низкосортных стальных сплавов, но на 45% легче. [6] Титан на 60% плотнее алюминия, но более чем в два раза прочнее [6] , чем наиболее часто используемый алюминиевый сплав 6061-T6. Некоторые титановые сплавы (например, Beta C) достигают предела прочности на разрыв более 200000 фунтов на квадратный дюйм (1400 МПа). [10] Однако титан теряет прочность при нагревании выше 430 ° C (806 ° F). [11]
Он довольно твердый (хотя и не такой твердый, как некоторые марки термообработанной стали), немагнитный и плохо проводит тепло и электричество. Обработка требует мер предосторожности, так как материал размягчается и истирается, если не использовать острые инструменты и не использовать надлежащие методы охлаждения. Как и конструкции из стали, титановые конструкции имеют предел выносливости, который гарантирует долговечность в некоторых областях применения. [9] Удельная жесткость титановых сплавов также обычно не так хороша, как у других материалов, таких как алюминиевые сплавы и углеродное волокно, поэтому их меньше используют для конструкций, требующих высокой жесткости.
Как и конструкции из стали, титановые конструкции имеют предел выносливости, который гарантирует долговечность в некоторых областях применения. [9] Удельная жесткость титановых сплавов также обычно не так хороша, как у других материалов, таких как алюминиевые сплавы и углеродное волокно, поэтому их меньше используют для конструкций, требующих высокой жесткости.
Металл представляет собой диморфный аллотроп, гексагональная альфа-форма которого превращается в объемноцентрированную кубическую (решеточную) β-форму при 882 ° C (1620 ° F). [11] Удельная теплоемкость альфа-формы резко увеличивается по мере ее нагрева до этой температуры перехода, но затем падает и остается довольно постоянной для β-формы независимо от температуры. [11] Подобно цирконию и гафнию, существует дополнительная омега-фаза, которая термодинамически стабильна при высоких давлениях, но является метастабильной при атмосферном давлении.Эта фаза обычно гексагональная ( идеальная ) или тригональная ( искаженная ) и может рассматриваться как происходящая из-за мягкого продольного акустического фонона β-фазы, вызывающего коллапс (111) плоскостей атомов. [12]
[12]
Химические свойства
Наиболее заметным химическим свойством титана является его превосходная устойчивость к коррозии; он почти так же устойчив, как платина, способен противостоять воздействию разбавленной серной и соляной кислот, а также газообразного хлора, хлоридных растворов и большинства органических кислот. [3] Однако он растворим в концентрированных кислотах. [14] Диаграмма Пурбе на изображении показывает, что титан на самом деле термодинамически является очень химически активным металлом.
Однако он медленно реагирует с водой и воздухом, поскольку образует пассивное и защитное оксидное покрытие, которое защищает его от дальнейшей реакции. [2] Когда он образуется впервые, этот защитный слой имеет толщину всего 1-2 нм, но продолжает медленно расти; достигая толщины 25 нм за четыре года. [15]
Титан легко реагирует с кислородом при температуре 1200 ° C (2190 ° F) на воздухе и при 610 ° C (1130 ° F) в чистом кислороде с образованием диоксида титана. [7] В результате металл не может плавиться на открытом воздухе, так как он горит до того, как будет достигнута точка плавления. Плавление возможно только в инертной атмосфере или в вакууме. При 550 ° C (1022 ° F) он соединяется с хлором. [3] Он также реагирует с другими галогенами и поглощает водород. [4]
[7] В результате металл не может плавиться на открытом воздухе, так как он горит до того, как будет достигнута точка плавления. Плавление возможно только в инертной атмосфере или в вакууме. При 550 ° C (1022 ° F) он соединяется с хлором. [3] Он также реагирует с другими галогенами и поглощает водород. [4]
Титан — один из немногих элементов, который горит в чистом газообразном азоте, реагируя при температуре 800 ° C (1470 ° F) с образованием нитрида титана, который вызывает охрупчивание. [16]
Эксперименты показали, что природный титан становится радиоактивным после бомбардировки дейтронами, излучающими в основном позитроны и жесткие гамма-лучи. [3]
Соединения
Степень окисления +4 доминирует в химии титана, [17] , но соединения со степенью окисления +3 также распространены. [18] Из-за этой высокой степени окисления многие соединения титана имеют высокую степень ковалентной связи.
Звездчатые сапфиры и рубины получают свой астеризм из-за присутствующих в них примесей диоксида титана. [15] Титанаты — это соединения, содержащие диоксид титана. Титанат бария обладает пьезоэлектрическими свойствами, что позволяет использовать его в качестве преобразователя при взаимном преобразовании звука и электричества. [7] Сложные эфиры титана образуются в результате реакции спирта и тетрахлорида титана и используются для водонепроницаемости тканей. [7]
Нитрид титана (TiN), имеющий твердость, эквивалентную сапфиру и карборунду (9,0 по шкале Мооса), [19] часто используется для покрытия режущих инструментов, таких как сверла. [20] Он также находит применение в качестве декоративной отделки золотого цвета и в качестве барьерного металла при производстве полупроводников. [21]
Тетрахлорид титана (хлорид титана (IV), TiCl 4 , иногда называемый «щекоткой» [22] ) — это бесцветная жидкость, которая используется в качестве промежуточного продукта при производстве диоксида титана для красок. [23] Он широко используется в органической химии в качестве кислоты Льюиса, например, при альдольной конденсации Мукаямы. [24] Титан также образует низший хлорид, хлорид титана (III) (TiCl 3 ), который используется в качестве восстановителя. [25]
[23] Он широко используется в органической химии в качестве кислоты Льюиса, например, при альдольной конденсации Мукаямы. [24] Титан также образует низший хлорид, хлорид титана (III) (TiCl 3 ), который используется в качестве восстановителя. [25]
Дихлорид титаноцена является важным катализатором образования углерод-углеродной связи. Изопропоксид титана используется для эпоксидирования по Шарплесу. Другие соединения включают бромид титана (используемый в металлургии, суперсплавах и высокотемпературных электропроводках и покрытиях) и карбид титана (обнаруженный в высокотемпературных режущих инструментах и покрытиях). [4]
появление
Сумма значений не равна 100% из-за округления. Титан всегда связан с другими элементами в природе.Это девятый по распространенности элемент в земной коре (0,63% по массе) [27] и седьмой по распространенности металл. Он присутствует в большинстве магматических горных пород и образовавшихся из них отложениях (а также в живых существах и естественных водоемах). [2] [3] Из 801 типа магматических пород, проанализированных Геологической службой США, 784 содержали титан. [27] Его доля в почве составляет примерно 0,5–1,5%. [27]
[2] [3] Из 801 типа магматических пород, проанализированных Геологической службой США, 784 содержали титан. [27] Его доля в почве составляет примерно 0,5–1,5%. [27]
Он широко распространен и встречается в основном в минералах анатаз, брукит, ильменит, перовскит, рутил, титанит (сфен), а также во многих железных рудах. [15] Из этих минералов только рутил и ильменит имеют какое-либо экономическое значение, но даже их трудно найти в высоких концентрациях. Значительные месторождения титансодержащего ильменита существуют в Западной Австралии, Канаде, Китае, Индии, Мозамбике, Новой Зеландии, Норвегии и Украине. [15] Большое количество рутила также добывается в Северной Америке и Южной Африке и способствует ежегодному производству 90 000 тонн металла и 4,3 миллиона тонн диоксида титана. [15] Общие запасы титана оцениваются более чем в 600 миллионов тонн. [15]
Титан содержится в метеоритах и обнаружен на Солнце и в звездах M-типа; [3] самый холодный тип звезд с температурой поверхности 3200 ° C (5790 ° F). [28] Камни, принесенные с Луны во время миссии Аполлона-17, состоят на 12,1% из TiO 2 . [3] Он также содержится в угольной золе, растениях и даже в организме человека.
[28] Камни, принесенные с Луны во время миссии Аполлона-17, состоят на 12,1% из TiO 2 . [3] Он также содержится в угольной золе, растениях и даже в организме человека.
Изотопы
Основная статья: Изотопы титанаТитан природного происхождения состоит из 5 стабильных изотопов: 46 Ti, 47 Ti, 48 Ti, 49 Ti и 50 Ti, причем 48 Ti является наиболее распространенным (73,8% природного изобилие). Было охарактеризовано одиннадцать радиоизотопов, наиболее стабильным из которых является 44 Ti с периодом полураспада 63 года, 45 Ti с периодом полураспада 184,8 минут, 51 Ti с периодом полураспада 5.76 минут и 52 Ti с периодом полураспада 1,7 минуты. Все оставшиеся радиоактивные изотопы имеют период полураспада менее 33 секунд, а у большинства из них период полураспада составляет менее половины секунды. [8]
Изотопы титана имеют атомный вес от 39,99 ед. ( 40 Ti) до 57,966 ед. ( 58 Ti). Первичная мода распада перед наиболее распространенным стабильным изотопом 48 Ti — это захват электронов, а первичная мода после — бета-излучение.Первичные продукты распада перед 48 Ti — изотопы элемента 21 (скандий), а первичные продукты после — изотопы элемента 23 (ванадий). [8]
( 40 Ti) до 57,966 ед. ( 58 Ti). Первичная мода распада перед наиболее распространенным стабильным изотопом 48 Ti — это захват электронов, а первичная мода после — бета-излучение.Первичные продукты распада перед 48 Ti — изотопы элемента 21 (скандий), а первичные продукты после — изотопы элемента 23 (ванадий). [8]
История
Титан был обнаружен в составе минерала в Корнуолле, Соединенное Королевство, в 1791 году геологом-любителем и пастором Уильямом Грегором, тогдашним викарием прихода Крид. [29] Он обнаружил присутствие нового элемента в ильмените [4] , когда он нашел черный песок у ручья в соседнем округе Манаккан и заметил, что песок притягивается магнитом. [29] Анализ песка определил присутствие двух оксидов металлов; оксид железа (объясняющий притяжение к магниту) и 45,25% белого оксида металла, который он не смог идентифицировать. [27] Грегор, понимая, что неопознанный оксид содержит металл, который не соответствует свойствам какого-либо известного элемента, сообщил о своих открытиях Королевскому геологическому обществу Корнуолла и в немецком научном журнале Crell’s Annalen . [29]
[29]
Примерно в то же время Франц-Йозеф Мюллер фон Райхенштейн произвел подобное вещество, но не смог его идентифицировать. [4] Оксид был независимо открыт в 1795 году немецким химиком Мартином Генрихом Клапротом в рутиле из Венгрии. [29] Клапрот обнаружил, что он содержит новый элемент, и назвал его в честь титанов греческой мифологии. [28] Узнав о более раннем открытии Грегора, он получил образец манакканита и подтвердил, что он содержит титан.
Процессы, необходимые для извлечения титана из различных руд, трудоемки и дороги; его невозможно восстановить обычным способом путем нагревания в присутствии углерода, поскольку при этом образуется карбид титана. [29] Чистый металлический титан (99,9%) был впервые получен в 1910 году Мэтью А. Хантером в Политехническом институте Ренсселера путем нагревания TiCl 4 с натрием при 700–800 ° C в процессе Хантера. [3] Металлический титан не использовался за пределами лаборатории до 1932 года, когда Уильям Джастин Кролл доказал, что его можно получить путем восстановления тетрахлорида титана (TiCl 4 ) кальцием. [30] Восемь лет спустя он усовершенствовал этот процесс, используя магний и даже натрий в том, что стало известно как процесс Кролла. [30] Хотя исследования более эффективных и дешевых процессов продолжаются (например, FFC Cambridge), процесс Кролла все еще используется для коммерческого производства. [3] [4]
[30] Восемь лет спустя он усовершенствовал этот процесс, используя магний и даже натрий в том, что стало известно как процесс Кролла. [30] Хотя исследования более эффективных и дешевых процессов продолжаются (например, FFC Cambridge), процесс Кролла все еще используется для коммерческого производства. [3] [4]
Титан очень высокой чистоты производился в небольших количествах, когда в 1925 году Антон Эдуард ван Аркель и Ян Хендрик де Бур открыли процесс йодида, или кристаллического бруска, путем реакции с йодом и разложения образовавшихся паров над горячей нитью до чистого металла. [31]
В 1950-х и 1960-х годах Советский Союз впервые применил титан в военных и подводных целях (классы «Альфа» и «Майк») [32] в рамках программ, связанных с холодной войной. [33] Начиная с начала 1950-х годов, титан начал широко использоваться в целях военной авиации, особенно в высокопроизводительных реактивных самолетах, начиная с таких самолетов, как F100 Super Sabre и Lockheed A-12.
В США Министерство обороны осознало стратегическую важность металла [34] и поддержало первые попытки его коммерциализации. [35] В период «холодной войны» США считали титан стратегическим материалом.Правительство Южной Кореи, а большой запас титановой губки поддерживался Национальным центром оборонных запасов, который был окончательно исчерпан в 2005 году. [36] Сегодня крупнейший в мире производитель, российская ВСМПО-Ависма, по оценкам около 29% доли мирового рынка. [37]
В 2006 году Министерство обороны США выделило 5,7 млн долларов консорциуму из двух компаний на разработку нового процесса производства порошка металлического титана. Под воздействием тепла и давления порошок можно использовать для создания прочных и легких изделий, начиная от брони и заканчивая компонентами для аэрокосмической, транспортной и химической промышленности. [38]
Производство и изготовление
Титан (минеральный концентрат)
Обработка металлического титана происходит в 4 основных этапа: [39] восстановление титановой руды до «губки», пористой формы; плавление губки или губки плюс лигатуры с образованием слитка; первичное производство, при котором слиток превращается в обычные прокатные изделия, такие как заготовка, пруток, лист, лист, полоса и труба; вторичное изготовление готовых профилей из прокатных изделий.
Поскольку металл реагирует с кислородом при высоких температурах, он не может быть получен путем восстановления его диоксида. [9] Металлический титан, таким образом, коммерчески производится с помощью процесса Кролла, сложного и дорогостоящего периодического процесса. (Относительно высокая рыночная стоимость титана в основном связана с его переработкой, при которой жертвуется другой дорогой металл, магний. [40] ) В процессе Кролла оксид сначала превращается в хлорид посредством карбохлорирования, в результате чего газообразный хлор пропускается через раскаленный рутил или ильменит в присутствии углерода для получения TiCl 4 .Его конденсируют и очищают фракционной перегонкой, а затем восстанавливают расплавленным магнием при 800 ° C в атмосфере аргона. [7]
Недавно разработанный метод, Кембриджский процесс FFC, [41] , может в конечном итоге заменить процесс Кролла. В этом методе используется порошок диоксида титана (который представляет собой очищенную форму рутила) в качестве сырья для получения конечного продукта, который представляет собой порошок или губку. Если используются порошки смешанных оксидов, продукт представляет собой сплав, производимый по гораздо более низкой цене, чем при традиционном многоступенчатом процессе плавления.Кембриджский процесс FFC может сделать титан менее редким и дорогим материалом для аэрокосмической промышленности и рынка предметов роскоши, и его можно увидеть во многих продуктах, которые в настоящее время производятся с использованием алюминия и специальных сортов стали.
Если используются порошки смешанных оксидов, продукт представляет собой сплав, производимый по гораздо более низкой цене, чем при традиционном многоступенчатом процессе плавления.Кембриджский процесс FFC может сделать титан менее редким и дорогим материалом для аэрокосмической промышленности и рынка предметов роскоши, и его можно увидеть во многих продуктах, которые в настоящее время производятся с использованием алюминия и специальных сортов стали.
Обычные титановые сплавы получают восстановлением. Например, восстанавливаются купротитан (восстанавливается рутил с добавлением меди), железоуглеродистый титан (ильменит, восстановленный коксом в электрической печи) и манганотитан (рутил с оксидами марганца или марганца). [42]
- 2 FeTiO 3 + 7 Cl 2 + 6 C → 2 TiCl 4 + 2 FeCl 3 + 6 CO (900 ° C)
- TiCl 4 + 2 Mg → 2 MgCl 2 + Ti (1100 ° C)
В настоящее время обозначено и используется около 50 марок титана и титановых сплавов, хотя коммерчески доступно только несколько десятков. [43] ASTM International признает 31 марку металлического титана и сплавов, из которых марки с 1 по 4 являются коммерчески чистыми (нелегированными).Эти четыре отличаются различной степенью прочности на разрыв в зависимости от содержания кислорода, причем степень 1 является наиболее пластичной (наименьшая прочность на разрыв при содержании кислорода 0,18%), а степень 4 наименьшей (наибольшая прочность на разрыв с содержание кислорода 0,40%). [15] Остальные марки представляют собой сплавы, каждая из которых предназначена для определенных целей, будь то пластичность, прочность, твердость, удельное электрическое сопротивление, сопротивление ползучести, сопротивление коррозии в определенных средах или их сочетание. [44]
[43] ASTM International признает 31 марку металлического титана и сплавов, из которых марки с 1 по 4 являются коммерчески чистыми (нелегированными).Эти четыре отличаются различной степенью прочности на разрыв в зависимости от содержания кислорода, причем степень 1 является наиболее пластичной (наименьшая прочность на разрыв при содержании кислорода 0,18%), а степень 4 наименьшей (наибольшая прочность на разрыв с содержание кислорода 0,40%). [15] Остальные марки представляют собой сплавы, каждая из которых предназначена для определенных целей, будь то пластичность, прочность, твердость, удельное электрическое сопротивление, сопротивление ползучести, сопротивление коррозии в определенных средах или их сочетание. [44]
Сплавы, на которые распространяется ASTM, и другие сплавы также производятся в соответствии с аэрокосмическими и военными спецификациями (SAE-AMS, MIL-T), стандартами ISO и национальными спецификациями, а также собственными спецификациями конечных пользователей для аэрокосмической, военной и др. медицинские и промышленные применения. [45]
медицинские и промышленные применения. [45]
С точки зрения производства, вся сварка титана должна выполняться в инертной атмосфере аргона или гелия, чтобы защитить его от загрязнения атмосферными газами, такими как кислород, азот или водород. [11] Загрязнение вызовет ряд условий, например охрупчивание, которое ухудшит целостность сварных швов сборки и приведет к разрушению соединения. Промышленно чистый плоский продукт (лист, плита) можно легко формовать, но при обработке необходимо учитывать тот факт, что металл имеет «память» и имеет тенденцию к упругому возврату. Особенно это касается некоторых высокопрочных сплавов. [46] [47] Титан нельзя паять без предварительного покрытия его металлом, который поддается пайке. [48] Металл можно обрабатывать на том же оборудовании и с помощью тех же процессов, что и нержавеющую сталь. [11]
Приложения
Цилиндр титановый, сорт
«Grade 2».Титан используется в стали в качестве легирующего элемента (ферротитан) для уменьшения размера зерна и в качестве раскислителя, а также в нержавеющей стали для уменьшения содержания углерода. [2] Титан часто легируют алюминием (для уменьшения размера зерна), ванадием, медью (для упрочнения), железом, марганцем, молибденом и другими металлами. [49] Применения для изделий из титана (лист, лист, пруток, проволока, поковки, отливки) можно найти на промышленных, аэрокосмических, развлекательных и развивающихся рынках. Порошок титана используется в пиротехнике как источник ярко горящих частиц.
Пигменты, добавки и покрытия
Около 95% титановой руды, добываемой на Земле, предназначено для переработки в диоксид титана (TiO 2 ), интенсивно белый перманентный пигмент, используемый в красках, бумаге, зубной пасте и пластмассах. [50] Он также используется в цементе, драгоценных камнях, в качестве оптического глушителя бумаги, [51] и упрочняющего агента в графитовых композитных удилищах и клюшках для гольфа.
TiO 2 химически инертен, устойчив к выцветанию на солнечном свете и очень непрозрачен: это позволяет ему придавать чистый и блестящий белый цвет коричневым или серым химическим веществам, которые составляют большинство бытовых пластиков. [4] В природе это соединение содержится в минералах анатаз, брукит и рутил. [2] Краска, изготовленная из диоксида титана, хорошо переносит суровые температуры и стойкость к морской среде. [4] Чистый диоксид титана имеет очень высокий показатель преломления и оптическую дисперсию выше, чем у алмаза. [3] Диоксид титана не только является очень важным пигментом, но также используется в солнцезащитных кремах, поскольку он сам по себе защищает кожу. [9] В последнее время оксид титана стал использоваться в очистителях воздуха (в качестве фильтрующего покрытия) или в пленке, используемой для покрытия окон зданий, чтобы оксид титана подвергался воздействию ультрафиолетового света (солнечного или искусственного) и влаги в воздухе образуются реактивные окислительно-восстановительные частицы, такие как гидроксильные радикалы, которые могут очищать воздух или поддерживать чистоту оконных поверхностей. [52]
[52]
Аэрокосмическая и морская промышленность
Благодаря высокому отношению прочности на разрыв к плотности, [7] , высокой коррозионной стойкости, [3] , устойчивости к усталости, высокой трещиностойкости, [53] и способности выдерживать умеренно высокие температуры без ползучести, титановые сплавы являются используется в самолетах, броне, кораблях, космических кораблях и ракетах. [3] [4] Для этих применений титан, легированный алюминием, ванадием и другими элементами, используется для различных компонентов, включая критически важные структурные детали, противопожарные стенки, шасси, выхлопные каналы (вертолеты) и гидравлические системы. .Фактически, около двух третей всего производимого титана используется в авиационных двигателях и каркасах. [54] SR-71 «Blackbird» был одним из первых самолетов, в конструкции которого широко использовался титан, что открыло дорогу его использованию в современных военных и коммерческих самолетах. Приблизительно 59 метрических тонн (130 000 фунтов) используются в Boeing 777, 45 в Boeing 747, 18 в Boeing 737, 32 в Airbus A340, 18 в Airbus A330 и 12 в Airbus A320. Airbus A380 может использовать 146 тонн, в том числе около 26 тонн в двигателях. [55] В двигателях титан используется для изготовления роторов, лопаток компрессоров, компонентов гидравлической системы и гондол. Титановый сплав 6АЛ-4В составляет почти 50% всех сплавов, используемых в авиастроении. [56]
Приблизительно 59 метрических тонн (130 000 фунтов) используются в Boeing 777, 45 в Boeing 747, 18 в Boeing 737, 32 в Airbus A340, 18 в Airbus A330 и 12 в Airbus A320. Airbus A380 может использовать 146 тонн, в том числе около 26 тонн в двигателях. [55] В двигателях титан используется для изготовления роторов, лопаток компрессоров, компонентов гидравлической системы и гондол. Титановый сплав 6АЛ-4В составляет почти 50% всех сплавов, используемых в авиастроении. [56]
Из-за высокой коррозионной стойкости к морской воде титан используется для изготовления гребных валов и оснастки, а также в теплообменниках опреснительных установок; [3] в нагревателях-охладителях для аквариумов с соленой водой, леске и поводке, а также для водолазных ножей.Титан используется для производства корпусов и других компонентов морских устройств наблюдения и мониторинга для научного и военного использования. В бывшем Советском Союзе были разработаны технологии изготовления подводных лодок в основном из титана. [57]
[57]
Промышленное
Сварные титановые трубы и технологическое оборудование (теплообменники, резервуары, технологические сосуды, клапаны) используются в химической и нефтехимической промышленности в первую очередь для обеспечения устойчивости к коррозии. Определенные сплавы используются в скважинной и никелевой гидрометаллургии из-за их высокой прочности (например,g .: титановый сплав Beta C), коррозионной стойкости или их комбинации. В целлюлозно-бумажной промышленности титан используется в технологическом оборудовании, подверженном воздействию агрессивных сред, таких как гипохлорит натрия или влажный газообразный хлор (на отбеливателе). [58] Другие области применения: ультразвуковая сварка, пайка волной припоя, [59] и мишени для распыления. [60]
Тетрахлорид титана (TiCl 4 ), бесцветная жидкость, играет важную роль в качестве промежуточного продукта в процессе производства TiO 2 , а также используется для производства катализатора Циглера-Натта, а также для иридирования стекла, поскольку оно дымится.







