Химическое и гальваническое меднение: состав и подготовка
Современная техника выдвигает жесткие требования к характеристикам конструктивных элементов, во многих случаях эти задачи решает химическое меднение. Использование специальных покрытий поверхностей деталей выгодно экономически, так как гальваническое меднение позволяет понизить металлоемкость изделий из дорогостоящих металлов.
Физико-механические характеристики меди и сферы использования меднения
Плотность меди 8,96 г/см3, атомная масса 693,54, удельное электрическое сопротивление 1,68×10-8 Ом×м, температура плавления +1083°С. На открытом воздухе в присутствии агрессивных химических соединении медь окисляется, при контакте с сернистыми соединениями покрывается пленкой сульфида меди темно-коричневого или серого оттенков. Под влиянием углекислоты и влаги пленка приобретает зеленый цвет, верхний слой состоит из гидрокарбонатов. Медь легко растворяется в растворе азотной кислоты, разбавленная серная кислота на химическое меднение негативного влияния почти не оказывает. Но наличие кислорода увеличивает скорость протекания химических реакций. При наличии открытых пор в покрытии образуется гальванопара, что нужно учитывать при меднении. Железо в этом случае является анодом, коррозионные процессы протекают очень интенсивно.
В связи с такими особенностями, процесс меднения в большинстве случаев должен завершаться дополнительной обработкой поверхностей. Покрытия шлифуются или полируются до зеркального блеска. Медь имеет высокую адгезию с различными металлами: алюминий, серебро, цинк, никель, свинец, хром и т. д. В связи с этими особенностями химическое меднение часто используется для создания подслоя при серебрении, никелировании, хромировании поверхностей деталей. Меднение получило широкое распространение в качестве метода эффективной защиты отдельных участков деталей от появления эффекта науглероживании при процессе цементации. В зависимости от назначения деталей или изделий гальваническое нанесение меди может иметь следующую толщину:

Толщина слоя меди на поверхности обрабатываемых деталей
Сравнительные показатели растворов
В процессе меднения используется большое количество специальных технологических растворов, разделяемых на две большие группы:
- Простой кислый электролит. Из простых применяется фторборатный, кремнефторидный, сульфатный, хлоридный и сульфамидный раствор.
- Комплексный электролит. Преимущественно щелочные, медь присутствует как положительно или отрицательно заряженные комплексные ионы.
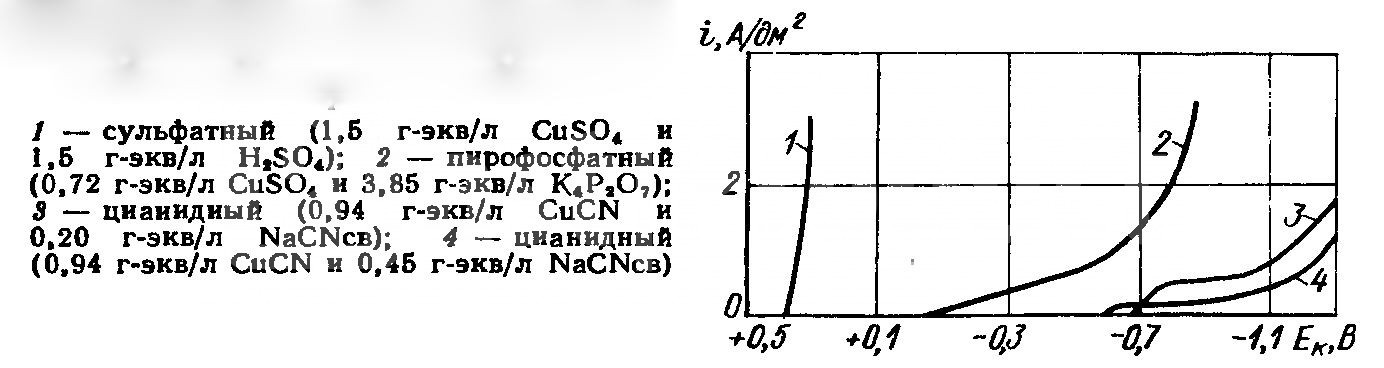
График поляризационных кривых осаждения меди из различных типов электролитов
Процесс осаждения в кислых электролитах происходит при высокой плотности по току, они устойчивы, просты по химическому составу. Главными составляющими являются соответствующие кислоты и соли, осадки меди из них достаточно плотны и имеют крупнокристаллическую структуру. Недостатки – непосредственное меднение стали, цинковых сплавов и иных металлов происходит с более низким отрицательным потенциалом, чем медь.
Обработка деталей в комплексных электролитах выполняется за счет комплексных ионов, для них требуется высокая катодная поляризация. Выход по току меньше, что способствует более равномерному осаждению, структура мелкокристаллическая. Используются пирофосфатные, цианидные, аммонийные, триполифосфатные, цитратные и другие растворы.
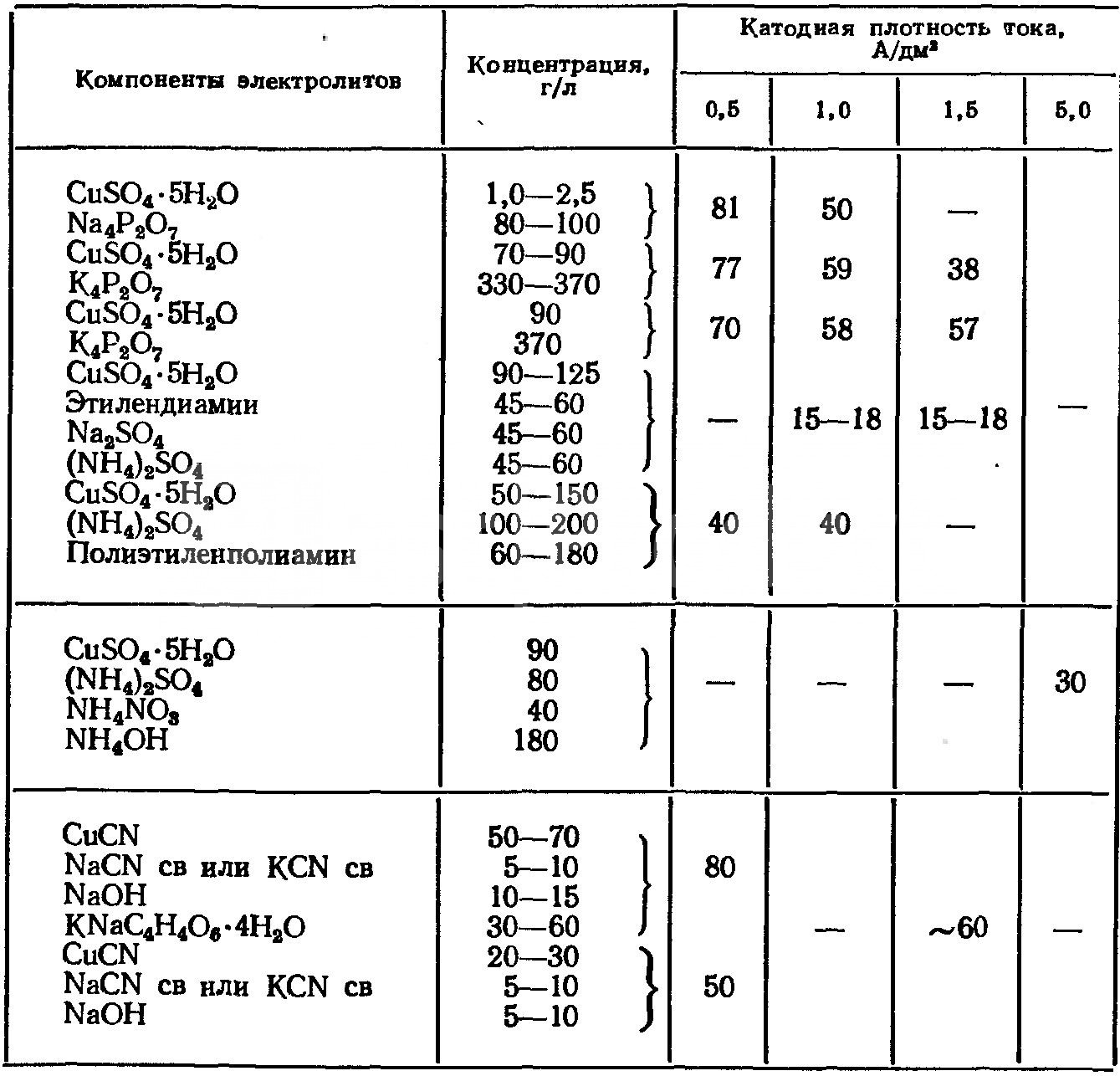
Способность рассеивания электролитов для меднения
Простые кислые составы
- Сульфатные. Главные компоненты серная кислота и сульфат меди. Сернокислое соединение отличается невысокой электропроводимостью, для повышения параметра добавляется серная кислота. Выход меди по току достигает 100%, на катоде не выделяется водород. За счет повышения концентрации кислоты уменьшается растворимость сульфата, что понижает верхний предел максимально допустимой плотности тока.

Влияние содержания серной кислоты на электропроводность электролита
При перемешивании увеличивается концентрация медных ионов на катодном слое. При повышении температуры возрастает растворимость сульфата меди, электролит повышает кислотность, что приводит к получению мелкокристаллических осадков.
Для улучшения катодной поляризации в электролит добавляются поверхностно активные вещества. Дополнительно они уменьшают образование наростов на острых краях.

Режимы и состав сульфатных электролитов для меднения
Для образования блестящего покрытия используются аноды АМФ, не допускающие образование шлама, или аноды из особо чистой рафинированной меди.
Влияние концентрации меди на плотность тока с перемешиванием (1) и без перемешивания (2). Электролит фторборатный.
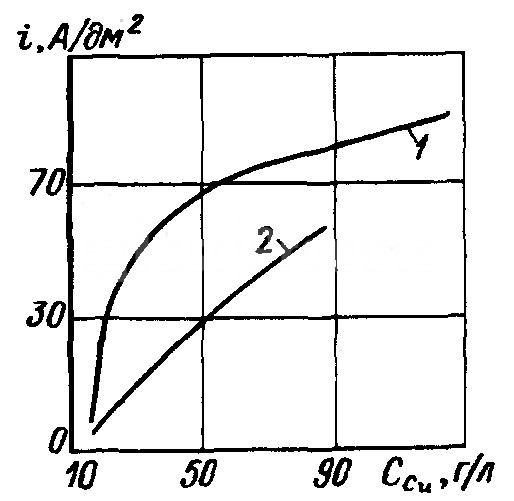
Электролит фторборатный.
Для недопущения попадания шлама аноды помещаются в чехлы, изготовленные из кислотоустойчивого материала, дополнительно раствор постоянно фильтруется.
- Фторборатные. Отличаются высокой устойчивостью, гальваническое нанесение получается плотным и мелкокристаллическим, рассеивающие показатели такие же, как при сульфатном меднении. За счет большой растворимости увеличивается плотность тока, осаждать медь непосредственно на детали нельзя.

Состав и режим работы фторборатных электролитов
При непрерывном перемешивании допускается повышать плотность тока. Контроль технологически параметров меднения осуществляется измерением кислотности раствора. Для повышения качества меднения используется карбонат натрия, для понижения медный купорос.
- Нитратные. Электролит используется при гальванопластике, обеспечивает повышенное качество осадка.
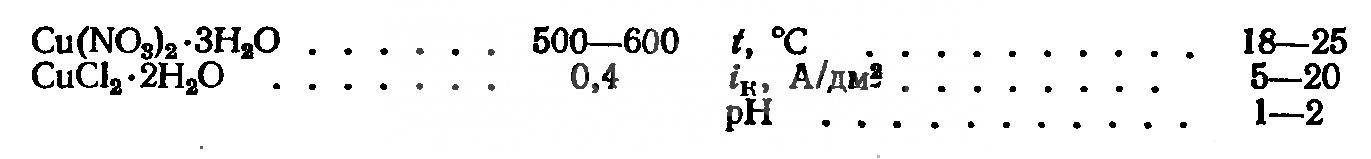
Режимы и состав нитратных электролитов
Комплексные электролиты
- Цианидные. Условия обработки значительно отличаются от осаждения из кислых, в них медь существует в виде комплексных ионов, что заметно понижает ее активность. Увеличение плотности тока принуждает катодный потенциал резко смещаться в поле отрицательных значений. Но процесс меднения нельзя производить при увеличенной плотности тока в связи с тем, что выход меди может падать до нуля. Главными компонентами раствора являются свободный цианид натрия и комплексный цианид калия. Во время работы содержание меди понижается из-за недостаточной их растворимости.
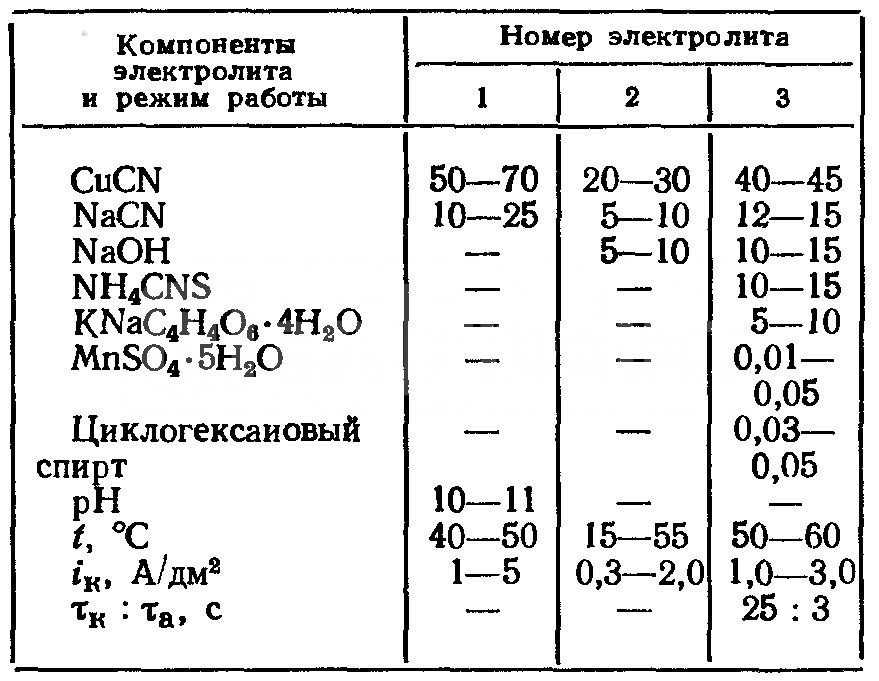
Режим и состав цианидных электролитов для меднения
- Пирофосфатные. Медные осадки имеют мелкокристаллическую структуру, гладкие, блестящие или полублестящие. Для улучшения качества обработки и повышения катодной и анодной плотностей может добавляться медный купорос. Катодный потенциал в пирофосфатных растворах имеет более отрицательные параметры, чем у кислотных.

Режим и состав пирофосфатных электролитов
- Этилендиаминовые. Процесс меднения может осуществляться непосредственно по поверхности стали, при низких плотностях тока катодная поляризация достигает больших значений. Рассеивающие характеристики выше, чем у сульфатных, но ниже, чем имеет цианидный раствор.
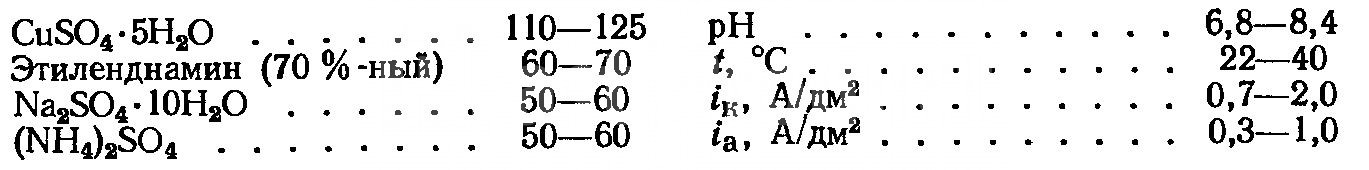
Режим и состав этилендиаминовых электролитов
Загрузка и выгрузка деталей должна выполняться при минимальной силе тока, в первые 40–50 секунд дается толчок тока, в три раза превышающий рабочие значения меднения.
- Полиэтиленполиаминовые. Во время обработки деталей потенциалы смещаются в поле отрицательных значений, электролит применяется вместо цианидных.

Режим работы и составы полиэтиленполиаминовых электролитов
- Аммонийные. В состав входит аммиак, сульфат аммония и сульфат меди. При невысоких плотностях тока уменьшается выход по току, улучшение меднения осуществляется за счет добавления нитрата аммония. Осадки равномерные по толщине, плотные и полублестящие.
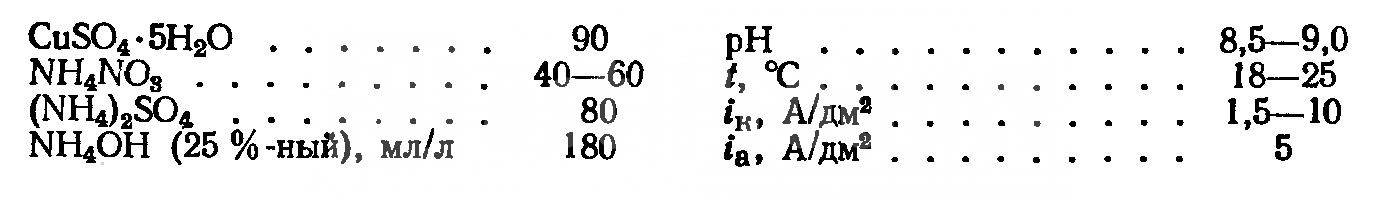
Режимы работы и состав аммонийного электролита
Без специальной обработки поверхностей медные осадки имеют недостаточную адгезию, причина – пассивирование стали раствором аммиака. Улучшение параметров покрытия достигается введением в раствор нитрата меди.
Устройство ванны медненияЛинейные параметры и конструктивные особенности должны отвечать требованиям ГОСТ 23738-85. Гальваническая ванна изготавливается из модифицированных особо устойчивых пластиков, конкретные марки подбираются с учетом параметров технологических процессов.
Ванна без кармана. Наиболее простая конструкция, применяется как в отдельности, так и на производственных линиях.
Ванна без кармана
Ванна с карманом. Обработка может выполняться с одновременными процессами удаления верхнего загрязненного слоя электролита.
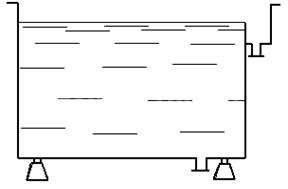
Ванна с карманом
Конкретный выбор ванны меднения осуществляется в зависимости от особенностей предприятия, характеристик подлежащих меднению деталей и общих производственных мощностей.
Во время проектирования рассчитываются максимальные нагрузки с учетом объема раствора, длина, высота и ширина может изменяться по желанию заказчиков. При необходимости на ванны меднения устанавливается дополнительное оборудование и водопроводная арматура. За счет специальных механизмов улучшается качество процесса меднения. Используемые пластики адаптируются к химическому составу электролита и температурным режимам меднения.
Механическая подготовка поверхностей
Перед меднением с поверхности должна удаляться окалина, заусеницы и раковины. Качество обработки регламентируется положениями действующего ГОСТа 9.301-86. Конкретные параметры шероховатости устанавливаются в зависимости от назначения покрытия. После механической обработки деталей с поверхности должны быть удалены все дефекты, оказывающие негативное влияние на качество меднения. В обязательном порядке удаляется техническая смазка и эмульсия, металлическая стружка, продукты коррозионных процессов и пыль.
Подготовка к меднению производится при следующих технологических операциях:
- Шлифование. Верхний слой деталей снимается абразивными элементами, может быть тонким, декоративным или грубым.
- Полирование. Во время операции сглаживаются мельчайшие выступы, поверхность блестящая зеркальная.
- Крацевание. Для очистки поверхностей применяются металлические щетки.
- Галтовка. Детали обкатываются в специальных колоколах.
- Химическое и электрохимическое обезжиривание. Для обработки используют органические и неорганические растворы.
От качества предварительной подготовки поверхностей во многом зависит процесс меднения и физические показатели осадков.
Меднение в домашних условиях — гальваника медью: сталь, вольфрам
Содержание статьи:
- Гальваника медью в домашних условиях: общие сведения
- Необходимые инструменты
- Подготовка материала
- Как правильно подготовить электролит
- Подготовка материала для меднения
- Техника безопасности
- Гальваника в домашних условиях: меднение
- Метод погружения
- Покрытие без погружения
- Особенности гальванопластики
Меднение в домашних условиях – это технологический процесс, позволяющий наносить на металл, а также другие материалы (вольфрам, сталь) слой меди толщиной от 1 до 300 мкм. Покрытие медным слоем обеспечивает хорошую адгезию металла и при увеличении толщины покрытий придает блеск изделиям, устраняет небольшие дефекты, позволяет создавать копии вещи. Удивительно, но все это можно делать и самим. Сегодня мы расскажем, как осуществить меднение металла в домашних условиях.
Гальваника медью в домашних условиях: общие сведения
С технической точки зрения обработка – это электрохимический процесс. В процессе всегда есть два «участника» анод+электролит (источник металла) и деталь.
Технология гальваники медью в домашних условиях достаточно проста. Заключается она в том, что за счет электролита и проводимого через него тока выделяются атомы металла. Они оседают на поверхности, образуя медное покрытие.
Среди основных этапов гальванического меднения в домашних условиях:
- Подготовка поверхности (механическая и химическая).
- Нанесение подслойного покрытия (если необходимо)
- Меднение в соответствующем исходному металлу электролите.
Для декоративного гальванического меднения подойдут электролиты матового и блестящего меднения. После нанесения слоя, можно обработать поверхность в электролитах серебра, золота никеля и т.д.
Необходимые инструменты для меднения в домашних условиях
«Ингредиенты», без которых меднение не состоится, но которые реально подготовить в домашних условиях. Наши гальваники утверждают, что прежде всего, нужны:
- Источник постоянного тока.Выбирается в зависимости от размера изделия.
- Аноды. Анодные пластины выполняют несколько функций. В первую очередь, они подводят в электролит ток, во-вторых, они возмещают убыль металла, уходящего на покрытие изделия.
- Рабочий электролит. Кислотный, щелочной или пирофосфорный раствор. Состав электролита выбирается в зависимости от исходного металла. Необходимо помнить, что любой электролит не универсален и подойдет не для всех работ.
Подготовка материала
Как правильно подготовить простой электролит меднения
Стоит отметить, что гальваника в домашних условиях медью сложна, потому что химические реактивы найти непросто. Компании, реализующие подобные продукты, не продают их без специальных документов. Но вы можете сделать все сами.
Электролит в домашних условиях возможно приготовить только при условии точного соблюдения рецептуры. В состав простейшего электролита входит:
- Дистиллированная вода (или бидистиллят).
- Медный купорос.
- Соляная или другая кислота.
Готовый раствор имеет яркий синий цвет, запаха нет. Допускается наличие некоторого осадка. Важно соблюдать все меры безопасности с химическими реактивами, особенно в домашних условиях: защита рук и глаз в первую очередь. Одежду, на которую случайно мог пролиться раствор, – лучше перевести в разряд дачной.
Хранить такую жидкость лучше в стеклянных бутылках или пластиковых канистрах, а также обязательно указать дату розлива и название раствора. Правильное хранение компонентов избавит вас от возможных проблем. Приготовление электролита должно проходить в чистой пластмассовой или стеклянной посуде.
Подготовка материала для меднения в домашних условиях
Химическое меднение — это альтернатива электрохимическому способу, но не всегда может его заменить. В этом процессе важно тщательно подготовить деталь, бесследно устранив царапины, загрязнения, сколы и т.д. Для того, чтобы обезжирить вещь, можно пускать в ход и чистые растворители, и обезжиривающие растворы.
При этом универсального метода нет – разные виды металла подвергаются очистке по-разному:
- Сталь. Обезжиривать сталь можно раствором, содержащим едкий натрий и едкий калий при 70-90 градусов по Цельсию. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой.
- Медь и сплавы. Обезжиривание осуществляется едким натрием, нагретым предварительно до 40°, около 10 минут.
- Чугун. Для процесса обезжиривания нужен раствор, содержащий едкий натрий, жидкое стекло, карбонат натрия и фосфат натрия при нагревании до 90°.
- Вольфрам. Меднение вольфрама в домашних условиях начинается с чистки предмета от грязи и прочих дефектов наждачной бумагой.
Техника безопасности при меднении в домашних условиях
Несмотря на возможность гальваники в домашних условиях (меднения), процесс остается опасным. В любом гальваническом процессе задействованы токсичные вещества, способные сильно нагреваться. Поэтому нужно неукоснительно соблюдать меры предосторожности.
Первое правило гальваники медью в домашних условиях – работайте только в нежилом, хорошо проветриваемом помещении. Подойдут такие места, как мастерская или гараж. Второе правило – применяемое оборудование нужно заземлить. Третье – это соблюдение личной безопасности.
Для обеспечения собственной защиты при меднении в домашних условиях нужно:
- Постоянно быть в респираторе, чтобы обезопасить дыхательные пути. лучше всего использовать вытяжку.
- Защитить руки прочными прорезиненными перчатками.
- Надеть специальную форму или клеенчатый фартук, противоожоговую обувь.
- Не забыть очки для безопасности зрительных органов.
- Не приносить в помещение еду и питье.
Перед меднением лучше заранее озаботиться прочтением специализированной литературы по данной теме. Желательно посоветоваться со специалистами данного профиля.
Гальваника в домашних условиях: меднение
Почему в гальванике столь востребована именно медь? Она имеет высокую адгезию (иными словами – сцепление) к самым разным материалам. Это значит, что она превосходно держится на изделиях из стали, вольфрама, не отлетая и не скалываясь.
Медь – красивый яркий металл, внешне напоминает самородки розово-красного оттенка. Материал проводит не только тепло, но и электрический ток – отсюда и высокий спрос в сфере электротехники и приборостроении. Однако чистую медь найти сложно. Чаще она поставляется с различными примесями.
Медные покрытия:
- Отличаются малым сопротивлением, что используется в электротехнике
- Скрывает мелкие недочеты поверхности.
- Быстро окисляется, что используют для получения эффекта «антик».
Технологий меднения существует две. Одна происходит путем погружения изделия в раствор электролиты (с подачей тока или без). Второй же способ – это метод селективного нанесения покрытия без погружения в раствор. Рассмотрим оба.
Метод погружения
В домашних условиях поверхность, подвергаемую гальванике, следует скрупулезно образом обработать. Например, наждачной бумагой и щеточкой. После обязательно обезжирьте деталь и промойте.
Дальше:
- Анодную пластину (можно две) помещают в емкость, которую будем называть ванной. На аноды замыкают положительную клемму.
- Между анодами на любом удобном проводнике подвешивается деталь, к ней подводят отрицательный полюс от блока питания.
- Готовый раствор вливается в ванночку – при этом уровень покрытия должен быть выше, чем расположена деталь.
- После подключения электродов к источнику тока выставляют рабочий ток. Это примерно 1 А/кв.дм. покрытия.
Продолжительность работы зависит от необходимой толщины слоя, обычно от 5 минут.
Покрытие без погружения
Данный способ меднения имеет ограничения – чаще всего он подходит для реставрации поверхности. Таким способом можно нанести только небольшую толщину металла. Нет смысла покрывать таким методом изделия, которые можно меднить в ванне.
Порядок действий при гальваническом меднении в домашних условиях:
- Готовят «тампон» для нанесения покрытия. Берут медный проводник и наматывают кусок искусственной ткани (полиэстер подойдет).
- Противоположный конец проводника подсоединяют к положительной клемме источника напряжения.
- Электролитным раствором наполняют емкость – так удобнее окунать карандаш.
- Деталь аккуратно очищают и обезжиривают, а потом помещают в пустую ванночку. Там изделие подсоединяется к отрицательной клемме.
- Тампон смачивают в растворе. Затем им проводят по поверхности изделия, закрашивая ее постепенно.
Процесс длится до полного покрытия медным слоем изделия.
Особенности гальванопластики в домашних условиях
Гальванопластика — это процесс нанесения меди на проводящую или непроводящую поверхность изделия с последующим снятием покрытия с негативной матрицы. Таким образом можно получить множество очень точных копий с одного изделия. При этом, есть условие: наращивание меди толщиной не менее 200 мкм, чтобы изделие получилось прочным.
Важно учесть, что, если поверхность изделия не имеет свойств проводника, то потребуется больше усилий – а именно, особое предварительное покрытие графитом, серебром или медью. Основным металлом для осуществления гальванопластики считается медь, но можно выращивать матрицы из серебра чистотой 9999.
Обучение гальванике
Можно сделать вывод, что меднение сегодня — это один из наиболее актуальных гальванотехнических процессов, обучиться которому может каждый. Компания «6 микрон» проводит обучение по направлению «Гальваника» для всех желающих! Вы сможете выбрать удобную для Вас программу обучения, которая лучше всего подойдет для гальваники в домашних условиях и не только. Все интересующие вопросы можно задать по телефону или по электронной почте, наши технологи проконсультируют по курсам для обучения.
Видео руководство по меднению деталей в домашних условиях:
Подробности Вы можете узнать по ссылке://6mkm.ru/uslugi/obuchenie-komplekti-dlya-prodazhi/
Автор материалов:Гордиенко Анастасия Вадимовна
Должность: главный технолог ООО «6 микрон»
Образование: высшее
Опыт работы в гальванике: 11 лет
Задать свой вопрос
3.9 / 5 ( 127 голосов )
Смотрите также:
10000
С ценами на услуги по гальваническому меднению можно ознакомиться в конце этой статьи. Процесс гальванического меднения в большинстве случаев является…
10000
Медь – один из первых материалов, которые смог «приручить» человек. Открытый около четырех тысяч лет назад, этот материал сегодня сохраняет…
10000
Медные покрытия редко используются как самостоятельные – в основном они нужны для промежуточных слоев перед никелированием, хромированием, серебрением. При этом…
Механизм гальванического меднения (теория и технология нанесения)
• Заказать ГАЛЬВАНИЧЕСКОЕ МЕДНЕНИЕ стали
• Заказать ГАЛЬВАНИЧЕСКОЕ МЕДНЕНИЕ нержавейки
• Заказать ГАЛЬВАНИЧЕСКОЕ МЕДНЕНИЕ алюминия
• Заказать ГАЛЬВАНИЧЕСКОЕ МЕДНЕНИЕ ЦАМ
• Заказать ГАЛЬВАНИЧЕСКОЕ МЕДНЕНИЕ диэлектриков
1. Что такое медь?
Медь — металл розового цвета с атомной массой 63,5, плотностью 8,9 г/см3, температурой плавления 10830С, удельным электросопротивлением 0,017 Ом мм. Медь пластична, твердость медных покрытий 2500-3000 МПа. Медь интенсивно растворяется в аэрированных аммиачных и цианидных растворах, азотной кислоте, медленнее — в хромовой, слабо — в серной и почти не взаимодействует с соляной кислотой. На воздухе медь легко реагирует с влагой, углекислыми и сернистыми соединениями, окисляется и темнеет. Стандартный потенциал меди по отношению к ее одновалентным нонам +0,52 В, двухвалентным ионам +0,34 В.
В жестких условиях эксплуатации медь и ее сплавы не должны контактировать с хромом, оловом, сталями, цинком, кадмием, алюминием и магнием.
Медные покрытия широко применяются в основном в качестве подслоя при нанесении многослойных покрытиях, а также для улучшения пайки, создания электропроводных слоёв, местной защиты стальных деталей при цементации.
2. Кинетика процесса меднения.
Для электролитического осаждения меди разработано большое количество электролитов, которые, обычно, разделяют на две группы: кислые и щелочные.
Катодные поляризационные кривые для некоторых из них приведены на рисунке 1.
Рисунок 1 — Катодные поляризационные кривые при меднении из электролитов: 1 — сульфатный; 2 — пирофосфатный; 3 — цианидный ; 4 -цианидный с повышенным содержанием свободных цианидов.
2.1 Процессы в кислых электролитах меднения.
К кислым электролитам относятся сульфатные и фторборатные электролиты. Их основные достоинства - простота состава и устойчивость в эксплуатации, но они обладают низкой рассеивающей способностью. Также из них невозможно непосредственно меднить сталь из-за выпадения контактной меди, а, следовательно, плохое сцепление со сталью слоя меди. Вследствие этого меднение осуществляется после предварительного осаждения медного слоя (3-4 мкм) из щелочных электролитов или после осаждения никелевого слоя (3-5 мкм).
Из кислых электролитов наиболее распространен сульфатный электролит. Основными компонентами сульфатных электролитов являются сульфат меди и серная кислота. Электропроводность нейтральных растворов сульфата меди невелика, поэтому в них добавляют серную кислоту, которая значительно повышает электропроводность растворов температуры перемешивания.
Предполагается, что на катоде разряд двухвалентных ионов меди протекает в две стадии:
Cu2++ e → Cu+
Cu+ + e → Cu
Замедленной стадией является первая реакция. Доля каждой стадии в общей кинетике меднения зависит от состава электролита и режима электролиза: плотности тока, температуры, перемешивания.
Выход меди по току около 100 %, так как выделения водорода на катоде не происходит, поскольку потенциалы выделения меди имеют более положительные значения, чем потенциалы выделения водорода.
Повышение кислотности электролита способствует уменьшению растворимости сульфата меди, что приводит к снижению верхнего предела допустимой плотности тока. Для увеличения концентрации ионов меди в катодном слое применяют перемешивание. В этом случае кислотность электролитов можно увеличивать. Чем интенсивнее перемешивание, тем выше может быть содержание серной кислоты. Повышение температуры способствует увеличению растворимости сульфата меди: при 25 °С — 23,05 г CuSO4 на 100 г воды; при 100 °С — 73,6 г. Повышенная кислотность способствует получению более мелкокристаллических осадков.
Вблизи анодов наряду с ионами Cu2+ в растворе могут находиться в незначительном количестве ионы одновалентной меди, образующиеся в результате протекания реакции:
Cu + Cu2+↔ 2Cu+
При накоплении в растворе
ионов Cu+ равновесие будет сдвигаться влево, и металлическая медь
будет выпадать в виде осадка.
При недостаточной кислотности раствора сульфат одновалентной меди будет гидролизоваться с образованием Сu(ОН)2 или СuО2
Cu2SO4 + H2O ↔ Cu2O + H2SO4
В результате в электролите будут взвешенные частицы металлической меди и оксида меди, которые, включаясь в катодный осадок, делают его темным, шероховатым, а иногда - рыхлым.
Присутствие серной кислоты способствует протеканию реакций окисления одновалентной меди:
Cu2SO4 + H2SO4
+ 1/2О2→ 2CuSO4 + Н2О
Cu2O + 2H2SO4 + 1/2O2→ 2CuSO4
+ 2H2O
Таким образом, серная кислота прежде всего нужна для предупреждения накопления ионов Cu+ и гидролиза ее солей.
В сульфатные электролиты иногда вводят поверхностно-активные вещества. Эти вещества вводят для повышения катодной поляризации, что способствует получению более мелкозернистых плотных, иногда блестящих, осадков. Благоприятное действие этих добавок сказывается в том, что они предупреждают образование наростов на краях и выступающих частях деталей. Наилучшими добавками являются декстрин (не более 1 г/л) и фенол или его сульфосоединения (1-10 г/л).
Для получения блестящих медных покрытий предложено большое количество блескообразующих добавок, обеспечивающих зеркальный блеск покрытий, придающих им пластичность и снижающих внутренние напряжения.
При работе с электролитами для получения блестящих покрытий особое внимание следует уделять анодам. Анодный процесс растворения меди достаточно сложен и подробно описан в статье.
Взвешенные частицы шлама
обычно являются причиной грубого шероховатого осадка. Вообще, медное покрытие особенно склонно к дендритообразованию при осаждении с нарушением технологического процесса, к которому относится и присутствие шлама в растворе. Частички шлама становятся при этом центрами кристаллизации и ток, вместо того, чтобы идти на зарождение новых зерен меди, расходуется на обрастание и разрастание этих частиц. Дендриты могут появляться и по другим причинам, одной из которых также является превышение допустимой плотности тока на выступающих частях деталей. Примеры дендритов на медном покрытии приведены на рисунке 2. Пример дендрита на циллиндрическом катоде и поперечный рез такого дендрита приведены на рисунке 3.
Рисунок 2 — Примеры дендритов на медном покрытии.
Рисунок 3 — Пример дендрита на циллиндрическом катоде и поперечный рез такого дендрита.
На качество получаемых блестящих покрытий большое влияние оказывает концентрация ионов Сl—. При пониженной концентрации снижается блеск покрытий и образуются прижоги на острых кромках деталей, при повышенном содержании образуются полосы на покрытиях.
Вредными примесями в
медных сульфатных электролитах являются мышьяк, сурьма, некоторые органические
вещества, образующие коллоидные растворы, анодный шлам.
Кроме сульфатных, используют фторборатные электролиты. Эти электролиты обладают высокой устойчивостью; получающиеся покрытия плотные и мелкокристаллические, рассеивающая способность электролитов примерно такая же, как у сульфатных. Большая растворимость фторбората меди позволяет применять повышенные плотности тока. Из этих электролитов осаждать медь непосредственно на стальные детали нельзя; необходим подслой никеля или меди из цианидных электролитов.
2.2 Процессы в щелочных электролитах меднения.
К щелочным электролитам относятся цианидные, пирофосфатные и этилендиаминовые электролиты. Основные достоинства: высокая рассеивающая способность, получение мелкокристаллических осадков, возможность непосредственно меднить стальные детали.
2.2.1 Цианистое меднение.
Довольно распространены цианидные электролиты. Условия осаждения меди из цианидных электролитов существенно отличаются от условий осаждения в кислых электролитах.
В цианидных электролитах медь находится в составе комплексных ионов, степень диссоциации, а, следовательно, и активность ионов меди очень мала. Поэтому потенциал выделения меди в них примерно на 0,9-1,2 В отрицательнее, чем в сульфатных растворах.
При малом количестве цианида аноды пассивируются. При недостаточном количестве свободного цианида, когда происходит пассивация анодов и на них разряжаются ионы ОН— с выделением кислорода, то не весь образующийся кислород выделяется в виде газа, а часть его расходуется на окисление цианида в цианит. Уменьшение содержания цианидов происходит также из-за взаимодействия их с углекислотой воздуха и образования карбонатов (NaCN → Na2CO3 ).
Содержание свободного цианида оказывает на катодный и анодный процессы противоположное влияние: для катодного процесса требуется минимальное содержание цианидов, для анодного — максимальное. При недостатке свободного KCN на анодах образуется зеленоватая пленка CuCN из-за того, что ионы меди не в состоянии перейти в комплексное соединение. Свободная поверхность анода уменьшается, плотность тока растет, и анодное растворение происходит с образованием ионов двухвалентной меди, которые в виде нерастворимого гидрата осаждаются на аноде. При этом аноды пассивируются и наблюдается интенсивное выделение кислорода.
Основными компонентами медных цианидных электролитов являются комплексный цианид меди и свободный цианид натрия. Из приведенных данных видно, что степень диссоциации комплексных ионов очень мала и уменьшается с увеличением содержания CN— в комплексе. Этим, по-видимому, объясняется повышение катодной поляризации при увеличении содержания свободного цианида в электролите.
Содержание меди в электролите во время работы обычно уменьшается вследствие недостаточной растворимости анодов. Снижение концентрации ионов меди в электролитах приводит к образованию пористых осадков. Кроме того, работая с малоконцентрированными медными электролитами, можно применять только пониженные плотности тока.
Постоянным компонентом цианидных электролитов является карбонат. Он накапливается в результате окисления цианида кислородом воздуха, особенно при нагревании:
2NaCN + 2Н2О + 2NaOH + О2 = 2Na2CO3 + 2NH3
Присутствие карбонатов в небольших количествах полезно, поскольку при этом повышается электропроводность электролитов. Однако при их накоплении свыше 70 г/л, а в концентрированных — до 140 г/л аноды проявляют склонность к пассивированию, а покрытия получаются пористыми. Карбонаты можно удалять при помощи хлорида бария и вымораживанием, охлаждая электролит до -5 °С. Следует отметить, что карбонаты натрия легче выпадают в осадок, чем калиевые. Сульфаты существенного влияния на процесс электролиза не оказывают.
Введение в электролит депассиваторов, в качестве которых применяют сегнетову соль KNaC4H4O6•4H2O и роданид калия KCNS, позволяет повысить рабочую плотность тока и устранить пассивацию анодов, но при этом следует одновременно повышать температуру электролита.
Высококонцентрированные по меди электролиты, содержащие депассиваторы, позволяют применять высокие плотности тока (до 10 А/дм2) при повышенной температуре и перемешивании. При этом возможно получить выход по току, близкий к 100 %.
Сульфиды, вводимые в
электролит, играют роль восстановителя, предупреждая накопление в ванне ионов
меди Cu2+.
Для замены ядовитых цианидных электролитов применяют пирофосфатные и этилендиаминовые электролиты.
2.2.2 Пирофосфатное меднение.
Из пирофосфатных электролитов получают медные осадки с мелкозернистой структурой. При нанесении тонких слоев осадки получаются гладкими, блестящими или полублестящими. Преимущества пирофосфатных электролитов перед кислыми заключаются в высокой рассеивающей способности и возможности непосредственно проводить меднение стальных деталей в разбавленном пирофосфатном электролите.
Основные компоненты пирофосфатных электролитов: CuSO4 или Сu2Р2О7 и К4Р2О7 или Na4P2O7. В растворах в присутствии Na4P2O7 образуется комплексная соль Na6[Cu(P2O7)2]; при избытке свободного пирофосфата может образовываться Na2[Cu(P2O7)2]. Константы нестойкости комплексов [Сu(Р2О7)2]6- и [Сu(Р2О7)2]2- соответственно равны 3•10-3 и 2•10-9.
В щелочных растворах при рН 8 и достаточном избытке свободных ионов Р2О74- медь находится преимущественно в виде шестизарядных комплексных ионов [Сu(Р2О7)2]6-.
В пирофосфатные электролиты вводят NH4NO3, который способствует повышению допустимой катодной и анодной плотностей тока и улучшает качество осадков. Из пирофосфатных электролитов можно получать блестящие осадки. В качестве блескообразующих добавок вводят Na2SeO3 совместно с лимонной или триоксиглутаровой кислотой, 2-меркаптотиазол и другие вещества.
При повышенных плотностях
тока может происходить пассивация анодов за счет образования на их поверхности
труднорастворимой оксидной или солевой пленки.
Катодный потенциал меди в пирофосфатных электролитах имеет более отрицательное значение, чем в кислых. Большая катодная поляризация объясняется пассивированием поверхности катода вследствие адсорбции ионов Р2О74- или образования оксидных (Сu2О8) и труднорастворимых соединений (Сu2Р2О7) в виде фазовой пленки.
Предполагают, что выделение меди на катоде из пирофосфатных растворов происходит в результате восстановления двухзарядных комплексов:
CuP2O72- + 2e—→ Cu + Р2О74-,
образующихся при диссоциации шестизарядных комплексов:
Cu(P2O7)26-↔ CuP2O72- + Р2О74-.
С повышением температуры ускоряется выделение меди, что связано как с ускорением диффузии комплексных анионов к катоду, так и с облегчением их разряда.
Структура осадков меди из пирофосфатного электролита более мелкая, по сравнению с сернокислымирастворами, с ростом плотности тока она укрупняется (рисунок 4)
Рисунок 4 — Микроизображения медного покрытия из пирофосфатного электролита при плотности тока 0,5 А/дм2 (слева) и 1 А/дм2 (справа).
Анодный выход по току в этих электролитах несколько выше катодного, поэтому при корректировке нет необходимости добавлять медные соли. Анодную плотность тока рекомендуется поддерживать в пределах 2-4 А/дм2. При более низкой плотности тока растворение идет недостаточно быстро, при более высокой — на поверхности анодов образуется труднорастворимая оксидная пленка.
Для предотвращения пассивации анодов должно быть достаточное количество свободных анионов Р2О74- и достаточно высокое рН раствора. Повышение температуры способствует отводу продуктов реакции и, следовательно, уменьшению пассивации анодов. Для этой же цели в электролиты вводят депассиваторы, которые способствуют снижению активности ионов Cu2+ в прианодном слое.
При работе пирофосфатных
ванн рекомендуется проводить фильтрацию электролита: для полублестящих
осадков — периодически или непрерывно, для блестящих — непрерывно.
Особенностью
этилендиаминовых электролитов меднения является возможность непосредственного
меднения стальных деталей. Детали в ванну загружают под током плотностью в 3-5
раз превышающей рабочую.
Данная статья является интеллектуальной собственностью ООО «НПП Электрохимия» Любое копирование без прямой ссылки на сайт www.zctc.ru преследуется по закону. Текст статьи обработан сервисом Яндекс «Оригинальные тексты»
Меднение в домашних условиях: технология и материалы

Обработка поверхности различных предметов производится для придания декоративного эффекта или в качестве промежуточной процедуры, предваряющей дальнейшие действия. Многие процессы доступны для выполнения и не требуют большого количества оборудования. Один из наиболее популярных способов обработки — меднение, его можно выполнить и в домашних условиях.
Что представляет собой процесс меднения
Меднение — это процесс нанесения на поверхность предмета тонкого слоя меди. Оно выполняется гальваническим методом, т. е. путем переноса ионов меди от положительно заряженного источника на обрабатываемую поверхность, заряженную отрицательно. Чаще всего процесс гальванического нанесения меди является подготовительным этапом перед покрытием никелем и хромом, но нередко меднение металла становится самостоятельным видом финишной отделки. Широко используется гальванопластика, для которой требуется создать покрытие из меди.

Разновидности меднения
Существует два варианта меднения в домашних условиях:
- С погружением обрабатываемой детали в электролит.
- Без погружения.
С погружением обрабатываемой детали в электролит. Для выполнения процедуры надо иметь емкость с электролитом, имеющую достаточный объем. После предварительной подготовки, состоящей в очистке поверхности наждачной бумагой и промывке в горячем растворе соды, предмет подключается к отрицательному электроду и погружается в электролит на определенное время.

Меднение с погружением детали в электролит
Без погружения. Можно обработать сталь, алюминий, свинец, цинк. Обработка производится без погружения в емкость, обычно такой вариант применяется для крупных деталей.
Оба варианта вполне доступны для самостоятельного выполнения в домашних условиях.

Меднение стали
Оборудование и материалы, необходимые для нанесения медного покрытия
Чтобы выполнять меднение стали или других металлов, придется запастись кое-какими материалами и устройствами. Понадобятся:
- Соляная кислота.
- Медный купорос (сернокислая медь).
- Дистиллированная вода.
- Источник постоянного тока, желательно с регулируемым напряжением (один из вариантов — ЛАТР), но подойдет и обычный трансформатор на 6–12 В.
- Емкость для электролита (оптимально — стеклянный резервуар).
- Две медных пластины, которые могут свободно поместиться в емкость.
- Соединительные провода.
Из воды, медного купороса и соляной кислоты надо изготовить электролит. Сначала в воду добавляется медный купорос, до получения насыщенного раствора. Его надо тщательно перемешивать, чтобы не оставалось твердых частиц. Затем в раствор тонкой струйкой добавляется соляная кислота (не наоборот!). Всего для нанесения покрытия понадобится:
- Вода — 980 г.
- Сернокислая медь — 190 г.
- Серная кислота — 40 г.
Теперь все готово, можно приступать к меднению в домашних условиях.
Внимание! Необходимо учитывать, что соляная кислота — химически активный реагент, поэтому следует запастись средствами защиты — перчатками, очками, максимально подготовить рабочее место.
Технология меднения
Порядок действий при нанесении покрытия:
Схема гальванического меднения
- Надо удалить тонкую пленку окислов с поверхности детали, подлежащей обработке. Используется наждачная бумага, металлическая щетка или иные абразивные материалы. Необходимо действовать очень аккуратно, поскольку сильные повреждения металла останутся заметными. В идеале, поверхность должна быть отполирована.
- Затем изделие тщательно промывается в горячем растворе кальцинированной соды. Это действие позволяет обезжирить поверхность.
- Подготовленное изделие подключается к отрицательному электроду от источника питания и помещается в раствор электролита.
- В раствор электролита опускаются медные пластины с присоединенным к ним положительным электродом от источника питания (анод). Необходимо следить, чтобы анод и катод не соприкасались. В идеале, расстояние между ними должно быть во всех участках одинаковым, но на практике этого сложно добиться.
- Меднение металла производится в несколько приемов. Первый слой покрытия, полученный в течение нескольких минут, рекомендуется удалить и вновь промыть деталь в содовом растворе. Это усилит сцепление слоя омеднения с основным металлом. Деталь выдерживается в растворе около 20–30 минут. Толщина слоя покрытия может достигать 300 мкм.

Схема осаждения металла
Нередко бывает необходимо удалить слой покрытия с хромированных частей. Для этого на деталь подается отрицательный заряд, а на положительный электрод наматывается тряпочка, смоченная в растворе серной кислоты (5%). Ею протирается поверхность детали, слой хромирования снимается. При выполнении процедуры необходимо защищать кожу, органы зрения и дыхания от паров кислоты.
Меднение деталей без погружения в раствор

Меднение алюминиевой детали без погружения в раствор
Гальваническое омеднение может выполняться без погружения детали в емкость с электролитом. Для этого надо подключить к ней отрицательный электрод. В качестве положительного контакта берется медный многожильный провод, конец которого освобождается от изоляции на 1–2 см и разминается так, чтобы получилось некое подобие кисти.
Для нанесения слоя медного покрытия «кисточка» обмакивается в электролит, затем ее концом проводят по поверхности детали, не прикасаясь к ней, но стараясь, чтобы между ними находилась прослойка. Постоянно обмакивая анод в электролит, покрывают слоем меди всю поверхность. Процедура требует навыка и времени, но результат того стоит.
Гальванопластика

Процесс гальванопластики
Покрытие медью может быть выполнено не только на металлических предметах. Широко распространена гальванопластика, когда меднение выполняется по различным засушенным растениям, насекомым и прочим неметаллическим предметам.
Технология нанесения покрытия мало отличается от обычной, только вначале процесса на поверхность надо нанести электропроводный лак. После засыхания лакового покрытия производятся обычные действия по нанесению слоя меди. Полученные изделия обладают высокими декоративными или художественными качествами и высоко оцениваются зрителями.
Видео по теме: Как сделать меднение своими руками в домашних условиях
Меднение в домашних условиях: химическое, гальваническое
В современном мире больше распространение получил медный сплав. Он наносится на поверхность для придания внешней привлекательности различных изделий. Меднение в домашних условиях зачастую проводится для существенного повышения показателя электропроводности. В некоторых случаях рассматриваемый процесс является промежуточной операцией, которая позволяет нанести другое вещество на поверхность.

 Меднение в домашних условиях
Меднение в домашних условияхИспользование меднения
Покрытие медью различных заготовок в последнее время часто проводится в домашних условиях. В большинстве случаев технология применяется для достижения следующих целей:
- Декорирование металла или пластика. Меднение металла в домашних условиях часто проводится для того, чтобы получить старинные на вид изделия, которые пользуются большой популярностью. Специальная процедура состаривания позволяет создать эффект длительного использования изделия. Кроме этого, медь после нанесения напоминает золото. Именно поэтому небольшой слой можно нанести для получения статуэтки или сувенира.
- Гальванопластика. Меднение стали подобным образом также может проводиться в домашних условиях. Суть технологии заключается в создании восковой или пластиковой основы, которая покрывается слоем рассматриваемого сплава. Гальванопластика часто применяется для получения ювелирных изделий или сувениров, матриц и волноводов. Применение специальных материалов позволяет существенно повысить качество покрытия.
- Получение деталей, используемых при создании различных механизмов. Меднение чугуна или другого металла проводят на производственных площадках при различных технологий. Покрытие заготовки медью позволяет существенно повысить электротехнические качества. Подобным образом можно получить клеммы или прочие подобные элементы, которые будут эксплуатироваться под напряжением. Изделия из чистой меди обходятся очень дорого. Именно поэтому часто применяется рассматриваемая технология.


Меднение стали
Меднение пластика в домашних условиях проводится крайне редко, так как подобный материал не выдерживает воздействие высокой температуры. Кроме этого, пластичность основания приводит к появлению структурных трещин.
Особенности меднения в домашних условиях
Меднение металла – особая технология нанесения слоя меди толщиной 1-300 мкм и больше. Особенности применяемых технологий определяют то, что медное покрытие будет прочно держаться на поверхности металла. Среди особенностей, которые приобретает заготовка, отметим следующие моменты:
- Пластичность.
- Высокая электропроводность. Медные изделия хорошо известны с тем, что могут проводить электричество и при этом не нагреваются. Именно поэтому часто создаются изделия, которые покрываются подобным сплавом.
- Более привлекательный вид. Медь блестит на солнце, на поверхности появляются блики.
- В атмосферных условиях сплав легко окисляется и покрывается налетом. Этот момент стоит учитывать при рассмотрении того, где и как именно будет использоваться изделие.
- Медная пленка со временем покрывается пятнами и радужными разводами.


Окисление стали
Обмеднение в домашних условиях может проводиться при применении специального раствора. Стоит учитывать, что процесс предусматривает использование специальных реагентов. Поэтому нужно предусмотреть наличие эффективной приточной вентиляции, а также индивидуальных средств защиты. Меденение пластика несколько отличается, предусматривает применение особой технологии.
Разновидности меднения
Рассматриваемая процедура доступна для выполнения даже новичкам в сфере металлургии. Для получения качественной поверхности нужно знать все особенности процесса. Меднение свинца и других металлов в домашних условиях может проводиться при применении двух различных технологий:
- С погружением в электролит. Подобная технология предусматривает окунание заготовки в подготовленный раствор, после чего подводится напряжение. Зачастую применяется в том случае, если размеры заготовки небольшие, так как требуется меньшее количество специального электролита. Для погружения заготовки требуется ванная или другая емкость, которая не реагирует на воздействие применяемого раствора.
- Без погружения в заранее подготовленную емкость. Она сложна в исполнении, но также позволяет достигнуть высокое качество медной поверхностной пленки.
В обоих случаях предусматривается подвод электричества, за счет чего вещество активизируется.
Наиболее подходящий способ обработки выбирается в зависимости от того, какой нужно достигнуть результат. Примером назовем:
- Получение защитно-декоративного слоя. В этом случае часто проводится смешивание хрома с никелем и медью. За счет подобного сочетания сплавов можно получить надежную поверхность.
- Для защиты поверхности на момент цементирования. Нанесение тонкого слоя меди позволяет защитить заготовку от цементирования. Покрывается раствором поверхность, которая в дальнейшем будет обрабатываться резанием.
- Восстановление и ремонт деталей. При восстановлении хромированных деталей автомобиля и мотоциклов может применяться рассматриваемая технология. При нанесении слоя не более 250 мкм можно скрыть поверхностные дефекты металла.
Обе технологии обработки характеризуются своими определенными особенностями, которые нужно учитывать.
Меднение в растворе с электролитом
Гальваническое покрытие медью в домашних условиях с погружением проводится крайне часто. Подобная технология позволяет получить равномерное покрытие. К особенностям подобного способа обработки можно отнести следующие моменты:
- Для удаления оксидной пленки перед меденением заготовка обрабатывается наждачной бумагой. После этого изделие промывается и обезжиривается горячей смесью из соды. Если не уделить внимание подготовительному этапу, то проводимый процесс не позволит получить устойчивое к механическому воздействие изделие. Металл, который подвержен воздействию коррозии, должен быть хорошо очищен, так как даже мелкая крошка может сделать поверхность неоднородной.
- В банку или другую емкость на медных проволоках опускается две пластины из этого же сплава. Они выступают в качестве анода. Применяемая тара должна быть из стекла.
- Между двумя анодами подвешивается обрабатываемая деталь, которая подключается к минусу, а пластины к плюсу. В качестве источника питания может использоваться батарея, выдающее напряжение 6В.
- Гальваническое меднение предусматривает применение определенного раствора. Он является связующим элементом между деталью и анодами. Раствор для гальванического меднения можно создать изготовить, для чего берется 20 грамм медного купороса и 3 миллилитра серной кислоты. Для разбавления и смешивания этих ингредиентов можно использовать 100 миллилитров дистиллированной воды. При работе с полученным раствором нужно быть крайне внимательным, так как при попадании вещества на открытые участки кожи могут возникнуть ожоги.
- Меднение алюминия медным купоросом в домашних условиях может проводиться только в том случае, если электроды были полностью покрыты раствором. Если они будут находиться в сухом состоянии, то они могут нагреться и расплавиться. При длительной обработке вещество может нагреться и его объем уменьшится.


Гальваническое меднение
При применении рассматриваемой технологии сила тока устанавливается на уровне 15 мА на каждый квадратный сантиметр. На покрытие всей поверхности специальным сплавом, как правило, уходит не менее 20 минут. При увеличении протяженности срока покрытие становится толще.
Меднение без опускания в раствор
Подобный метод применяется для покрытия стали, цинка или алюминия. Покрытие изделия медью в домашних условиях в этом случае проводится проводом, с которого предварительно снимается изоляция для получения своеобразной кисти. Обратный конец провода подключают к плюсу источнику энергии. Химическое меднение в домашних условиях также предусматривает использование специального раствора, который повышает эффективность процесса.
Среди особенностей создания требующего раствора можно отметить следующие моменты:
- Используется раствор медного купороса. Его можно приобрести в специализированных магазинах. Кроме этого, специальный электролит изготавливается при смешивании различных химических элементов.
- Состав немного подкисляют. За счет этого существенно повышается эффективность проводимой процедуры.
Вещество наносится на поверхность, после чего подготавливается металлическая поверхность. Она очищается от загрязняющих веществ, после чего обезжиривается. После этого подготовленная заранее пластина укладывается в ванночку и к ней подводится минус от источника тока.


Меднение алюминия
Подобный процесс предусматривает, чтобы между собранными проводками и пластиной постоянно был слой электролита. За счет этого обеспечивается высокая степень проводимости. Для того чтобы покрыть изделие небольших размеров требуется сего несколько секунд.
После нанесения покрытия изделие сушится на воздухе. Нельзя допускать попадания различных загрязняющих веществ. Следующий шаг заключается в натирании медной прослойки шерстяной тряпкой или другим сукном. В большинстве случаев рассматриваемая технология применяется в том случае, когда изделие имеет большие размеры и не может погружаться в ванную.
Необходимое оборудование
Медное покрытие может наноситься в домашних условиях при применении даже самого обычного оборудования. Установка ванной для проведения рассматриваемой процедуры проводится примерно также, как и гальванических. Стоит учитывать, что существует два типа активных растворов: кислые и щелочные.
При работе может применяться:
- Небольшие медные пластины в качестве электродов.
- Проволока для подачи тока.
- Источник тока, к примеру, АКБ, который рассчитан на подачу тока напряжением 6 В.
- Для регулировки силы тока может устанавливаться реостат.
Меднение алюминия и других сплавов в домашних условиях не требует большого количества времени. Для очистки получаемой поверхности могут применяться различные ткани.
Меднение в домашних условиях: алюминия, стали медным купоросом
Меднение – это процесс нанесения на поверхность медного слоя гальваническим способом.
Медный слой придает изделию внешнюю привлекательность, что позволяет использовать прием гальванического покрытия медью в дизайнерских проектах. Также он придает металлу высокую электропроводность, что позволяет подвергать изделие дальнейшей поверхностной обработке.

Меднение можно использовать в качестве основного процесса для создания поверхностного слоя, а также как промежуточную операцию для дальнейшего нанесения другого металлического слоя. К такому способу можно отнести, например, процесс серебрения, хромирования или никелирования.
Меднение можно проводить в домашних условиях. Это дает возможность решить много бытовых проблем.
Гальваника в домашних условиях: оборудование и материалы
Чтобы выполнить покрытие медным слоем самостоятельно, нужно приобрести необходимое для процесса оборудование и материалы.

Прежде всего, нужно подготовить источник электрического тока. Разные домашние мастера советуют использовать силу тока, разброс которой в большом диапазоне. Работа должна проводиться на постоянном токе.
В качестве источника тока можно взять батарейку КБС-Л напряжением 4,5 вольт или новую батарейку марки «Крона» с рабочим напряжением 9 вольт. Можно также вместо нее использовать выпрямитель малой мощности, дающий напряжение не более 12 вольт, или автомобильный аккумулятор.
Обязательным является использование реостата для регулировки напряжения и плавного выхода из процесса.
Для раствора электролита должна быть заготовлена нейтральная емкость, например из стекла, а также пластиковая широкая посуда, имеющая достаточные размеры для размещения в ней детали. Емкости должны выдерживать температуру не менее 80оС.
Также понадобятся аноды, обеспечивающие покрытие всей поверхности детали. Они предназначены для подведения тока в электролитный раствор и его распределение по всей площади детали.
Для проведения гальваники в домашних условиях понадобятся также химреактивы для приготовления раствора:
- медный купорос,
- соляная или другая кислота,
- дистиллированная вода.
Заготовив все необходимое, можно приступать к работе.
Видео:
Меднение стальных изделий
Меднение стали медным купоросом является одним из основных процессов в области гальваники потому, что оно используется для предварительного покрытия медью. Она отличается высокой адгезией к стальной поверхности, в отличие от других металлов, которые не обладают хорошим сцеплением со сталью. Медный слой при соблюдении технологии держится на стальных изделиях прекрасно.
Есть две технологии нанесения покрытия: с погружением изделия в электролитный раствор и способ неконтактного покрытия поверхности медью без помещения в жидкий электролитный раствор.
Меднение путем погружения в раствор
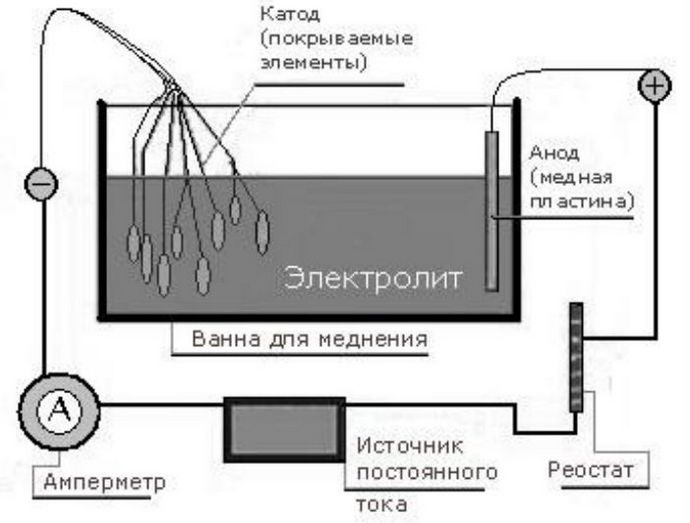
Процесс выполняется с соблюдением следующих этапов:
- С поверхности стальной детали удаляется окисная пленка с помощью наждачной бумаги и щетки, а затем деталь промывается и обезжиривается содой с финишной промывкой водой.
- В стеклянную банку помещаются две медные пластины, подсоединенные к медным проводникам, которые служат анодом. Для этого их соединяют вместе и подводят к положительной клемме прибора, используемого в качестве источника тока.
- Между пластинами свободно подвешивается обрабатываемая деталь. К ней подводится отрицательный полюс клеммы.
- В цепь встраивается тестер с реостатом, чтобы регулировать силу тока.
- Готовится электролитный раствор, в состав которого обычно входит медный купорос – 20 грамм, кислота (соляная или серная) – от 2 до 3 мл, растворенная в 100 мл (лучше дистиллированной) воды.
- Готовый раствор заливается в подготовленную стеклянную банку. Он должен покрыть помещенные в банку электроды полностью.
- Электроды подключаются к источнику тока. С помощью реостата устанавливается ток (10-15 мА должны приходиться на 1см2 площади детали).
- Через 20-30 минут ток отключается, и деталь, покрытая медью, достается из емкости.
Видео:
Покрытие медью без помещения в электролитный раствор
Такой способ используется не только для стальных изделий, но и алюминиевых предметов и изделий из цинка. Процесс осуществляется так:
- Берется многожильный медный провод, с одного конца которого снимается изоляционное покрытие, а проводкам из меди придается вид своеобразной кисточки. Для удобного использования «кисть» закрепляют на ручке — держателе (можно взять деревянную палку).
- Другой конец провода без кисти подсоединяется к положительной клемме используемого источника напряжения.
- Готовится электролитный раствор на основе концентрированного медного купороса с добавлением небольшого количества кислоты. Он наливается в широкую емкость, необходимую для удобного окунания кисти.
- Подготовленная металлическая деталь, очищенная от оксидной пленки и обезжиренная, помещается в пустую ванночку и подсоединяется к отрицательной клемме.
- Кисть смачивается приготовленным раствором и водится вдоль поверхности пластины, не прикасаясь к ней.
- После достижения необходимого медного слоя, процесс заканчивается, а деталь промывается и сушится.
Между поверхностью детали и импровизированной медной кистью всегда должен быть слой из раствора электролита, поэтому кисть необходимо обмакивать в электролит постоянно.
Меднение алюминия медным купоросом
Нанесение на поверхность меди – отличный способ обновления алюминиевых столовых приборов и других изделий из алюминия, используемых дома.
Меднение алюминия медным купоросом можно провести самостоятельно. Упрощенный вариант для демонстрации процесса – это покрытие медью алюминиевой пластинки простой формы.

На этом примере можно потренироваться. Выполнение процесса происходит так:
1. Поверхность пластинки необходимо сначала зачистить, а затем обезжирить.
2. Затем нужно нанести на нее немного концентрированного раствора сернокислой меди (медного купороса).
3. Следующим действием является подсоединение к алюминиевой пластинке провода, подсоединенного к отрицательному полюсу. Подсоединять провод к пластинке можно с помощью обычного зажима.
4. Положительный заряд подается на устройство, состоящее из оголенного медного провода с диаметром от 1 до 1,5 мм, конец которого распределяется между щетинами зубной щетки.
Во время работы этот конец провода не должен касаться поверхности алюминиевой пластины.
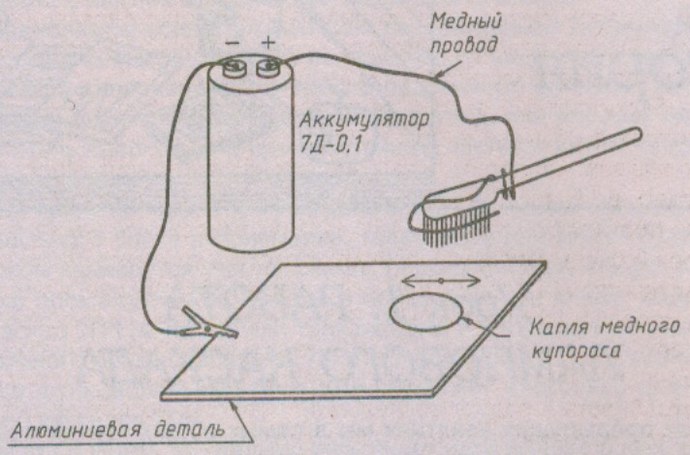
5. Обмакнув щетину в раствор медного купороса, начинают водить щеткой в подготовленном для покрытия медью месте. При этом не нужно допускать замыкания цепи, прикасаясь к поверхности алюминиевой пластины концом медного провода.
6. Омеднение поверхности сразу становится визуально заметно. Чтобы слой был качественным, с окончанием процесса не нужно торопиться.
7. После завершения работы слой меди нужно выровнять дополнительной очисткой, удалив остатки медного купороса и протерев поверхность спиртом.
Гальванопластика в домашних условиях
Гальванопластикой называют процесс электрохимического воздействия на изделие с целью придания ему необходимой формы осаждаемым на поверхности металлом.

Обычно эту технологию используют для покрытия металлом неметаллических изделий. Широко применяют ее в ювелирной области и дизайне бытовых предметов.
Покрытие рабочего изделия должно обладать электропроводящими свойствами. При отсутствии такого слоя сначала предмет покрывают графитом или бронзой.
Основными металлами, используемыми для гальванопластики, являются медь, никель, серебро и хром. Также используют металлизацию поверхностей сплавами из стали.
Гальванопластика в домашних условиях особенно популярна среди мастеров. Чтобы создать нужную форму, с копии делается ее слепок. Для этого используют легко плавящийся металл, графит и гипс.
Видео:
После изготовления формы предмет подвергают покрытию металлом с использованием электролита.
Химическое меднение стальных деталей своими руками
Здравствуйте, уважаемые читатели и самоделкины!Множество различных деталей и инструментов зачастую изготавливают из высокопрочной стали, однако ее поверхность подвержена коррозии. Для защиты от нее изделия покрывают хромом.
Также можно защитить изделия при помощи нанесения слоя меди.
В данной статье, автор YouTube канала «Kovanca Polock» расскажет Вам про химический способ меднения металлических деталей или инструментов.
Этот способ достаточно прост, не потребует электричества, и с легкостью может быть повторен в домашних условиях.
Материалы.
— Медный купорос (100 г)
— Дистиллированная вода
— Средство для мытья посуды на щелочной основе
— Спирт
— Пищевая сода
— Аккумуляторный электролит
— Наждачная бумага, ветошь.
Инструменты, использованные автором.
— Защитные очки из поликарбоната, резиновые перчатки
— Шуруповерт, проволока
— Орбитальная шлифовальная машинка
— Стеклянные баночки, пластиковые миски
— Металлическая губка для мытья посуды.
Процесс меднения стали.
Первым делом мастер приступает к приготовлению рабочего раствора.
Использование защитных очков и резиновых перчаток настоятельно рекомендуется!
Основным реагентом послужит обычный медный купорос, который можно приобрести в цветочном магазине.
В стеклянную банку объемом 0,5 литра наливается 150 мл теплой воды (около 40 градусов). В нее засыпается 100 гр. купороса.
Для ускорения растворения кристаллов купороса автор изготовил простую мешалку из проволоки, загнув ее конец в кольцо. Эта мешалка зажимается в патроне шуруповерта, и ей перемешивается раствор до полного растворения купороса.
В отдельной емкости отмеряется 250 мл электролита для свинцовых аккумуляторов.
Электролит представляет собой раствор серной кислоты с водой в пропорции 60:40.
Далее, в раствор купороса добавляется 50 мл медицинского спирта. После перемешивания заливается 250 мл электролита. Состав еще раз перемешивается.
При работе с электролитом следует быть очень осторожным. Можно получить химические ожоги. При попадании на кожу следует сразу же обработать ее раствором соды (далее он также будет применяться, и его следует приготовить заранее).
Также потребуется подготовить два промывочных состава. В две разные емкости наливается по литру чистой воды.
В первой емкости растворяется пара столовых ложек пищевой соды. Этот раствор потребуется для нейтрализации кислоты.
Во второй миске нужно растворить 2-3 ложки порошкообразного чистящего средства на щелочной основе.
Первым испытуемым послужит стальная профильная труба. Мастер предварительно зачистил ее поверхности мелкозернистой наждачной бумагой при помощи орбитальной шлифовальной машинкой. Чем лучше будет подготовлено изделие, тем качественнее получится меднение поверхностей.
Теперь, используя металлическую губку для мытья посуды, поверхности изделия обезжириваются в щелочном растворе моющего средства.
Заготовка вытирается насухо, и несколько раз на несколько секунд опускается в рабочий раствор. Тончайший слой меди образуется практически мгновенно.
После этого мастер промывает деталь в растворе соды, нейтрализуя серную кислоту.
Затем этот процесс повторяется несколько раз, начиная с обработки в щелочном, окунанием в рабочий, и заканчивая промывкой в содовом растворах.
Для демонстрации качества полученного покрытия, автор натирает обработанную поверхность металлической губкой с большим усилием. Небольшие царапины конечно образуются, но при этом целостность медного слоя не нарушается.
Теперь автор покажет способ меднения оцинкованных инструментов на примере торцевого гаечного ключа. При этом он единожды обезжирил его поверхность, и будет только периодически нейтрализовывать кислоту в содовом растворе.
Напоследок автор покрыл медью сложную металлическую деталь в виде кованой дверной ручки. Ее он выдержал в течение нескольких минут в рабочем растворе.
Вот такие отличные результаты меднения металлических изделий получились. Теперь можно полировать поверхности.
Слой меди сможет защитить инструменты от коррозии, однако такая поверхность со временем потемнеет, и покроется патиной. Также возможно позеленение некоторых участков. Именно поэтому после медного слоя выполняется хромирование.
Выполнить его без применения гальваники и спецрастворов затруднительно, поэтому можно нанести слой лака.
Кстати говоря, образование патины на различных декоративных кованых элементах даже придаст им особый шарм.
Благодарю автора за простой и доступный способ меднения металлических поверхностей!
Всем хорошего настроения, крепкого здоровья, и интересных идей!
Авторское видео можно найти здесь.
Источник (Source)
Покрытие медью | Меднение Услуги
Быстрые ссылки
Возможности нанесения покрытия | Характеристики покрытия | Соображения | Часто задаваемые вопросы
Услуги по медному покрытию
Медь — это металлический элемент красно-оранжевого цвета, известный своей высокой электропроводностью, пластичностью и стойкостью к коррозии. Эти свойства делают медь популярным выбором для покрытия компонентов в широком спектре отраслей — от аэрокосмической и автомобильной до электроники и телекоммуникаций.
Если вы ищете компанию, которая может предоставить услуги по нанесению покрытий медью, которые помогут вашему бизнесу снизить затраты, сократить время выполнения заказа и производить высококачественную продукцию в соответствии со строгими требованиями, компания Sharretts Plating Company может вам помочь. В SPC мы предоставляем гальваническое покрытие меди и другие услуги по медному покрытию в соответствии с вашими потребностями.

Возможности и методы нанесения покрытия
Мы можем наносить медные покрытия различной толщины на ряд основных материалов и типов продукции.Вот некоторые из используемых нами методов:
- Гальваника: При гальванике меди металлическую подложку помещают в электролитическую ванну, и электрический ток используется для прилипания ионов меди к поверхности основного материала. В результате на поверхности появляется тонкий слой меди.
- Покрытие ствола: Этот высокоэффективный тип гальваники позволяет SPC одновременно покрывать медью многие мелкие детали. Для достижения наилучших результатов компания SPC разрабатывает большую часть оборудования для нанесения покрытий на стволы собственными силами.
- Покрытие без применения электролита: Покрытие без применения электролита использует чисто химический процесс без внешнего источника энергии для создания металлического покрытия. Этот метод позволяет получать покрытия, которые имеют тенденцию быть менее пористыми и более устойчивыми к коррозии, что делает его идеальным для продуктов, которые будут подвергаться воздействию сложных условий.
- Гальваника стойки: Гальваника стойки рекомендуется, когда технические характеристики покрытия сложны и должны выполняться строгие требования к испытаниям.Мы можем вместить как опытные образцы, так и серийное производство.
- Плотное покрытие: Плотное покрытие создает более толстое покрытие, чем другие методы. Толщина толстого покрытия обычно превышает 0,001 дюйма. Например, пластинчатые боеприпасы часто имеют толстую пластину толщиной 0,020 дюйма.
Помимо металлов, SPC может обеспечить меднение для пластмасс, керамики и некоторых гибридных материалов.
Технические характеристики медного покрытия
В зависимости от отрасли вам может потребоваться, чтобы ваши продукты соответствовали определенным спецификациям или ожиданиям в отношении контроля качества.Следующие характеристики относятся к изделиям с медным покрытием:
- MIL-C-14550A: В этой спецификации изложены требования к адгезии, испытаниям и минимальной толщине медного покрытия, используемого для различных применений в вооруженных силах США.
- ASTM B734-97: Эта спецификация устанавливает стандарты для гальваники меди для инженерных целей, таких как прекращение термообработки и поверхностное упрочнение.
Рекомендации по нанесению гальванических покрытий на медь
Хотя медь является высокоэффективным гальваническим раствором во многих ситуациях, некоторые специфические свойства меди накладывают определенные ограничения на ее использование.Поскольку медь является высокоактивным металлом, она не идеальна для прямого покрытия железом, если сначала не будет нанесено базовое покрытие из никеля.
Также может потребоваться использование раствора цианида в сочетании с раствором меди для обеспечения максимальной адгезии. Цианид очень токсичен, поэтому во время процесса меднения важно проявлять большую осторожность. Медь также имеет относительно тусклый цвет, что означает, что могут потребоваться другие добавки, если требуется более яркая отделка.
Процесс гальваники меди состоит из множества основных этапов, обеспечивающих получение высокофункционального готового продукта.Пункты, которые следует учитывать при размещении заказа на меднение, включают требования к покрытию, процедуры отбора образцов и испытаний, а также окончательную браковку, повторное слушание или сертификацию.
Медное гальваническое покрытие на пластике
Гальваническое покрытие медью можно наносить на пластмассовые и другие неметаллические поверхности, существенно «металлизируя» пластмассовые детали. Меднение на пластиковых подложках часто используется для придания пластику электропроводности, что является первоочередной задачей в электронной промышленности. Медное покрытие пластика также может укрепить деталь и придать ей блеск, что сделает ее более эстетичной, что может быть важно для некоторых применений.
В SPC мы можем использовать гальваническое покрытие меди для покрытия основных материалов из:
- АБС
- тефлон
- Поликарбонат
- Нейлон, армированный минералами
- И более
Часто задаваемые вопросы по медному покрытию
Найдите ответы на распространенные вопросы о меднении.
Что такое гальваника меди?
Гальваника меди — это метод нанесения покрытия, при котором используется постоянный электрический ток для осаждения растворенной меди на поверхности изделия.
Каковы преимущества гальваники медью?
Хотя гальваническое покрытие может использоваться для многих различных типов металлических покрытий, гальваническое покрытие меди имеет несколько явных преимуществ. Медь является отличным проводником электричества, поэтому вы можете использовать гальваническое покрытие меди, чтобы улучшить проводимость основного материала. Медь также обладает высокой податливостью, что делает ее идеальной для изгибающихся компонентов и обеспечивает хорошую защиту от коррозии.
Какова история гальваники меди?
Хотя процесс гальваники со временем развивался и улучшался, гальваника меди не нова.Рудиментарные варианты гальваники были разработаны в начале 19 века.
В каких приложениях используется гальваника меди?
Многие отрасли промышленности полагаются на медное гальваническое покрытие в электротехнике, промышленности и обогреве из-за проводимости и тепловых свойств материала. Медное гальваническое покрытие можно также использовать в качестве грунтовки перед нанесением других покрытий или в качестве обработки поверхностей перед пайкой.
Производители могут покрывать пластмассовые компоненты или изделия медью для улучшения характеристик.Вы можете найти гальваническое покрытие меди на полупроводниках, печатных схемах и многом другом.
Почему выбирают компанию Sharretts Plating?
SPC обладает более чем 80-летним опытом предоставления услуг по меднению для промышленных и коммерческих клиентов. Мы работаем, чтобы удовлетворить потребности вашей отрасли, используя строгий процесс контроля качества от начала проекта до момента доставки. Чтобы узнать больше о том, как мы можем удовлетворить ваши требования к медному покрытию или запросить ценовое предложение, свяжитесь с нами сегодня.
Дополнительные ресурсы:
.Меднение стали в домашнем магазине
60000 тем вопросов и ответов — образование, алоха и развлечениятема 30852
Обсуждение началось в 2001, но продолжаться до 2020 года
2001 г.В. Я делаю рамы из квадратных стальных труб 4 на 4 дюйма длиной 20 футов и плоских стальных 4 на 8 футов для монтажа внешних электрических сетей для моего рыбоводного хозяйства. Я пробовал горячее цинкование на дюжине, но деформирование было проблемой. Я тоже покрасил некоторые, но краска действует как электрический изолятор и затрудняет хорошее заземление.
Меднение — практическое решение? Я работаю с новой сталью, у меня есть пескоструйный аппарат и мойка высокого давления с горячей водой (иногда ошибочно называемая паровой машиной), и я привык работать с соляной кислотой. [аффил. ссылка на информацию о продукте на Amazon] , и сульфат меди тоннами, но я не желаю подвергать себя или свою ферму каким-либо действительно едким или ядовитым растворам.
Если это возможно, где бы я мог найти информацию и оборудование для низкотехнологичного предприятия по меднению.
Билл К. [фамилия удалена редактором в целях конфиденциальности]farm — Greensboro, Alabama
A. Привет, Билл.
Медь, вероятно, не лучший выбор, потому что она потускнеет, подвергнется коррозии и станет непроводящей (возможно, вы видели зеленые или коричневые медные крыши). Когда вы видите не корродированную медь, это потому, что она имеет лаковое (изолирующее) покрытие. Никелирование, вероятно, лучший выбор.
Вы можете знать, а можете и не знать, что мастерские по нанесению покрытий распространены повсеместно, и вы, вероятно, можете найти в вашем районе уже существующий магазин, чтобы покрыть эти обрамления для вас, если вы хотите пойти по этому пути.
Гальваника как детский научный эксперимент очень проста — третьеклассники проводили эксперименты в нашем FAQ «Как работает гальваника». Но прочная, функциональная обшивка — это совсем другое. Одна из проблем заключается в том, что большинство покрытий (исключение составляет цинкование) более благородно, чем сталь, поэтому, если есть какая-либо пористость или точечные отверстия, покрытие вызывает быструю коррозию основного металла стали, чтобы защитить его. На этой фотографии показана никелированная стойка для бара, предназначенная для использования в помещении после в один прекрасный день на улице =>
Я бы посоветовал поиграться с гальваникой, если хотите, и повеселиться (используйте сульфат меди и немного соляной кислоты, если вы уже знаете, как с ними безопасно обращаться), но присылайте свои настоящие детали в гальванический цех 🙂
Удачи и всего наилучшего,
Тед Муни, П.E.
finish.com — Пайн-Бич, Нью-Джерси
Стремление к жизни Алоха
2004
В. Я хочу покрыть медью некоторые стальные фигурки для наружного освещения. Удастся ли мне использовать ваши методы и экспериментировать в более широком масштабе? Фигуры из тяжелой стали, около 6 дюймов в высоту. У меня есть медная электрическая шина из коммунальной промышленности, которую я хотел использовать для анода, и тяжелое зарядное устройство на 12 вольт типа Booster [ссылка на информацию о продукте на Amazon] снабдить ток.Могу ли я использовать это, чтобы растворить достаточно меди в солях, чтобы адекватно покрыть фигуры? Сколько и какого типа соли потребуется примерно на 1 галлон раствора для покрытия? Кроме того, где я могу найти соли? Это моя первая встреча с гальваникой. Я понимаю процесс, но у меня не так много оборудования для работы. Я хочу попробовать это только для некоторых орнаментальных фигур — любая помощь будет признательна. Был бы медный купорос [аффил. ссылка на информацию о продукте на Amazon] кристаллы, растворенные в воде, могут быть вам полезны?
Дуэйн Ви [фамилия удалена редактором для конфиденциальности]любитель — Абилин, Техас
2004 г.
А.Привет, Дуэйн. Вы понимаете принцип наших инструкций по научному проекту по гальванике, но, вероятно, не совсем понимаете его реальные ограничения 🙂
Вы можете заставить электроны перемещаться от одного полюса к другому с помощью аккумулятора или выпрямителя (или зарядного устройства), и таким образом вы можете заставить металл, находящийся на одном полюсе, растворяться в ионизированном состоянии в водном растворе, переносить эти ионы через раствор, и преобразовать их обратно в металлическое состояние на другом полюсе, перемещая металл от одного полюса к другому.Это очень полезные знания для студентов, помогающие им понять принципы химии и электричества и позволяющие им увидеть их в действии — вот почему мы подготовили и разместили эксперимент. Но, извините, к сожалению, этот эксперимент не слишком приближает домовладельца / любителя к успешному гальваническому покрытию меди как функционального покрытия на фигурах из стали / железа 🙂
«Функциональный» — ключевое слово. Вы не можете успешно гальванизировать функциональное покрытие на стали / железе простой солью меди, такой как сульфат меди или ацетат меди (раствор уксуса), в первую очередь потому, что оно будет «погружаться в осадок» (вспомните урок класса естественных наук, где вы бросаете гвозди в сульфат меди, и они сами покрывают медью пластину без электричества) и не будут иметь адгезии.Чтобы получить функциональное, липкое покрытие, вам нужно начать сначала с другого раствора для нанесения покрытия (раствор цианидного меднения), который слишком опасен для домашнего использования, или с запатентованного раствора пирофосфата меди. Покрытие ученика не будет мелкозернистым, оно не будет беспористым, оно не будет ярким, оно не будет постоянной толщины, оно не будет ложиться на углубления ваших фигурок.
Удачи и получайте удовольствие, но не делайте этого с цифрами, если они представляют для вас ценность, пока вы не проведете много экспериментов — вместо этого отправьте их в гальванический цех, который может использовать правильный химический состав на основе цианида. для реальных приложений, в отличие от демонстраций научного класса.Удачи!
.Медное покрытие пластмасс — Sharretts Plating Company
Оглянитесь вокруг дома или офиса, и вы, несомненно, увидите что-то, что сделано из меди или содержит ее. Этот обильный и чрезвычайно универсальный металл играет важную роль в существовании человека на протяжении более 10 000 лет. Хотя медь больше не является основным ингредиентом пенни, который до 1982 года состоял на 95% из меди (теперь они сделаны из цинка с медным покрытием), этот мягкий красновато-коричневый металл является основным компонентом многих производственных и промышленных процессов.Основные области применения меди включают электропроводку, сантехнику, кровлю и промышленное оборудование. Медь также широко используется в гальванической промышленности.
Что такое медь?
Медь — это природный химический элемент, который добывают из земной коры. Добытые месторождения сульфида меди содержат около одного процента меди. Извлеченная медь относительно мягкая, что отчасти объясняет наличие одной из ее наиболее заметных характеристик: отличной электрической и теплопроводности.В этих двух областях медь уступает только серебру; однако он намного дешевле серебра. Медь также естественно устойчива к коррозии. Он вступает в реакцию с кислородом атмосферы, образуя слой оксида меди, который защищает от ржавчины. Однако под воздействием сульфидов медь потускнеет.
История использования меди
В то время как люди использовали медь около 10 000 лет, фактический процесс извлечения меди из ее руд начался приблизительно 7 000 лет назад.Людям потребовалось еще 2000 лет, чтобы обнаружить, что мягкую медь можно усилить, сплавив ее с другими металлами. Первым известным сплавом, созданным людьми, была бронза, которая представляет собой комбинацию меди и до 25% олова. Это привело к тому, что стало известно как бронзовый век, когда многие инструменты, посуда и другие изделия были сделаны из бронзы. Латунь, представляющая собой сплав меди и цинка, была впервые разработана около 2500 лет назад.
На протяжении веков медь использовалась во многих целях.Древние римляне использовали медь, добываемую на Кипре, в качестве валюты. На самом деле химический символ меди Cu произошел от латинского слова «cuprum», что означает «с острова Кипр».
Шведы использовали медную валюту для финансирования своих военных действий в 17 веках. Медь также стала материалом, излюбленным многими скульпторами в период Возрождения. Дагерротип, предшественник современной фотографии, созданной в 19 веках, состоял из куска посеребренной меди.Статуя Свободы была даже вылеплена из меди французским скульптором Гюставом Эйфелем.
Гальваника меди
Гальваника меди на другие металлы уже много лет является широко распространенной промышленной практикой. Гальваника — это процедура, при которой металлическая деталь, известная как подложка, помещается в раствор электролита. Затем в ванну для нанесения покрытия подается электрический ток, который наносит тонкое металлическое покрытие на поверхность подложки. Гальваника может использоваться для ряда целей, таких как повышение коррозионной и износостойкости, улучшение электрической и теплопроводности, добавление эстетической привлекательности и улучшение адгезии.Три основных типа гальваники меди включают:
- Щелочной цианид: Ванна щелочного цианида меди обеспечивает отличную метательную способность и однородную толщину отложений. Однако цианидный компонент делает этот раствор чрезвычайно токсичным, и с ним необходимо обращаться с особой осторожностью.
- Щелочные нецианиды: В настоящее время доступны нетоксичные растворы для нанесения покрытий, не содержащие цианидов. Однако они могут быть не такими эффективными, как щелочные цианистые ванны во всех случаях меднения.Например, использование щелочного раствора, не содержащего цианида, во время гальванического покрытия цинкового литья под давлением может привести к образованию неприлипающих отложений меди, что по существу сделает всю процедуру неэффективной.
- Кислотная медь: Кислотная ко
Покрытие медью для различных металлов — Гальваника — EPi
Щелочной нецианидный процесс
Формула E-Brite 5.0 Cu решает проблему погружения в покрытие медного цилиндра. Он наносится непосредственно на цинковую отливку (zamac), и полученное покрытие прилипает к отливке.
Обладает равномерным распределением низкой плотности тока и превосходной рассеивающей и укрывной способностью, особенно в областях с низким током, и по этим свойствам превосходит цианидную медь.E-Brite 5.0 Cu образует непористый, мелкозернистый, гладкий и плотный пластичный медный осадок.
Можно дополнительно покрыть медью или никелем до необходимой толщины.
Документация
Сопутствующие товары
E-Kleen 163
Концентрированное жидкое нейтральное средство для замачивания на основе фосфатов, комнатная температура.Очищает водорастворимые масла и нефтепродукты и …
E-Kleen 173
Слабощелочная порошкообразная смесь, используемая в качестве электролитического и пропитывающего очистителя. Содержит сильно обогащенные поверхностно-активные вещества, …
E-Pik 216
Слабокислый жидкий концентрат, используемый для подготовки литых цинковых поверхностей к нанесению покрытия.Специально разработан для использования с EPi …
Электронный Брайт 757
Яркий процесс E-Brite 757 — это однокомпонентный процесс, который дает блестящие белые отложения высокой четкости, отражательной способности и …
Свернуть информацию .